Clear Sky Science · de
Onkogene PI3Kα-Varianten zeigen ein abgestuftes Konformationsspektrum mit mutationsspezifischen verborgenen Taschen
Wenn eine einzelne DNA-Änderung nicht ausreicht
Krebs wird oft als eine Erkrankung von Mutationen beschrieben, doch diese Studie zeigt, dass nicht alle Mutationen allein wirken. Die Forschenden untersuchten ein zentrales wachstumssteuerndes Enzym, PI3Kα, und fanden heraus, dass wenn zwei spezifische DNA-Änderungen gemeinsam in derselben Kopie seines Gens auftreten, sie dieses Protein in aktivere Konformationen drängen können als jede einzelne Veränderung allein. Das ist wichtig, weil überaktive PI3Kα nicht nur Krebs antreibt, sondern auch bei gutartigen Überwuchssyndromen und Entwicklungsstörungen des Gehirns eine Rolle spielt – und es hilft zu erklären, warum manche Tumoren schlecht auf aktuelle Medikamente ansprechen.
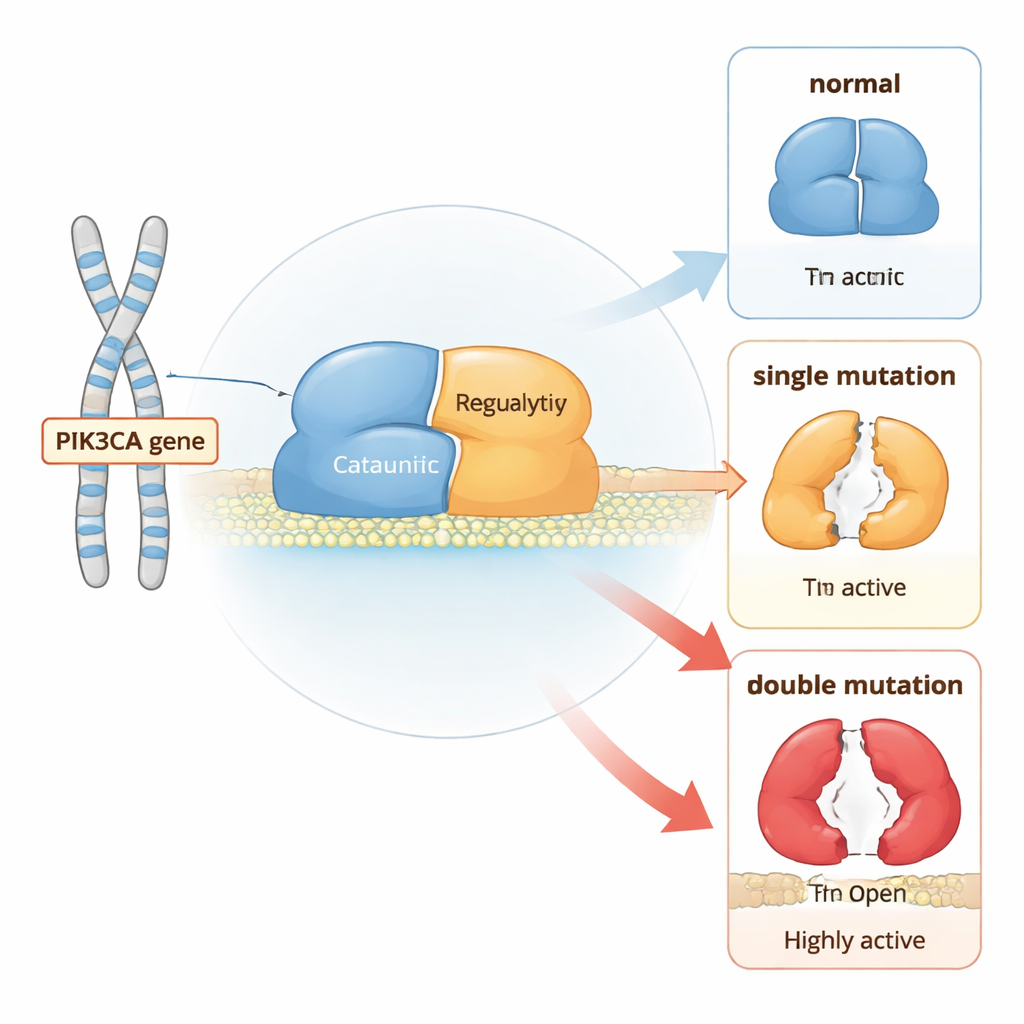
Ein molekularer Schalter für Zellwachstum
PI3Kα ist ein zweiteiliges Protein, das nahe der Zellmembran sitzt und Wachstumssignale weiterleitet. Unter normalen Bedingungen bleibt es größtenteils in einer „aus“-Position, bis Rezeptoren an der Zelloberfläche stimuliert werden. Dann bewegt sich PI3Kα zur Membran und wandelt ein Lipid namens PIP2 in PIP3 um, das der Zelle signalisiert zu wachsen und sich zu teilen. Um unkontrolliertes Wachstum zu verhindern, wirken mehrere Bereiche des Proteins wie eingebauter Bremsen: eine Region klemmt den katalytischen Kern fest, eine andere hält eine flexible Aktivierungsschleife nahe, und eine Partneruntereinheit hilft, den gesamten Komplex in Schach zu halten.
Wie Einzel- und Doppelmutationen das Gleichgewicht kippen
Mithilfe langer, atomarer Computersimulationen verglichen die Autoren die normale PI3Kα mit Varianten, die entweder einzelne „Hotspot“-Krebsmutationen oder Kombinationen eines Hotspots mit einer schwächeren Mutation im selben Molekül tragen. Sie fanden heraus, dass jede Mutation beeinflusst, wie oft das Protein offenere, aktivere Formen aufsucht, aber Doppelmutanten verschieben das Gleichgewicht deutlich stärker als einzelne Veränderungen. Insbesondere arbeiten einige Mutationspaare zusammen, um die Kontakte zu lockern, die ein regulatorisches Element (nSH2) an seinem Platz halten, und um ein anderes Segment (iSH2) von seiner Andockstelle wegzuschieben. Diese koordinierte Bewegung entriegelt den katalytischen Kern, wodurch es dem Protein leichter fällt, zur Membran zu wandern und die Signalübertragung zu starten.
Wie das Substrat die Reaktionsstelle erreicht
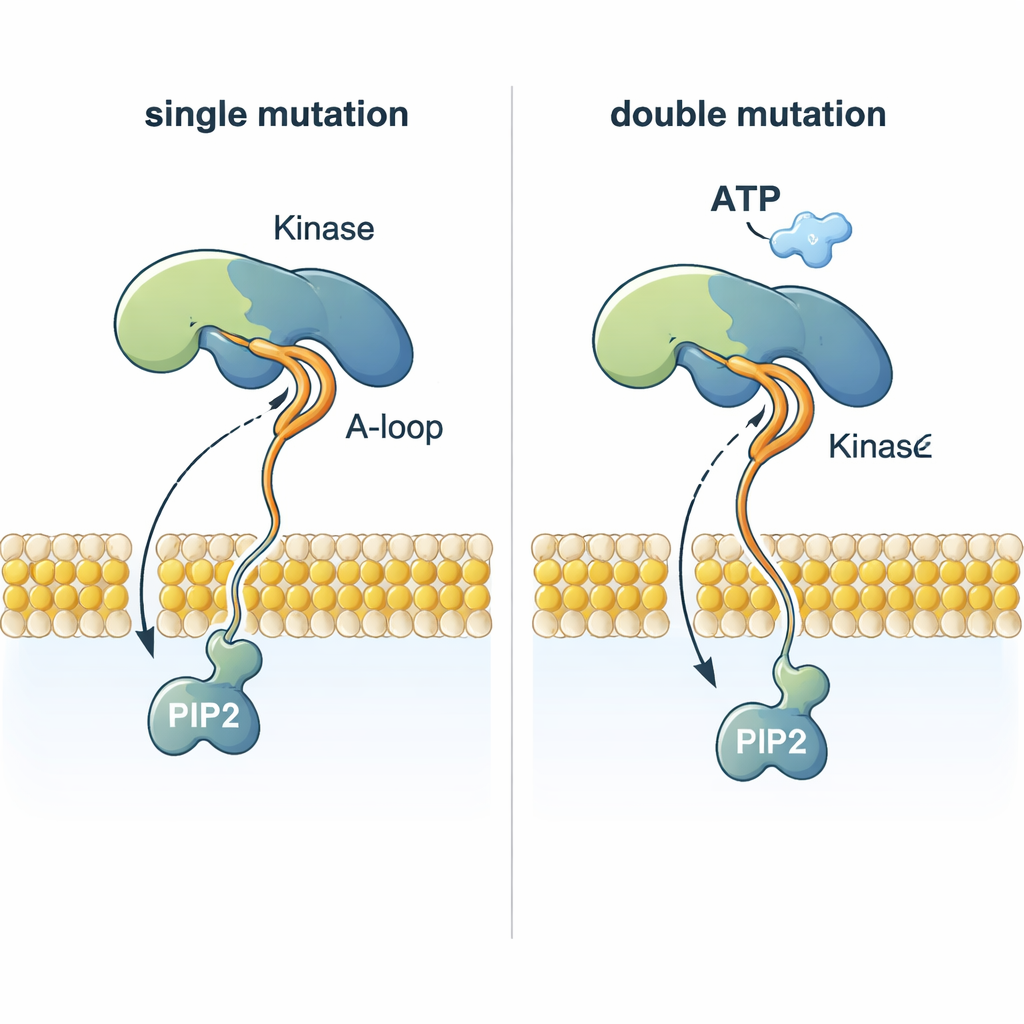
Ein auffälliges Rätsel ist, wie PI3Kα eine Phosphatgruppe von ATP — das fast 2 Nanometer über der Membran liegt — auf PIP2 übertragen kann, das in die Membran eingebettet ist. Die Simulationen zeigen, dass bestimmte Mutationen eine flexible Aktivierungsschleife so umformen, dass ein stark positiv geladener Abschnitt Richtung Membran hervortritt. Diese Schleife kann den negativ geladenen Kopf von PIP2 erfassen, ihn aus der Lipidschicht herausziehen und zur Position des ATP führen. Doppelmutanten, die eine membranverankernde Mutation mit einer verändernden Mutation in dieser Schleife kombinieren, koordinieren PIP2 deutlich effizienter als normale PI3Kα oder Einzelmutanten, was eine strukturelle Erklärung dafür liefert, warum Tumoren mit zwei PI3Kα-Mutationen besonders aggressiv sein können.
Verborgene Wirkungsstellen durch Bewegung aufgedeckt
Weil PI3Kα groß und flexibel ist, hat ein einzelnes Medikament, das auf seine aktive Stelle zielt, oft Schwierigkeiten, gegen alle Mutantenformen wirksam zu sein, und kann Nebenwirkungen wie schwere Veränderungen des Blutzuckers verursachen. Indem die Forschenden verfolgten, wie das Protein über die Zeit „atmet“ und sich verformt, entdeckten sie „kryptische" Taschen — temporäre Vertiefungen, die sich nur in bestimmten Mutationskonformationen öffnen und in statischen Kristallstrukturen unsichtbar bleiben. Diese Taschen treten an mutationsspezifischen Orten auf, beispielsweise in der Nähe von Bereichen, die sich bei bestimmten Doppelmutanten besonders stark bewegen. Das legt nahe, dass sorgfältig entwickelte allosterische Wirkstoffe, die abseits der aktiven Stelle binden, darauf ausgelegt werden könnten, einzelne Mutantenvarianten in sicherere, weniger aktive Konformationen zu sperren.
Auf dem Weg zu klügeren Kombinationstherapien
Insgesamt stützt die Arbeit die Sichtweise eines „One-Two-Punch“ in der Krebsgenetik: Eine starke Hotspot-Mutation plus ein schwächerer Partner im selben PI3Kα-Molekül können ein abgestuftes Spektrum aktiverer Formen erzeugen, das oft mit schwereren klinischen Verläufen verbunden ist. Für die Therapie argumentieren die Autoren, dass es statt der Abhängigkeit von einem einzelnen Inhibitor effektiver sein könnte, Wirkstoffe zu kombinieren, die unterschiedliche Taschen anvisieren — eine an der aktiven Stelle und eine oder mehrere allosterische Stellen, die nur in spezifischen Mutanten existieren. Solche Cocktails könnten prinzipiell die PI3Kα-Aktivität präziser dämpfen, toxische Nebenwirkungen reduzieren und die Behandlung besser an das genaue Mutationsmuster des Tumors eines Patienten anpassen.
Zitation: Jang, H., Yavuz, B.R., Zhang, M. et al. Oncogenic PI3Kα variants reveal graded conformational spectrum with mutation-specific cryptic pockets. Commun Chem 9, 100 (2026). https://doi.org/10.1038/s42004-026-01906-x
Schlüsselwörter: PI3K alpha, onkogene Mutationen, allosterische Inhibitoren, molekulare Dynamik, Signaltransduktion