Clear Sky Science · de
Sequenz- und Längenskalen-abhängige Dynamik in Biokondensaten hoch geladener unstrukturierter Proteine
Warum winzige Proteintröpfchen wichtig sind
In unseren Zellen finden viele lebenswichtige Reaktionen in weichen, tropfenähnlichen Strukturen ohne umgebende Membran statt. Diese „biomolekularen Kondensate“ verhalten sich wie kleine flüssige Kompartimente und bestehen häufig aus flexiblen, stark geladenen Proteinen. Experimente haben gezeigt, dass sich Moleküle in einigen dieser Tröpfchen überraschend schnell bewegen können, obwohl die Tröpfchen als Ganzes recht dickflüssig und klebrig erscheinen. Dieser Artikel behandelt eine einfache, aber wichtige Frage: Wie steuert die genaue Reihenfolge positiver und negativer Ladungen entlang dieser Proteine, wie schnell sich Dinge innerhalb solcher Tröpfchen bewegen?
Tröpfchen aus flexiblen geladenen Ketten bauen
Die Autoren konzentrieren sich auf intrinsisch ungeordnete Proteine — lange, flexible Ketten, die keine starren Faltungen einnehmen. Viele dieser Ketten tragen sowohl positive als auch negative Ladungen, in unterschiedlichen Mustern entlang ihrer Länge. Mithilfe groß angelegter Computersimulationen erzeugte das Team Modelltröpfchen aus zahlreichen Kopien solcher Proteine sowie Wasser und kleinen Ionen, um das dichte Innenleben realer Kondensate nachzubilden. Sie variierten systematisch, wie „blockig“ das Lademuster war, von Sequenzen, in denen sich positive und negative Ladungen abwechseln, bis zu Sequenzen, in denen alle positiven Ladungen zusammengefasst und alle negativen Ladungen in einem separaten Block gruppiert sind.
Wassergehalt und Fluidströmung prägen die Bewegung
Die Simulationen zeigten, dass diese Tröpfchen trotz hoher Wasseranteile — je nach Lademuster zwischen etwa 55 % und 84 % — wie echte Flüssigkeiten wirken können. Diese Wassermenge bedeutet, dass Fluidströmungen oder Hydrodynamik nicht vollständig unterdrückt sind, wie es viele Theorien für dichte Polymersysteme vorhersagen würden. Durch die Verfolgung der Wanderung von Proteinesegmenten über die Zeit fanden die Autorinnen und Autoren Bewegungsmuster, die typisch sind für Ketten, deren Bewegung durch das umgebende Fluid unterstützt wird, statt allein durch Reibung stark gebremst zu werden. Dieser hydrodynamische Einfluss reicht bis hinauf und sogar über die Größe einer gesamten Proteinkette hinaus, insbesondere in Tröpfchen aus Sequenzen mit gemischteren Ladungen und dadurch mehr Wasser.
Lokale Lademuster steuern mikroskopische Flexibilität
Bei genauerem Hinsehen untersuchten die Autoren, wie kurze Abschnitte jeder Kette im Tröpfchen entspannen und sich neu anordnen. Verschiedene Bereiche desselben Proteins, die dieselbe Anzahl von Bausteinen enthalten, konnten je nach ihrem lokalen Mix aus positiven und negativen Ladungen sehr unterschiedlich schnell bewegen. Abschnitte mit ausgeglichener Ladung entspannten schneller, während von einer Ladungsart dominierte Bereiche träger waren. Überraschenderweise blieben diese Unterschiede stark, obwohl einfache Screening-Überlegungen vorhersagen würden, dass elektrostatische Effekte unter den salzigen, dichten Bedingungen nur kurzreichweitig sein sollten. Die Studie zeigt, dass das Verknüpftsein der Ladungen entlang einer Kette langreichweitige elektrische Korrelationen bewahrt, die die lokale Bewegung stark beeinflussen.
Die Viskosität hängt von der Größe des Messprobes ab
Das Team fragte dann, wie „dick“ sich diese Tröpfchen auf unterschiedlichen Längenskalen anfühlen. Mithilfe einer Methode, die winzige Wellenbewegungen im Impuls des Fluids mit seinem Strömungswiderstand verknüpft, berechneten sie eine Längenskalen-abhängige Viskosität. Bei allen Sequenzen erscheint die Flüssigkeit auf sehr kleinen Skalen dünnflüssiger und auf der Skala des gesamten Tröpfchens dicker. Diese Größenabhängigkeit ist besonders ausgeprägt bei den blockigen Lademustern: Für das am stärksten segregierte Muster ist die Makroskalenviskosität mehr als zwanzigmal höher als die lokale, monomernahe Viskosität. Im Gegensatz dazu zeigen Tröpfchen aus gut gemischten Sequenzen eine deutlich kleinere Lücke. Insgesamt steigt die makroskopische Viskosität steil mit der Proteinkonzentration an, ähnlich wie bei dichten neutralen Polymersystemen, obwohl die Proteine selbst stark geladen sind.
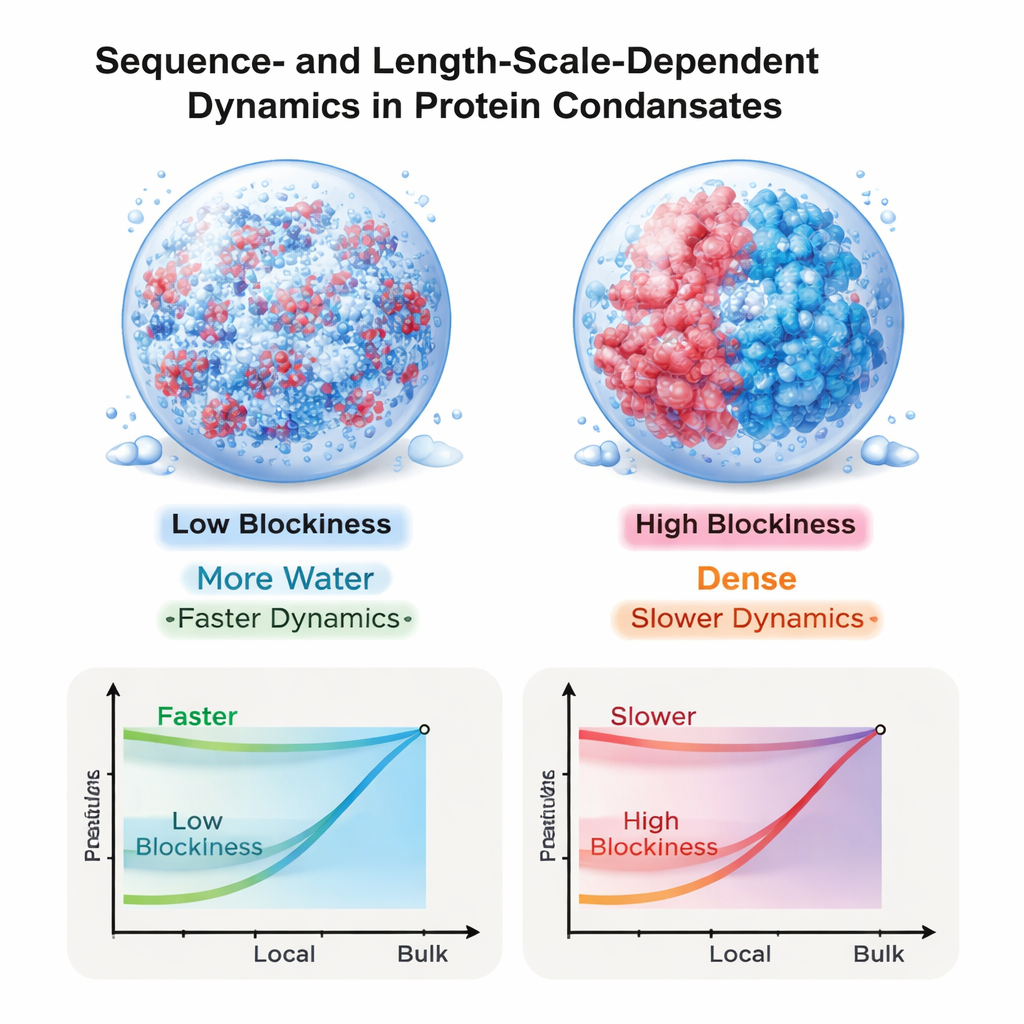
Simulationen mit rätselhaften Experimenten verbinden
Diese Ergebnisse helfen, ein scheinbares Paradoxon aus jüngeren Experimenten zu klären: Wie können kleine Moleküle und Proteinabschnitte sich so schnell in Kondensaten diffundieren, die als Ganzes extrem viskos erscheinen? Die aus dieser Arbeit hervorgehende Antwort lautet, dass sowohl der Wasserfluss als auch langreichweitige elektrostatische Wechselwirkungen in diesen Tröpfchen weiterhin wichtig sind und dass ihr Einfluss stark davon abhängt, wie die Ladungen entlang jeder Kette angeordnet sind. Sequenzen mit blockigen Lademustern erzeugen dichte, hochviskose Tröpfchen, die auf mikroskopischen Skalen dennoch relativ flüssig bleiben, während gemischtere Sequenzen insgesamt beweglichere Umgebungen liefern. Indem die Studie zeigt, dass die Ladungssequenz die Bewegung auf verschiedenen Längenskalen unterschiedlich abstimmen kann, liefert sie ein Gestaltungsprinzip für das Engineering synthetischer proteinbasierter Materialien und erklärt, wie Zellen das Verhalten von Kondensaten über die detaillierte Sequenz ihrer ungeordneten Proteine steuern können.
Zitation: Zhou, H., Wu, Z., Jiang, L. et al. Sequence and length-scale dependent dynamics in biocondensates of highly charged disordered proteins. Commun Chem 9, 98 (2026). https://doi.org/10.1038/s42004-026-01903-0
Schlüsselwörter: biomolekulare Kondensate, intrinsisch ungeordnete Proteine, Lademuster, Proteindynamik, Viskosität