Clear Sky Science · de
Dynamik der photoinduzierten Oxidation von CO zu CO2 auf Rutil (110)
Warum es wichtig ist, Moleküle in Billionstelsekunden zu beobachten
Unser modernes Leben beruht auf chemischen Reaktionen, die Luft und Wasser reinigen und Sonnenlicht in nutzbare Energie umwandeln. Viele dieser Reaktionen finden auf den Oberflächen fester Materialien statt, sogenannten Photokatalysatoren, die durch Licht angetrieben werden. Diese Studie blickt in eine dieser Reaktionen hinein – wie das giftige Kohlenmonoxid (CO) auf einer Titandioxid‑Oberfläche zu Kohlendioxid (CO2) umgewandelt wird – und zwar in Zeitspannen von nur wenigen Billiardsteln einer Sekunde. Das Verständnis dieser ultraschnellen Schritte kann Wissenschaftlern helfen, intelligentere Materialien für die Schadstoffbeseitigung, selbstreinigende Oberflächen und Solartechnologien zu entwerfen.
Eine lichtgetriebene Aufräumtruppe
Titandioxid ist ein bewährtes Material, das in selbstreinigenden Fenstern, luftreinigenden Beschichtungen und experimentellen Solar‑Kraftstoffgeräten eingesetzt wird. Es ist kostengünstig, stabil und kann Licht nutzen, um auf seiner Oberfläche kraftvolle Reinigungsreaktionen auszulösen. Aber nicht alle Formen von Titandioxid verhalten sich gleich. Zwei gebräuchliche Modifikationen, Anatase und Rutil, unterscheiden sich darin, wie effizient sie Reaktionen wie die Umwandlung von CO in CO2 vorantreiben. Während Anatase insgesamt meist aktiver ist, war das genaue Timing der einzelnen Reaktionsschritte – insbesondere wie Sauerstoff aus der Luft aktiviert wird – bisher unklar. Diese Studie konzentriert sich auf die Rutil‑Form mit einer bestimmten Oberflächenorientierung, bekannt als (110), um genau zu messen, wie schnell CO oxidiert, sobald Licht auf das Material trifft.
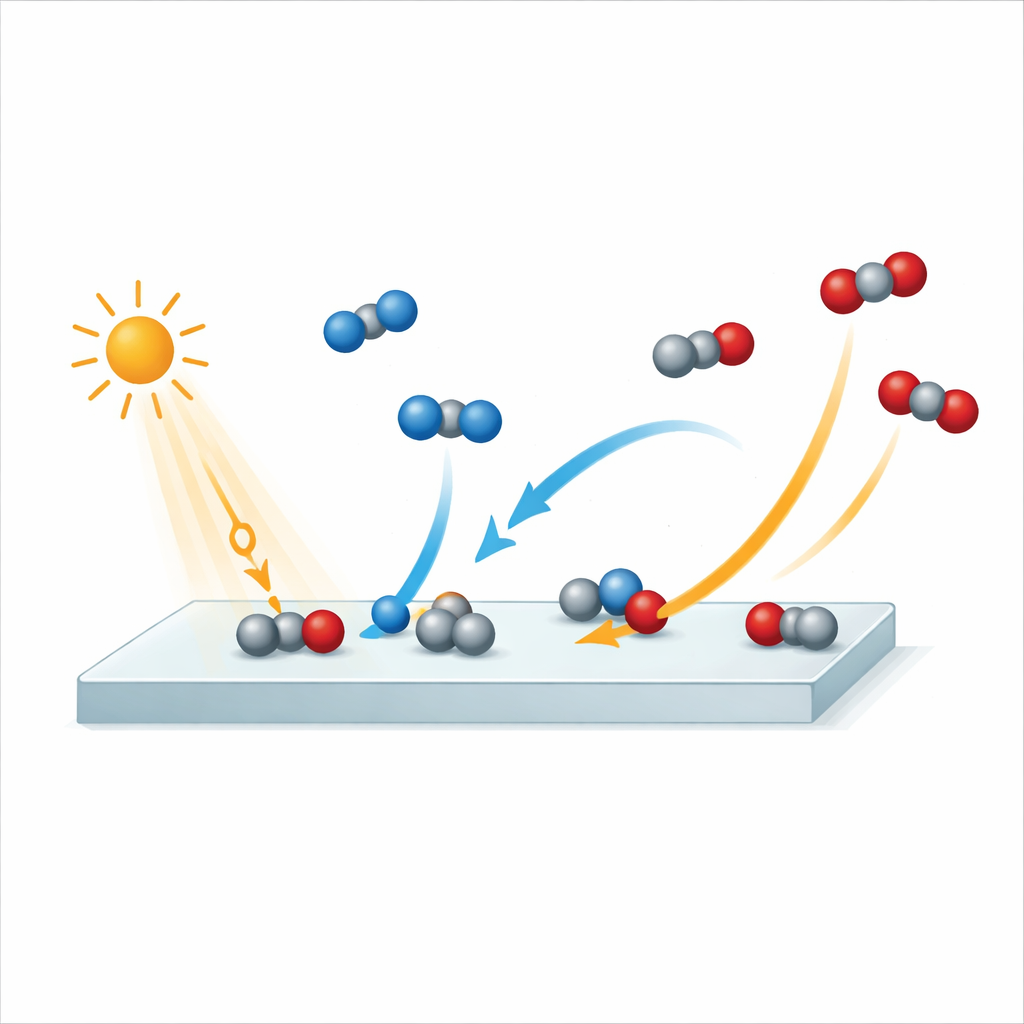
Eine Reaktion mit extrem hoher Geschwindigkeit filmen
Um diesen Prozess einzufangen, nutzten die Forscher eine Freie‑Elektronen‑Laser‑Anlage in Hamburg, die extrem kurze Röntgenblitze erzeugt. Zuerst trafen sie die Rutiloberfläche mit einem Puls von Infrarotlicht, der wie ein winziger Kamerablitz die Reaktion startet. Ein sorgfältig zeitlich abgestimmter Röntgenpuls untersuchte dann, wie sich die Atome und Elektronen auf der Oberfläche veränderten. Durch das Wiederholen dieser Abfolge bei unterschiedlichen Verzögerungen zwischen Licht‑ und Röntgenpuls bauten sie eine Art „molekularen Film“ der Reaktion mit einer zeitlichen Auflösung von etwa 250 Femtosekunden auf – eine Femtosekunde ist ein Millionstel eines Milliardstels einer Sekunde. Das Team verfolgte Signale von Sauerstoffatomen in der Oberfläche und in den Gasen, wodurch sie CO, CO2, Wasser und das Oxid selbst während des Ablaufs unterscheiden konnten.
CO2 in weniger als einer Billionstelsekunde einfangen
Die zentrale Beobachtung ist, dass neues CO2 auf der Rutiloberfläche bereits innerhalb von 200 bis 800 Femtosekunden nach dem Lichtpuls erscheint. Das bedeutet, dass Sauerstoff aus benachbarten O2‑Molekülen aktiviert, Bindungen gebrochen und CO zu CO2 in weniger als einer Billionstelsekunde umgewandelt wird. Nach etwa 0,8 Pikosekunden schwächt sich das frische CO2‑Signal ab, da das Produkt von der Oberfläche desorbiert. Auffällig ist, dass diese gesamte Sequenz auf Rutil schneller abläuft als auf Anatase: Frühere Arbeiten fanden dort das erste auftauchende CO2 erst nach etwa 1,2 bis 2,8 Pikosekunden unter ansonsten ähnlichen Bedingungen. Obwohl Anatase insgesamt mehr CO2 produziert und als stärkerer Photokatalysator gilt, führt Rutil den entscheidenden Oxidationsschritt schneller aus.
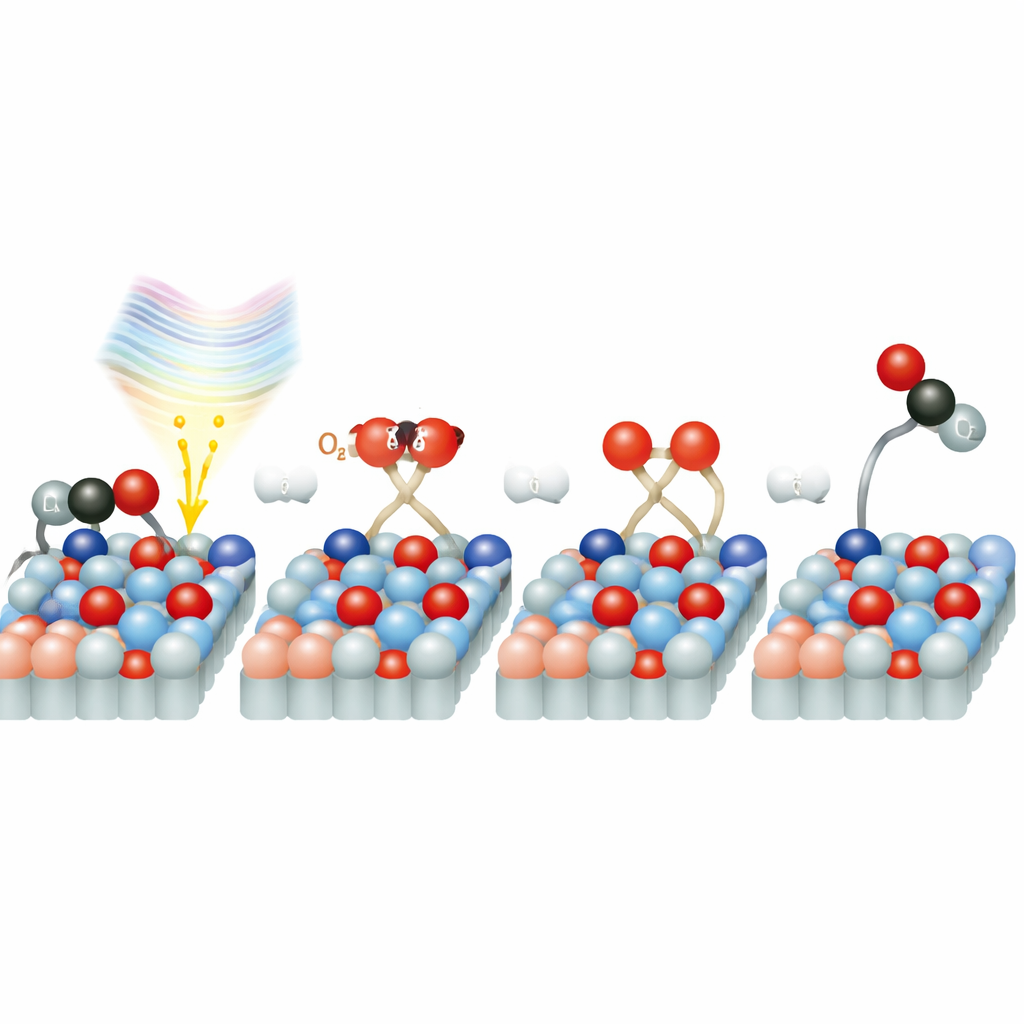
Ein Abkürzungsweg für Sauerstoff
Warum verläuft die Reaktion auf Rutil so schnell? Detaillierte Computersimulationen deuten darauf hin, dass Sauerstoffmoleküle, die auf der Oberfläche sitzen, spezielle elektronische Zustände erzeugen, die als Brücke zwischen Festkörper und O2 fungieren. Wenn das 770‑Nanometer‑Laserlicht absorbiert wird, kann es direkt ein Elektron vom Titandioxid in das Sauerstoffmolekül bewegen und so eine geladene, aktivierte Sauerstoffspezies bilden. Diese „Abkürzung“ umgeht den langsameren Weg, bei dem Elektronen zunächst durch das Volumen des Festkörpers reisen und dann zur Oberfläche diffundieren. Sobald aktiviert, spaltet der Sauerstoff schnell und ein Sauerstoffatom verbindet sich mit CO zu CO2. Die Studie zeigt außerdem, dass Spuren von Wasser auf der Oberfläche sowohl Reaktionsstellen blockieren als auch bei geringen Mengen potenziell den Ladungstransfer und die Sauerstoffaktivierung unterstützen können, was eine zusätzliche Komplexitätsebene hinzufügt.
Den elektronischen Aufbau mit der realen Leistung verbinden
Zusammenfassend zeigt die Arbeit, dass winzige Details in der Art und Weise, wie Elektronen zwischen einer Oberfläche und benachbarten Molekülen wandern, die Reaktionsgeschwindigkeiten dramatisch verändern können, selbst zwischen zwei eng verwandten Materialien. Während Anatase im Hinblick auf die gesamte photokatalytische Ausbeute weiterhin die Nase vorn hat, zeigt Rutil einen schnelleren Sauerstoffaktivierungsschritt, der mit dieser speziellen Ladungsübertragungsroute verknüpft ist. Durch die Verknüpfung ultraschneller Messungen mit fortgeschrittenen Simulationen liefert die Studie eine Roadmap zur Gestaltung von Oberflächen, damit lichtausgelöste Reaktionen effizienter ablaufen. Langfristig könnten solche Erkenntnisse Ingenieuren helfen, bessere Beschichtungen zur Luftreinigung, effektivere antibakterielle Oberflächen und verbesserte Materialien für sonnengetriebene Kraftstoffproduktion und Wasserspaltung zu entwickeln.
Zitation: Gleissner, H., Wagstaffe, M., Wenthaus, L. et al. Dynamics of CO photooxidation to CO2 on rutile (110). Commun Chem 9, 127 (2026). https://doi.org/10.1038/s42004-026-01901-2
Schlüsselwörter: Photokatalyse, Titan‑dioxid, ultraschnelle Spektroskopie, Oberflächenchemie, Oxidation von Kohlenmonoxid