Clear Sky Science · de
Entwicklung eines vierfach-konjugierten Kohlenstoffdot-Nanomodells für die gezielte Gliomtherapie
Neue Hoffnung für hartnäckige Gehirntumoren
Hochgradige Hirntumoren wie das Glioblastom gehören zu den schwersten Krebsformen, die es zu behandeln gilt. Viele wirksame Wirkstoffe im Körperinneren können entweder die schützende Blut–Hirn-Schranke nicht passieren oder schädigen auf dem Weg gesundes Gewebe. Diese Studie beschreibt ein im Labor konstruiertes „intelligentes“ Nanopartikel, das gezielter in Hirntumoren eindringen, einen wirkstarken Medikamentencocktail transportieren und diesen direkt im Zellkern von Tumorzellen freisetzen soll — dort, wo er den größten Schaden für Krebszellen anrichten und normale Zellen schonen kann.
Ein winziger Lieferwagen aus Kohlenstoff
Im Zentrum des neuen Ansatzes stehen Kohlenstoffdots — Nanopartikel im Nanometerbereich aus Kohlenstoff, die kostengünstig herzustellen sind, sich gut mit Wasser mischen und unter bestimmten Lichtbedingungen fluoreszieren. Ihre Oberflächen bieten viele chemische Andockstellen, sodass sie gleichzeitig mit mehreren biologischen Komponenten versehen werden können. In dieser Arbeit erzeugten die Forschenden ein „vierfach-konjugiertes“ Nanomodell: Jeder Kohlenstoffdot wurde in einer einstufigen Reaktion chemisch an zwei verschiedene Zielpeptide und zwei antitumorale Wirkstoffkomponenten gebunden. Dieses modulare Design verwandelt jeden Dot in einen winzigen Lieferwagen, der Tumorzellen erkennen, zelluläre Barrieren überwinden und Wirkstoffe an die richtige intrazelluläre Adresse bringen kann.
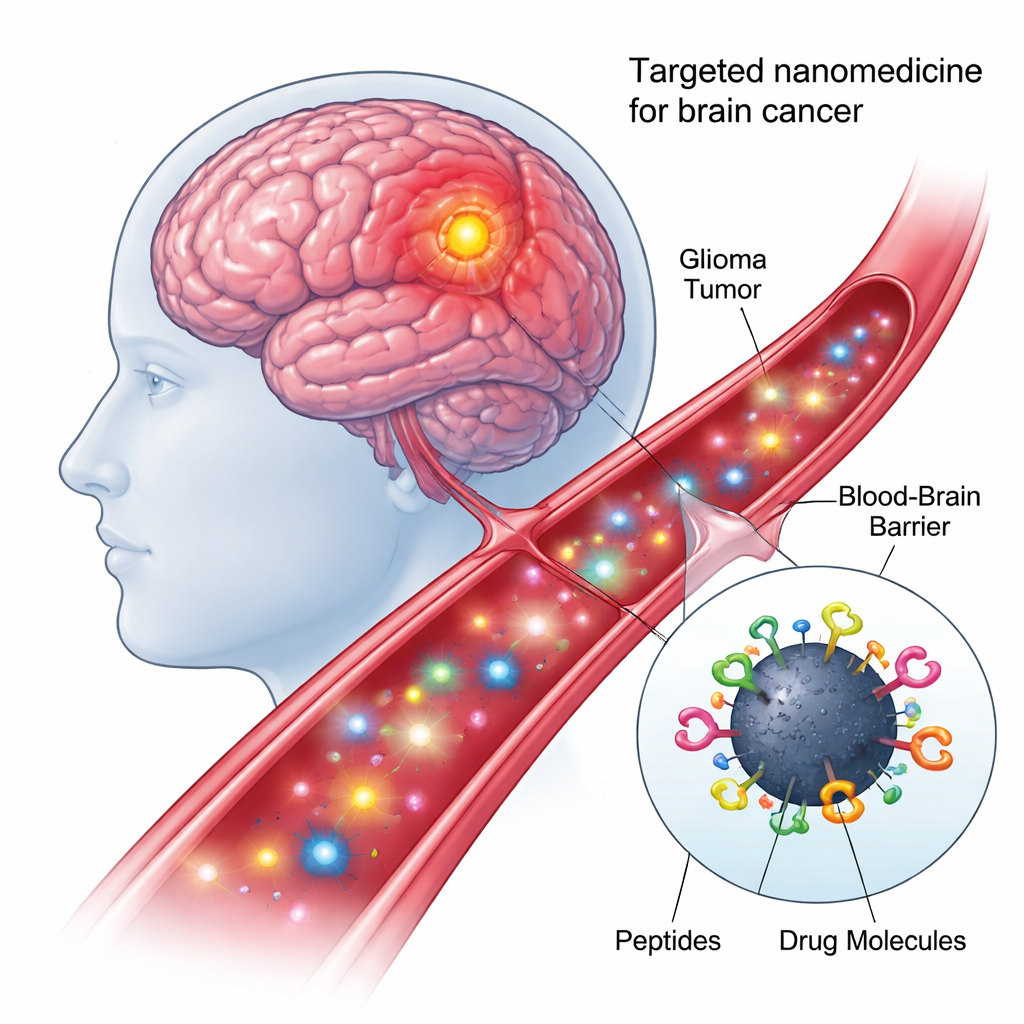
Die richtigen Gehirnzellen finden und betreten
Das erste Peptid auf dem Nanopartikel, genannt shPep-1, ist so konzipiert, dass es einen Rezeptor namens IL13Rα2 erkennt. Dieser Rezeptor ist auf vielen aggressiven Hirntumoren — einschließlich adultem und pädiatrischem Glioblastom sowie diffusem intrinsischem Ponsgliom — stark exprimiert, während er auf normalen Gehirnzellen nur schwach vorkommt. Durch die Bindung an IL13Rα2 hilft shPep-1 den Kohlenstoffdots, gezielt Tumorzellen anzusteuern und über rezeptorvermittelte Aufnahme in sie einzudringen. Das zweite, längere Peptid, lnPep-1, enthält ein nukleäres Lokalisationssignal: eine kurze Sequenz, die Fracht dabei unterstützt, die Kernmembran zu passieren und das Steuerzentrum der Zelle zu erreichen, wo die DNA liegt. Zusammen verleihen diese beiden Peptide dem Nanopartikel sowohl Tumorpräferenz als auch die Fähigkeit, einmal innen den Zellkern zu erreichen.
Ein koordinierter Wirkstoffangriff
Die therapeutische Ladung besteht aus zwei kleinen Molekülen. Das erste ist Epirubicin, ein bekanntes Chemotherapeutikum, das Krebszellen tötet, indem es sich in die DNA einlagert und Enzyme blockiert, die zur Reparatur doppelsträngiger Brüche benötigt werden. Das zweite ist ein Metabolit namens 5-Aminoimidazol-4-carbonsäure (AIC), der aus dem Hirntumormedikament Temozolomid bei physiologischem pH entsteht. In früheren Arbeiten zeigte dieselbe Gruppe, dass die Kombination von Epirubicin und AIC auf einem Kohlenstoffdot die Abtötung von Krebszellen stärker verbessert als jedes Medikament allein. Im neuen Design werden beide gemeinsam auf dem dualen Peptid-Nanopartikel ausgeliefert, um einen synergistischen Effekt direkt im Zellkern der Tumorzellen zu erzielen.
Stark in Tumorzellen, schonender für normale Zellen
Um die Wirksamkeit des Nanomodells zu prüfen, setzte das Team mehrere Zelllinien hochgradiger Gliome — erwachsenes Glioblastom, pädiatrisches Glioblastom und ein Modell des diffusen intrinsischen Ponsglioms — den vierfach-konjugierten Kohlenstoffdots aus. Schon bei sehr niedrigen Konzentrationen (bereits ab etwa 50 Nanomolar) sank die Lebensfähigkeit der Tumorzellen auf ungefähr die Hälfte der unbehandelten Kontrollen, und bei höheren Dosen töteten alle getesteten Konjugate die Mehrheit der Tumorzellen. Wichtig ist, dass das vierfache Nanomodell einfachere „Einzelpeptid“-Versionen übertraf, obwohl es insgesamt weniger Epirubicin trug. Bei nicht-krebserregenden vaskulären glatten Muskelzellen war es deutlich weniger toxisch: Diese Zellen benötigten etwa 25–40-mal mehr Nanopartikel, um einen ähnlichen Lebensfähigkeitsverlust zu zeigen, was auf ein nützliches Sicherheitsfenster durch Tumorzielgerichtetheit statt auf rohe Dosiserhöhung hindeutet.
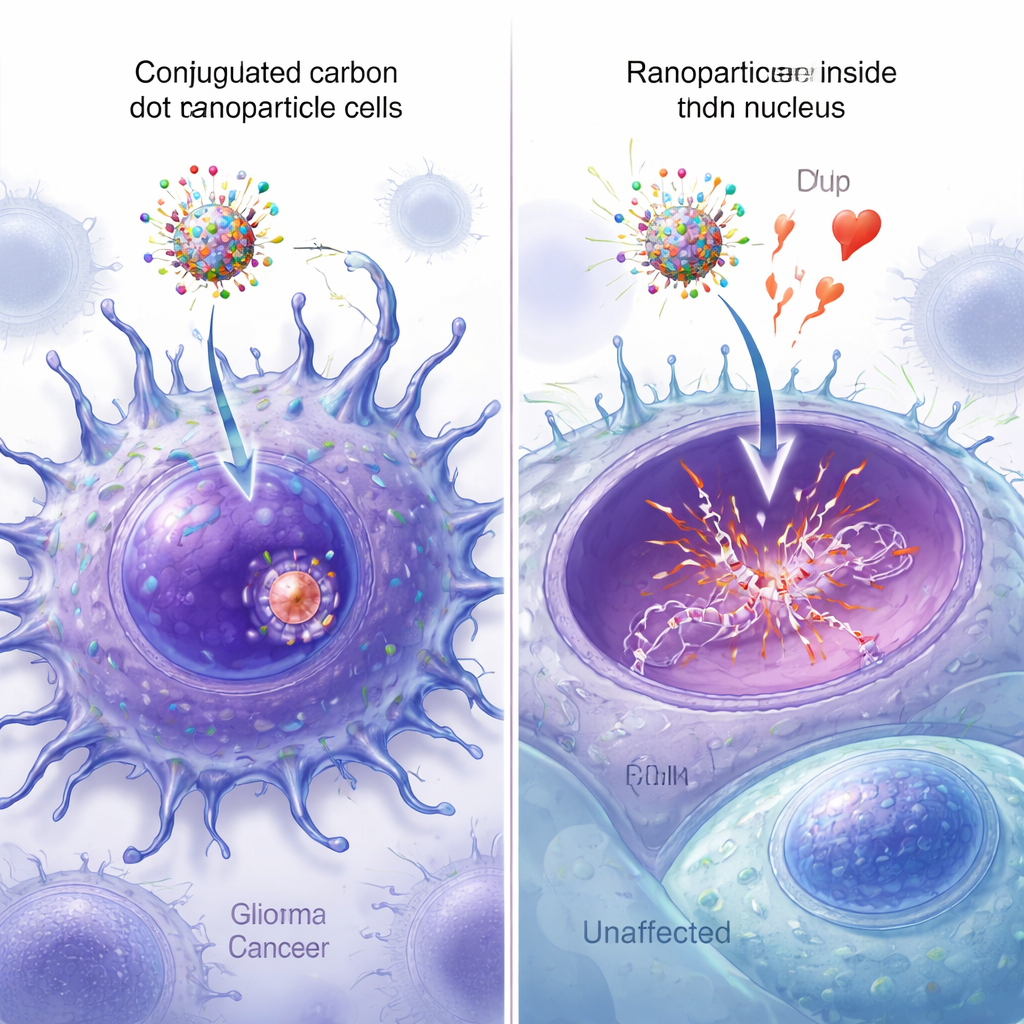
Nachweis, dass die Nanopartikel den Zellkern erreichen
Fluoreszierende Varianten der Nanopartikel erlaubten es den Forschenden, zu beobachten, wie gut jedes Design in Zellen eindrang und den Zellkern erreichte. Unter dem Mikroskop zeigten Kohlenstoffdots mit beiden Peptiden das intensivste Signal, verteilt in den Krebszellen, mit starker Überlappung zwischen der grünen Nanopartikel-Fluoreszenz und der blauen Kernfärbung. Quantitative Bildanalysen bestätigten, dass die Dual-Peptid-Partikel die höchste Kern-Kolokalisierung aufwiesen und damit signifikant über den Partikeln lagen, die nur ein Peptid oder kein Peptid trugen. Zusätzliche Spektroskopie-, Massenspektrometrie- und Rasterkraftmikroskopie-Messungen bestätigten, dass alle vier Komponenten erfolgreich an die Kohlenstoffdots gebunden waren und ihre Größe moderat erhöhten, ohne die entscheidende DNA-Bindungsfunktion von Epirubicin zu stören.
Was das für die zukünftige Behandlung von Hirnkrebs bedeuten könnte
Für Patientinnen und Patienten handelt es sich bei diesen Befunden noch um einen frühen Zellkultur-Nachweis und nicht um eine sofort verfügbare Therapie. Dennoch zeigen sie ein vielversprechendes Konzept: ein kleines, stabiles und relativ einfach herzustellendes kohlenstoffbasiertes Nanopartikel, das sich schnell mit Zielpeptiden und Wirkstoffkombinationen anpassen lässt. Indem Wirkstoffe gezielt zu Tumorzellen gesteuert werden, die IL13Rα2 überproduzieren, und im Zellkern konzentriert werden, könnten solche Nanomedikamente eines Tages niedrigere Dosen, weniger Nebenwirkungen und personalisiertere Behandlungsstrategien für hochgradig tödliche Hirntumoren wie Glioblastom und diffuses intrinsisches Ponsgliom ermöglichen.
Zitation: Cilingir, E.K., Hettiarachchi, S.D., Rathee, P. et al. Development of a quadruple-conjugated carbon dot nanomodel for targeted glioma therapy. Commun Chem 9, 96 (2026). https://doi.org/10.1038/s42004-026-01900-3
Schlüsselwörter: Glioblastom, Nanomedizin, Kohlenstoffdots, gezielte Wirkstofffreisetzung, Gehirntumoren