Clear Sky Science · de
Ein generalisierbarer Test zur intrazellulären Akkumulation zur Charakterisierung der zytosolischen Wirkstofffreisetzung in Säugerzellen
Warum es wichtig ist, Wirkstoffe in die Zellen zu bringen
Viele der heute vielversprechendsten Medikamente — kleine Wirkstoffmoleküle, kurze Proteinfragmente namens Peptide und voll ausgeprägte Proteine — sind so konzipiert, dass sie Ziele innerhalb unserer Zellen angreifen. Die Zellmembran fungiert jedoch als strenges Sicherheitstor. Ein Wirkstoff kann an der Außenseite einer Zelle haften bleiben oder in innere Bläschen, sogenannte Endosomen, eingeschlossen werden und trotzdem nie das wässrige Innenreich, das Zytosol, erreichen, in dem viele Zielorte liegen. Dieser Artikel beschreibt einen neuen Labortest, den CHAMP-Assay, der Forschern nicht nur sagt, ob ein Molekül in eine Zelle gelangt, sondern ob es tatsächlich im Zytosol ankommt, wo es wirken kann.
Ein neuer Weg, das Eindringen von Wirkstoffen zu verfolgen
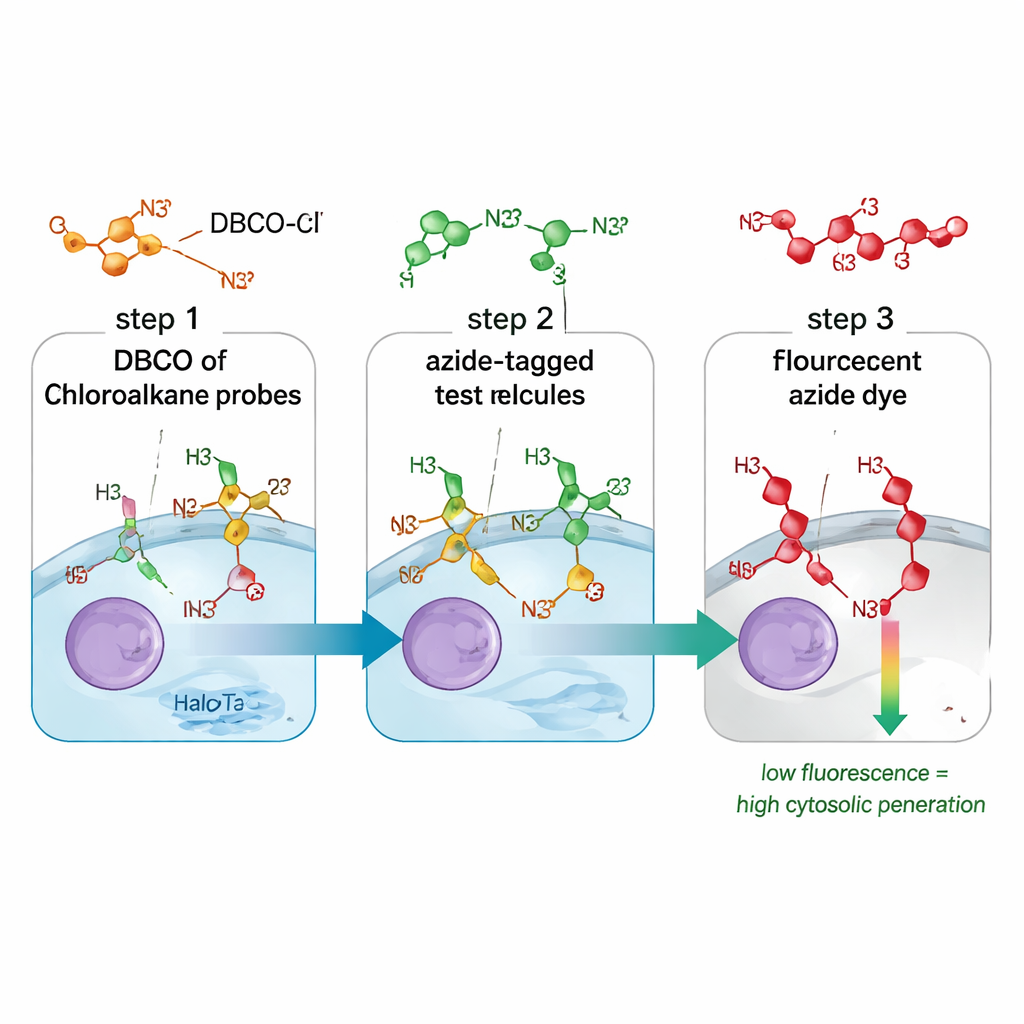
Traditionelle Methoden zur Messung der Wirkstoffaufnahme verwischen oft die Unterschiede zwischen Molekülen, die lediglich die Zelloberfläche berühren, in Endosomen sitzen oder erfolgreich das Zytosol erreichen. Zudem stützen sie sich häufig auf sperrige Fluoreszenzmarker, die das Verhalten eines Moleküls verändern können. Der CHAMP-Assay löst beide Probleme, indem er einen kleinen chemischen „Handgriff“ namens Azid mit einem Proteinmarker namens HaloTag kombiniert, das so konstruiert ist, frei im Zytosol kultivierter humaner Zellen zu schwimmen. Zunächst werden die Zellen mit einem Linker behandelt, der DBCO, eine angespannte Alkinform, an HaloTag koppelt. Anschließend fügen die Wissenschaftlerverbindung ihr Testmolekül hinzu, das die winzige Azid-Markierung trägt. Nur wenn dieses Molekül die Zellmembran ins Zytosol durchquert, können Azid und DBCO in einer hochselektiven chemischen Reaktion „clicken“. Ein abschließender fluoreszenter Azidfarbstoff zeigt, wie viele DBCO-Stellen noch frei sind: schache Zellen bedeuten, dass das Testmolekül eingedrungen ist und die meisten Stellen besetzt hat; helle Zellen deuten auf schlechten zytosolischen Zugang hin.
Vom Konzept zum funktionierenden Assay
Die Autorinnen und Autoren bestätigten zunächst, dass HaloTag korrekt hergestellt wurde und im Zytosol humaner HeLa-Zellen lokalisiert ist, indem sie einen standardmäßigen Chloroalkandye verwendeten und bildgebend nachwiesen. Sie optimierten dann jeden Schritt von CHAMP: wie viel DBCO-Linker zugeben, wie lange inkubiert werden muss und welcher fluoreszente Azidfarbstoff ein starkes, spezifisches Signal liefert, ohne die Zellen zu schädigen. Die Durchflusszytometrie — ein Instrument, das die Fluoreszenz in Tausenden einzelner Zellen misst — zeigte, dass der Assay schnell, robust und anpassbar ist. Entscheidend wies das Team nach, dass die Fluoreszenz tatsächlich von spezifischen Reaktionen an den HaloTag-Stellen stammt und nicht von unspezifischem Anhaften der Farbstoffe an Zellkomponenten, und dass die kleine Azid-Markierung das Eindringen der Moleküle in die Zellen nicht merklich störte.
Was der Assay über kleine Wirkstoffe und Peptide zeigt
Mit CHAMP in der Hand prüften die Forscher Hunderte azidmarkierter kleiner Moleküle und variierten systematisch Eigenschaften wie Ladung, Größe und Flexibilität. Sie beobachteten beispielsweise, dass die Umwandlung einer negativ geladenen Carbonsäure in ein neutrales Amid die zytosolische Akkumulation erhöhte und dass das Ausmaß und die Position der N‑Methylierung von Stickstoffatomen das Eindringen veränderten. Durch den Vergleich von Reaktionen an freien Kügelchen versus lebenden Zellen konnten sie die intrinsische chemische Reaktivität von der Barrierewirkung der Membran unterscheiden. Das Team wendete CHAMP auch auf ein Panel gängiger Antibiotika an und zeigte, dass einige deutlich besser ins Zytosol gelangten als andere — eine wichtige Information beim Umgang mit Bakterien, die sich innerhalb von Wirtszellen verstecken.
Supergeladene Peptide und Proteine überwinden die Barriere
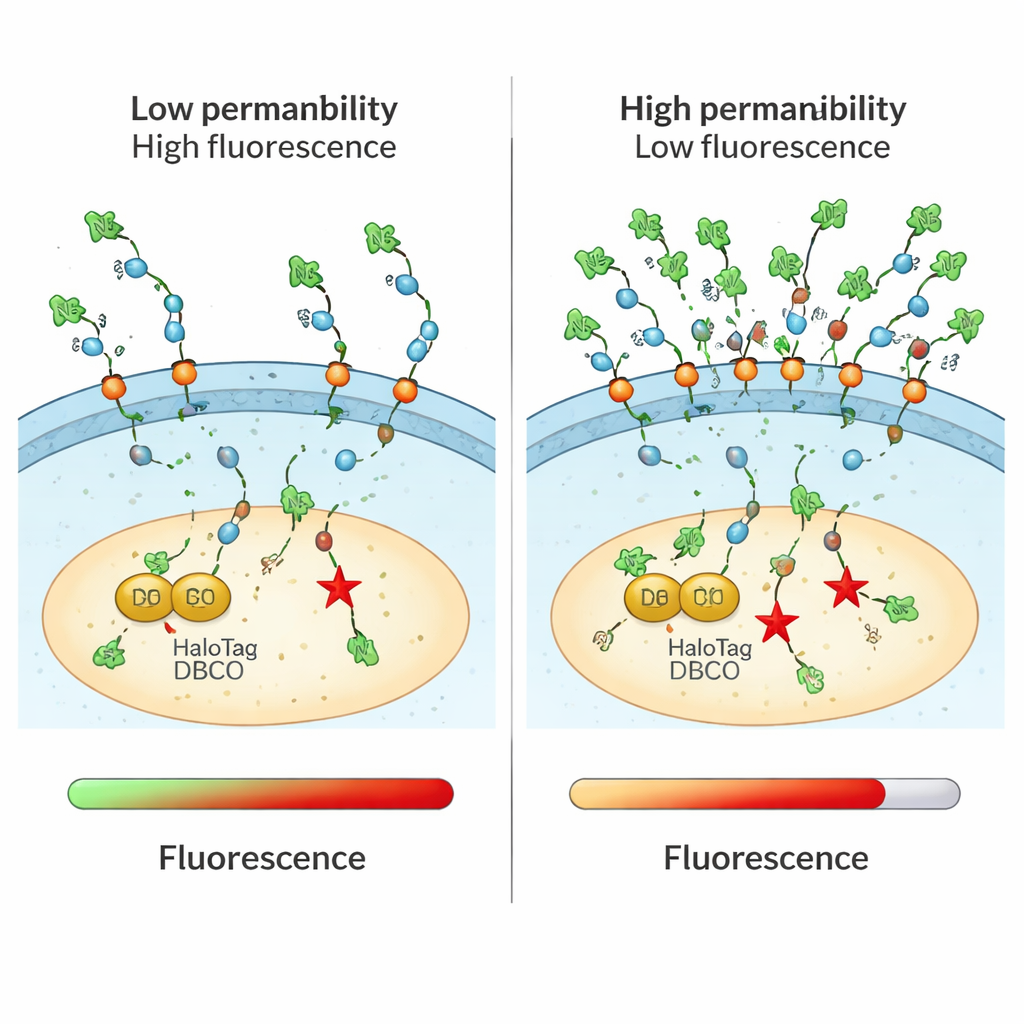
Der Assay erwies sich besonders geeignet für die Untersuchung größerer, stark geladener Moleküle, die sich mit anderen Methoden schwer verfolgen lassen. Die Autorinnen und Autoren untersuchten zellpenetrierende Peptide aus mehreren Argininresten und bestätigten einen klaren Trend: Längere, stärker positiv geladene Ketten lieferten mehr Substanz ins Zytosol, bis zu einem gewissen Punkt. Sie prüften, wie das Umkehren der Händigkeit (Stereochemie) bestimmter Aminosäuren den Eintritt veränderte, und fanden, dass Spiegelbildversionen teilweise besser akkumulierten — ein Hinweis auf subtile chirale Wechselwirkungen mit der Membran. CHAMP zeigte außerdem, dass „supergeladene“ Proteine — so konstruiert, dass sie viele positive Ladungen tragen — das Zytosol effektiver erreichen konnten als ihre normalen Gegenstücke, was ihr Potenzial als Transporter für große therapeutische Fracht unterstützt.
Gestaltungsregeln für künftige intrazelluläre Wirkstoffe
Durch systematische Tests von kleinen Molekülen, Peptiden, makrozyklischen Peptiden und modifizierten Rückgraten deckte die Studie allgemeine Gestaltungsprinzipien auf. Makrozyklische Peptide, deren Rückgrat zu Ringen geschlossen ist, erreichten tendenziell leichter das Zytosol als flexible lineare Versionen. Sorgfältig platzierte N‑Methylgruppen am Peptidrückgrat steigerten den Eintritt leicht, während zu viele davon kontraproduktiv sein konnten. Diese Struktur–Permeations-Beziehungen, aufgedeckt mit einem einzigen standardisierten Assay, liefern praktische Leitlinien für Chemiker, die Moleküle entwerfen möchten, die nicht nur an ihre Ziele binden, sondern diese auch innerhalb der Zellen erreichen können.
Wie das die Wirkstoffentwicklung unterstützt
Einfach ausgedrückt ist der CHAMP-Assay ein fein abgestimmter Verkehrszähler an der Haustür und im inneren Flur der Zelle. Er sagt Wissenschaftlern, welche experimentellen Wirkstoffe tatsächlich die Membran überwinden und ins Zytosol gelangen, ohne von Molekülen getäuscht zu werden, die an der Oberfläche oder in inneren Kompartimenten festsitzen. Da er mit einer Vielzahl von molekularen Formen und Größen funktioniert und nur eine winzige Azid‑Markierung verwendet, lässt sich CHAMP in Hochdurchsatz-Entdeckungsabläufe integrieren. Im Laufe der Zeit sollte dies die Entwicklung wirksamerer Behandlungsoptionen für Krankheiten beschleunigen, bei denen die wichtigsten Ziele hinter der Zellmembran verborgen sind.
Zitation: Bhandari, S., Ongwae, G.M., Dash, R. et al. A generalizable assay for intracellular accumulation to profile cytosolic drug delivery in mammalian cells. Commun Chem 9, 94 (2026). https://doi.org/10.1038/s42004-026-01898-8
Schlüsselwörter: intrazelluläre Wirkstofffreisetzung, Permeabilität der Zellmembran, zytosolische Akkumulation, zellpenetrierende Peptide, bioortogonale Click-Chemie