Clear Sky Science · de
Wasserstoff-unterstützte Dehydrochlorierung von 1,1,1,2-Tetrafluoro-2-chlorpropan zu 2,3,3,3-Tetrafluorpropen über Pd-Ag/nano-MgF2 mit optimierten isolierten Pd-Stellen
Sauberere Kühlmittel für eine sich erwärmende Welt
Klimaanlagen und Kühlschränke sorgen für unseren Komfort, doch viele der Stoffe, die ihnen ihre Wirksamkeit verleihen, sind starke Treibhausgase. Diese Studie adressiert eine zentrale Herausforderung: Wie lässt sich eines der wichtigsten Kältemittel der nächsten Generation, HFO‑1234yf, effizienter und mit kleinerer CO2-Bilanz herstellen? Durch das Design eines ausgefeilteren Katalysators – im Grunde eine mikroskopische chemische Maschine – zeigen die Autorinnen und Autoren einen Weg, dieses niedrig erwärmende Kältemittel bei niedrigeren Temperaturen und mit deutlich weniger unerwünschten Nebenprodukten zu produzieren.
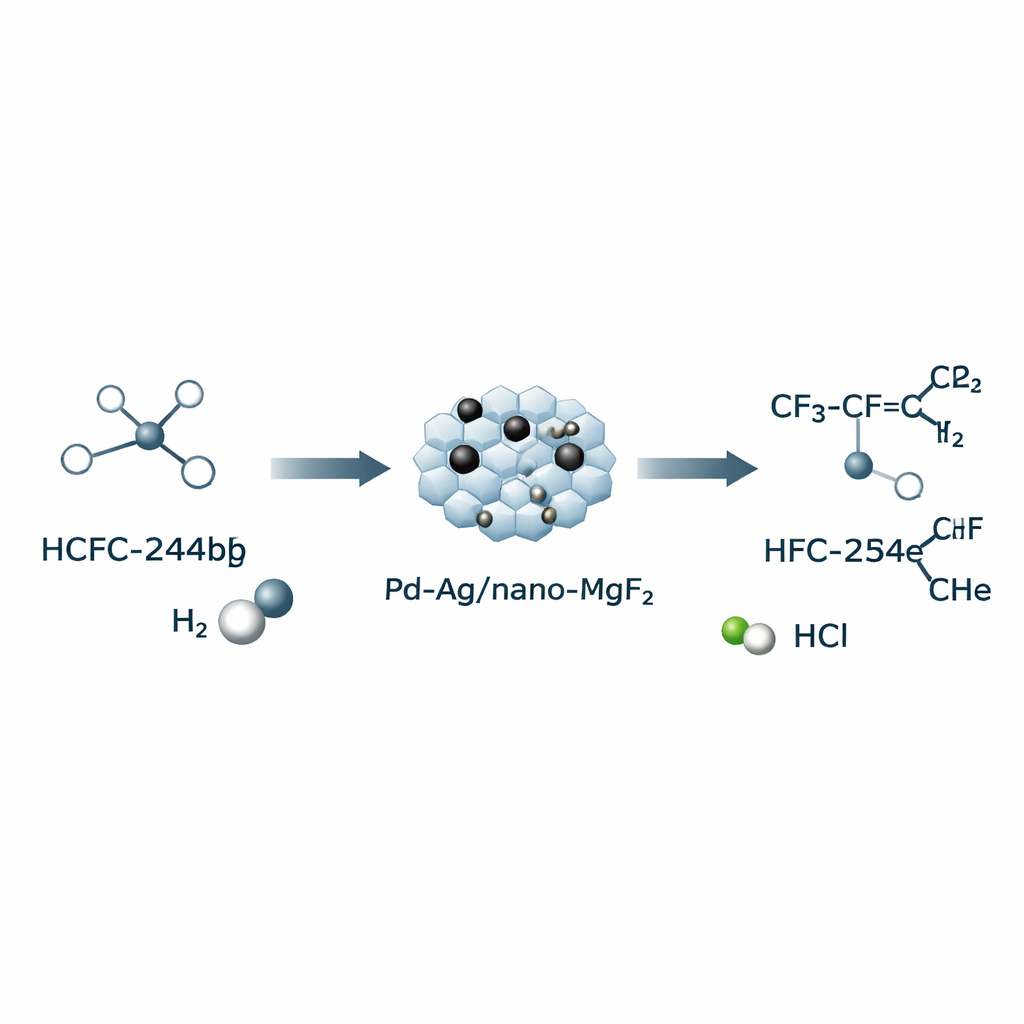
Warum bessere Kältemittelchemie nötig ist
Konventionelle Hydrofluorcarbone (HFCs), wie HFC‑134a, das in Fahrzeugklimaanlagen eingesetzt wird, speichern Wärme in der Atmosphäre um ein Vielfaches stärker als Kohlendioxid. Internationale Abkommen wie das Kigali‑Amendment reduzieren ihren Einsatz schrittweise und treiben die Industrie in Richtung Hydrofluoroolefine (HFOs), die vergleichbare Eigenschaften bei deutlich geringerem Treibhauspotenzial haben (häufig unter 10). HFO‑1234yf ist der führende Ersatzkandidat, doch die derzeitigen industriellen Herstellungsverfahren beruhen auf hochtemperaturigen, energieintensiven Schritten, die zudem Katalysatorlebensdauer verkürzen und Abfall erhöhen. Ein kühlerer, selektiverer Weg zu HFO‑1234yf könnte daher sowohl Emissionen als auch Betriebskosten senken.
Ein schonenderer Weg zu einem Schlüsselmolekül
Die Autorinnen und Autoren konzentrieren sich auf die Umwandlung einer verwandten Verbindung, HCFC‑244bb, zu HFO‑1234yf durch Entfernen von Salzsäure (HCl) unter Beteiligung von Wasserstoffgas. Diese „wasserstoff‑unterstützte Dehydrochlorierung“ erlaubt die Reaktion bei moderaten 270 °C – deutlich unter den oft erforderlichen 600–800 °C thermischer Verfahren. Zentrales Element ist ein maßgeschneiderter fester Katalysator: winzige hohle Partikel aus Magnesiumfluorid (nano‑MgF₂), die mit Palladium (Pd) und Silber (Ag) dotiert sind. Durch die Reihenfolge der Zugabe von Pd und Ag bei der Herstellung lässt sich steuern, wie gut sich die beiden Metalle mischen – welche Art von Legierung entsteht – und wie die aktiven Pd‑Stellen sich schließlich während der Reaktion an der Oberfläche ausbilden.
Aus Metallclustern werden Einzelatome
Während der ersten Betriebsstunden zeigen die Katalysatoren eine „Induktionsphase“: Die Umwandlung von HCFC‑244bb sinkt langsam, während die Selektivität zum gewünschten HFO‑1234yf stetig zunimmt. Mikroskopie, Spektroskopie und Oberflächenmessungen klären den Grund. Während die Reaktion abläuft, chloriert die vor Ort gebildete Salzsäure die Metallpartikel, zerteilt größere Pd‑Cluster und formt sie um zu isolierten Pd‑Atomen, die auf der nano‑MgF₂‑Oberfläche verankert sind. Katalysatoren, die anfangs einen höheren Grad an Pd–Ag‑Legierung aufweisen – erzielt, wenn Pd zuerst und dann Ag zugegeben wird – unterliegen der stärksten Umstrukturierung und weisen am Ende die größte Dichte an Einzelatom‑Pd‑Stellen auf. Dieses optimierte Material wandelt etwa 60 % von HCFC‑244bb um und leitet rund 82 % des Produkts in Richtung HFO‑1234yf, während es die tiefere Hydrierung zu einem unerwünschten gesättigten Produkt, HFC‑254eb, deutlich unterdrückt.
Wie das Verhalten von Wasserstoff das Resultat steuert
Um zu verstehen, warum isolierte Pd‑Atome so gut funktionieren, untersuchten die Forschenden, wie Wasserstoff, das Ausgangs‑Kältemittelmolekül und das Produkt mit verschiedenen Katalysatoroberflächen wechselwirken. Sie fanden heraus, dass HCFC‑244bb und Wasserstoff beide vorzugsweise auf Pd adsorbieren, nicht auf Ag, wobei Stärke und Art der Wasserstoffbindung entscheidend sind. Große Pd‑Aggregate tendieren dazu, „Spillover“-Wasserstoff zu erzeugen, der bei hohen Temperaturen stark gebunden bleibt und Überhydrierung fördert, wodurch wertvolles HFO‑1234yf in weniger nützliche gesättigte Produkte umgewandelt wird. Im Gegensatz dazu halten Einzelatom‑Pd‑Stellen Wasserstoff in einer reaktiveren, aber weniger persistierenden Form, genau richtig, um sauber HCl zu entfernen und die gewünschte Kohlenstoff‑Doppelbindung zu bilden. Computersimulationen auf Basis der Dichtefunktionaltheorie stützen diese Befunde: Sie zeigen, dass diese isolierten Pd–Fluorid‑Umgebungen das Abstrappen von Wasserstoff aus Schlüsselzwischenprodukten auf dem Weg zu HFO‑1234yf erleichtern, während sekundäre Hydrierungsschritte energetisch unvorteilhafter werden.
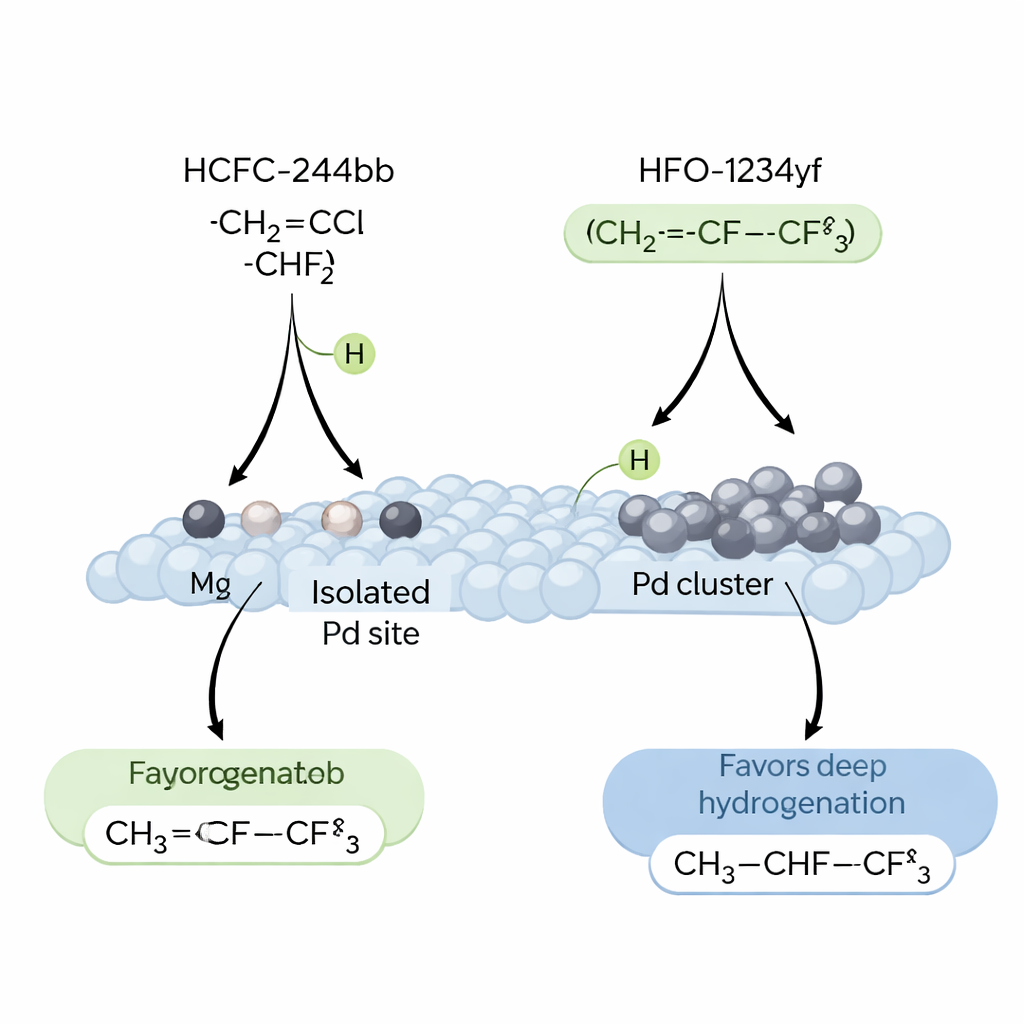
Vom Laborerkenntnis zum grüneren Kühlen
Praktisch gesehen liefert der beste Pd–Ag/nano‑MgF₂‑Katalysator Raten der HFO‑1234yf‑Bildung, die um ein Vielfaches höher sind als bei früheren Feststoffkatalysatoren, die auf harsche, hochtemperaturige Dehydrochlorierung setzten. Die Arbeit zeigt, dass die Kontrolle einzelner Metallatome – nicht nur von Nanopartikeln – Reaktionswege entscheidend lenken und sowohl Effizienz als auch Selektivität deutlich verbessern kann. Für Nichtfachleute lautet die Kernbotschaft: Besseres Katalysatordesign lässt sich direkt in sauberere Herstellung moderner Kältemittel übersetzen. Das wiederum hilft der Welt, Klimaziele zu erreichen, während unsere Gebäude, Fahrzeuge und Lebensmittelvorräte kühl bleiben.
Zitation: Yang, C., Mao, W., Dong, X. et al. Hydrogen-assisted dehydrochlorination of 1,1,1,2-tetrafluoro-2-chloropropane to 2,3,3,3-tetrafluoropropene over Pd-Ag/nano-MgF2 with optimized Pd isolated sites. Commun Chem 9, 93 (2026). https://doi.org/10.1038/s42004-026-01896-w
Schlüsselwörter: Kältemittel, Katalyse, Palladium-Silber, Treibhausgase, Hydrofluoroolefine