Clear Sky Science · de
Metalloberflächen-aktivierte DNAzym-Katalyse für effiziente DNA-Spaltung
Metalle, die DNA sich selbst schneiden lassen
Die meisten von uns denken bei Metall an etwas Festes und Inertes – gut für Münzen, Töpfe und Leitungen, aber nicht für Chemie in einem Glas Wasser. Diese Studie kehrt diese Vorstellung um, indem sie zeigt, dass nackte Metallstücke winzige, auf DNA basierende Katalysatoren, sogenannte DNAzyme, allein mit reinem Wasser und Luft einschalten können. Die Arbeit offenbart eine unerwartete Art, wie alltägliche Materialien wie Kupfer und andere Metalle an ihren Oberflächen komplexe, biologieähnliche Reaktionen antreiben können, und deutet auf neue Werkzeuge für Sensorik, Medizin und sogar Ursprungs-of-Life-Chemie hin. 
Was sind DNA-Scheren?
DNAzyme sind kurze DNA-Stränge, die sich zu Strukturen falten, die bestimmte chemische Reaktionen beschleunigen können, ähnlich wie Protein-Enzyme. Viele bekannte DNAzyme wirken wie molekulare Scheren, die andere DNA- oder RNA-Stränge schneiden, benötigen dafür aber fast immer gelöste Metallionen – etwa Kupfer, Zink oder Magnesium – in der Lösung. Ein solches DNAzym, PL genannt, ist ein sich selbst schneidender Strang, der normalerweise auf Kupferionen und bestimmte Hilfsmoleküle wie Vitamin C oder Wasserstoffperoxid angewiesen ist. Diese Helfer beteiligen sich an Redox- (Elektronentransfer-)Reaktionen, die hochreaktive Sauerstoffspezies erzeugen, die dann das DNA-Rückgrat an genau definierten Stellen angreifen und brechen.
Wenn ein Kupferdraht zum Cofaktor wird
Bei der Untersuchung eines elektrochemischen Setups zur Steuerung der PL-Aktivität bemerkten die Forscher etwas Überraschendes: Schon das Eintauchen eines nackten Kupferdrahts in eine Lösung, die PL und doppelgefiltertes Wasser enthielt, führte zu effizienter DNA-Spaltung – ganz ohne zugesetzte Kupferionen, Puffer oder Salze. Die Kupferoberfläche allein war so wirksam wie oder wirkte sogar besser als die traditionellen Mischungen aus Kupferionen plus Vitamin C oder Wasserstoffperoxid und schnitt die DNA genau an derselben Stelle. Folgetests zeigten, dass viele Kupfergegenstände – Bleche, Trichter, Töpfe und sogar Münzen unterschiedlicher Währungen – PL zur Spaltung anregen konnten, wobei das Ausmaß der Reaktion davon abhing, wie viel Metalloberfläche mit dem Tropfen in Kontakt stand. Frisch poliertes Kupfer funktionierte etwas schlechter als gealtertes, oxidiertes Kupfer, was nahelegt, dass eine dünne Luft-oxidierte Schicht die Reaktion sogar begünstigen kann.
Welche Oberflächen wirken – und warum
Um zu prüfen, ob es sich um eine kupferspezifische Kuriosität handelt, testete das Team 24 Metalle und 10 nichtmetallische Materialien. Sie fanden heraus, dass nur bestimmte Metalle wie Kupfer, Tantal und Vanadium PL stark aktivierten, während Glas, Kunststoff, Holz und andere Nichtmetalle nichts bewirkten. Messungen zeigten, dass geringe Mengen an Metallionen aus aktiven Oberflächen in das Wasser ausgewaschen werden, aber diese Ionen allein waren zu schwach, um die starke DNA-Spaltung zu erklären. Die fehlende Zutat erwies sich als reaktiver Sauerstoff, der aus gelöster Luft stammt. Mithilfe chemischer Fänger und Enzyme zeigten die Autoren, dass Superoxid – eine energiereiche Form des Sauerstoffs mit einem zusätzlichen Elektron – wesentlich ist. Wenn gelöster Sauerstoff durch Stickstoffdurchspülung entfernt wurde, verschwand die PL-Aktivität nahezu; ließ man wieder Sauerstoff zu, stellte sich die Spaltung wieder ein. Zusammen sprechen die Daten für einen Zyklus, in dem die Metalloberfläche und die ausgewaschenen Ionen gelösten Sauerstoff in Superoxid und Wasserstoffperoxid direkt an der Fest-Flüssig-Grenzfläche umwandeln, und diese Spezies dann die DNA-Spaltung antreiben. 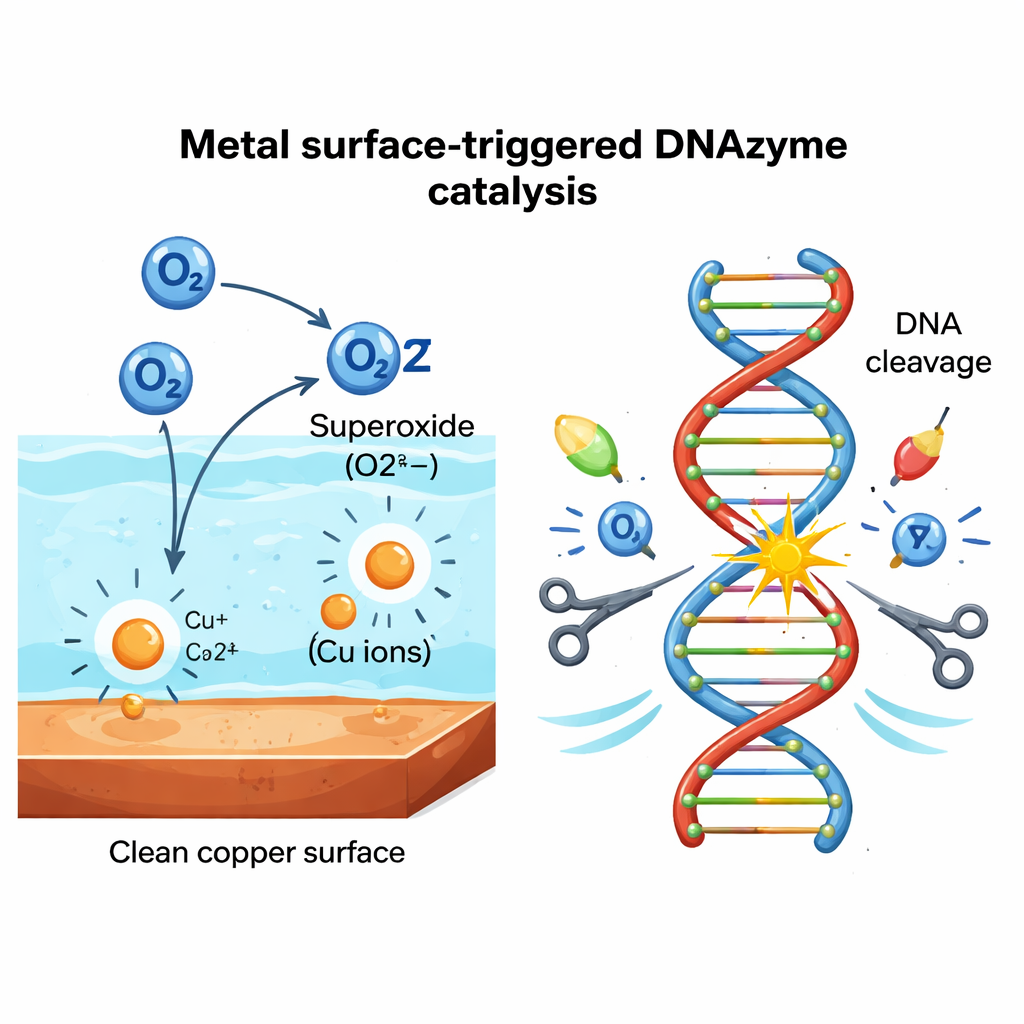
Helfer, Hemmer und andere DNA-Enzyme
Die oberflächenausgelöste Chemie ließ sich mit bekannten Molekülen hoch- oder herunterregeln. Chelatoren wie EDTA, die Metallionen binden, verlangsamten die Reaktion. Katalase, ein Enzym, das Wasserstoffperoxid abbaut, und Farbstoffe, die Superoxid auffangen, reduzierten ebenfalls die DNA-Spaltung und bestätigten so die Rolle dieser reaktiven Sauerstoffspezies. Im Gegensatz dazu verstärkten kleine Verbindungen wie Vitamin C, Glutathion und Katechol die Aktivität, indem sie den Redox-Zyklus nährten, der nahe der Metalloberfläche Superoxid erzeugt. Bemerkenswerterweise war der Effekt nicht auf PL beschränkt: Andere DNAzyme, die DNA oder RNA schneiden, darunter F-8, Ag10c und I-R3, wurden ebenfalls durch die entsprechenden massiven Metalle aktiviert (zum Beispiel Silbermetall für ein Ag-abhängiges DNAzym und Zinkmetall für ein Zn-abhängiges). Das deutet darauf hin, dass „metalloberflächenaktivierte“ DNA-Katalyse eher ein allgemeines Phänomen als eine einmalige Kuriosität sein könnte.
Warum das über das Labor hinaus wichtig ist
Für Leser außerhalb der Chemie lautet die zentrale Botschaft: Feststoff-Metalloberflächen können wie unsichtbare chemische Partner für DNA-basierte Katalysatoren wirken und nur Luft und Wasser nutzen, um die reaktiven Spezies zu erzeugen, die nötig sind, um DNA zu schneiden. Anstatt präzise Mengen an Metallionen aufzulösen, kann man einfach eine geeignete Metalloberfläche mit einer DNA-Lösung in Kontakt bringen und die Grenzfläche die Arbeit erledigen lassen. Das eröffnet Möglichkeiten für kostengünstige Sensoren, die auf Metallgegenstände reagieren, Werkzeuge, um schädliche Sauerstoffradikale in Zellen zu überwachen oder zu binden, und neue Wege, um zu untersuchen, wie lebenähnliche Reaktionen auf Mineral- oder Metalloberflächen ablaufen könnten. Kurz gesagt: Ihre Kupfermünze ist nicht nur Kleingeld – sie kann auch eine winzige chemische Fabrik für DNA-Scheren sein.
Zitation: Jiang, F., Dong, Y., Yu, W. et al. Metal surface-triggered DNAzyme catalysis for efficient DNA cleavage. Commun Chem 9, 91 (2026). https://doi.org/10.1038/s42004-026-01893-z
Schlüsselwörter: DNAzym, Metalloberflächenkatalyse, reaktive Sauerstoffspezies, Kupferschnittstellenchemie, DNA-Spaltung