Clear Sky Science · de
Gesteuerte spherulitische Kristallbildung aus Salzgemischen
Warum Salzkristalle wie Blumen aussehen können
Die meisten von uns stellen sich Kristalle als scharfe, facettierte Formen vor, doch in der Natur wachsen sie oft zu spektakulären Kugeln heran, die an Blumen oder Schneebälle erinnern. Diese sogenannten „Spherulite“ treten in Vulkangestein, Nierensteinen und sogar bei einigen Krankheiten im Zusammenhang mit fehlgefalteten Proteinen auf. Dieser Artikel untersucht, wie ein alltägliches Mineral, Natriumsulfat — dasselbe Salz, das in Waschmitteln und in einigen Baustoffen vorkommt — dazu gebracht werden kann, derart filigrane kugelförmige Kristalle zu bilden, und was dies über die Selbstassemblierung komplexer Strukturen aus einfachen Bestandteilen verrät.
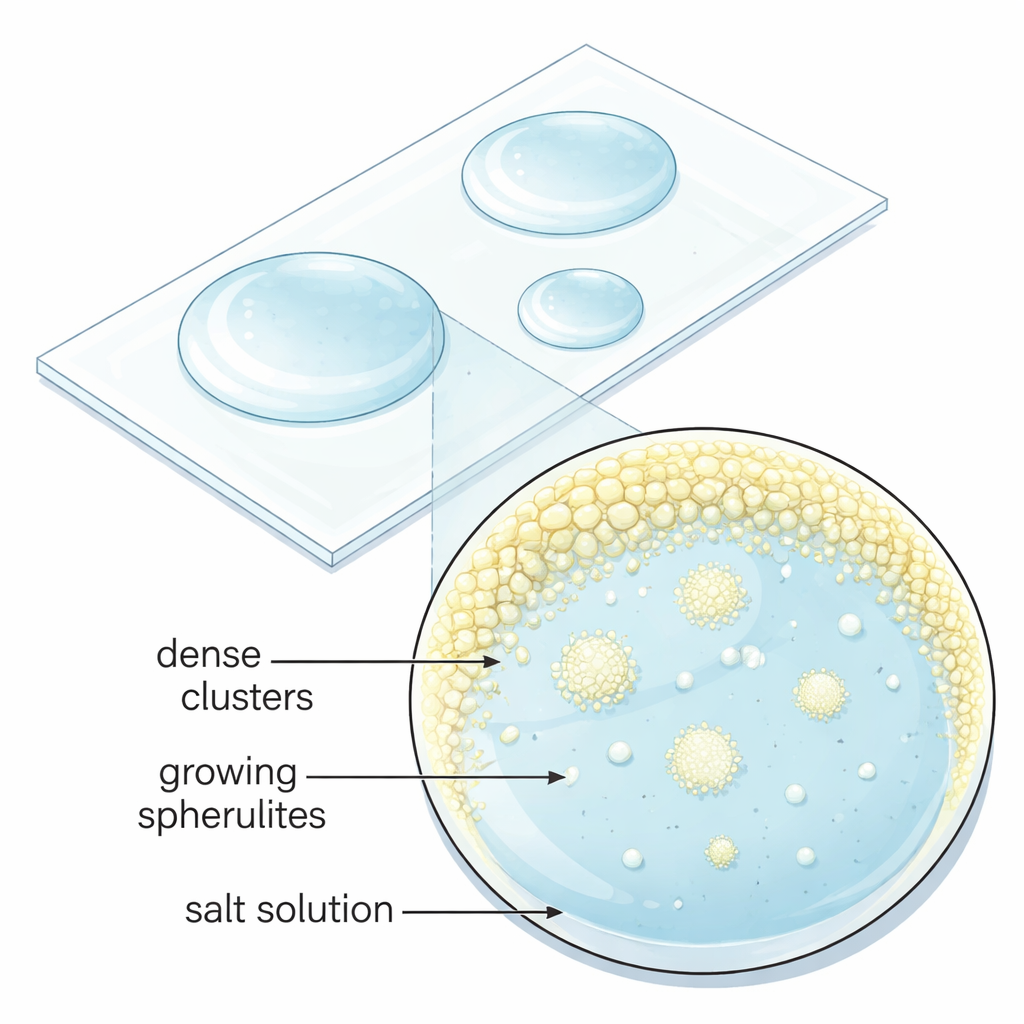
Von einfachen Salzen zu gestalteten Kugeln
Die Forschenden wollten verstehen, wann und wie Natriumsulfat zu Spheruliten statt zu gewöhnlichen blockigen Kristallen heranwächst. Sie bereiteten winzige Tröpfchen Wasser mit Mischungen aus Natriumsulfat und anderen Sulfatsalzen vor, deren Metallionen zwei positive Ladungen tragen, zum Beispiel Magnesium oder Eisen. Während diese Pikolitervon-Mikrolitertröpfchen langsam auf Glasobjektträgern bei Raumtemperatur verdampften, wurden die gelösten Salze immer stärker konzentriert, bis Kristalle zu wachsen begannen. Durch systematisches Variieren der Mischungsverhältnisse fanden sie bestimmte Zusammensetzungs-„Sweetspots“, in denen Natriumsulfat konsequent kugelige, radial strukturierte Kristalle bildete. Außerhalb dieser Bereiche lieferte dieselbe Lösung entweder reguläre facettierte Körner oder ein strukturloses, gelartiges Feststoffnetz — ein Hinweis darauf, dass die kugelförmigen Formen sorgfältig abgestimmte Bedingungen erfordern.
Kleine flüssige Taschen, die Kristallkugeln aussäen
Unter dem Mikroskop beobachtete das Team, dass Spherulite nicht direkt aus klarer Lösung entstanden. Stattdessen erzeugte die Verdampfung zunächst kleine, dichte Flüssigkeitsklümpchen, die am Rand des Tropfens in gelösten Ionen angereichert waren. Diese mikrongroßen Taschen hielten Minuten lang an, bevor plötzlich viele Spherulite auf einmal austrieben. Hochaufgelöste Elektronenmikroskopbilder der getrockneten Strukturen zeigten, dass jede Spherulite aus zahllosen Nanometer großen Natriumsulfatkristallen besteht, die ungefähr nach außen gerichtet sind und später zusammenwachsen. Dieses Verhalten widerspricht dem Lehrbuchbild des Kristallwachstums, bei dem ein einzelner stabiler Keim glatt wächst, und deutet stattdessen auf einen mehrstufigen „nicht-klassischen“ Weg hin, bei dem dichte Tröpfchen und Nanopartikel sich zusammenlagern und umorganisieren, bevor sie die endgültige Festform erreichen.
Wenn salziges Wasser erdnussbutterartig wird
Ein entscheidender Teil der Geschichte ist, wie zähflüssig die Lösung wird, wenn Wasser verloren geht. Indem sie verfolgten, wie schnell sich Spherulite ausbreiteten, und indem sie direkt die Fließeigenschaften verwandter Salzlösungen maßen, zeigten die Autorinnen und Autoren, dass gemischte Natrium–Magnesium- oder Natrium–Eisen-Lösungen außergewöhnlich viskos werden — bis zu etwa 100-mal dickflüssiger als Honig — genau in dem Moment, in dem Spherulite zu entstehen beginnen. Diese annähernd „Erdnussbutter“-Konsistenz verlangsamt die Ionenbewegung so stark, dass Diffusion, nicht die Oberflächenchemie, das Wachstumstempo der Kristalle begrenzt. In dieser trägen Umgebung bilden sich unzählige winzige Cluster und Nanokristalle und haben Zeit, zu kugelförmigen Aggregaten zusammenzukleben, anstatt zu wenigen großen, gut geformten Kristallen heranzuwachsen. Die divalenten Metallionen sind hier entscheidend: Sie binden Wasser stark und verknüpfen sich zu kurzen Ketten oder Netzwerken, die sowohl die Viskosität erhöhen als auch eine amorphe, gelartige Umgebung um die wachsenden Spherulite erzeugen.
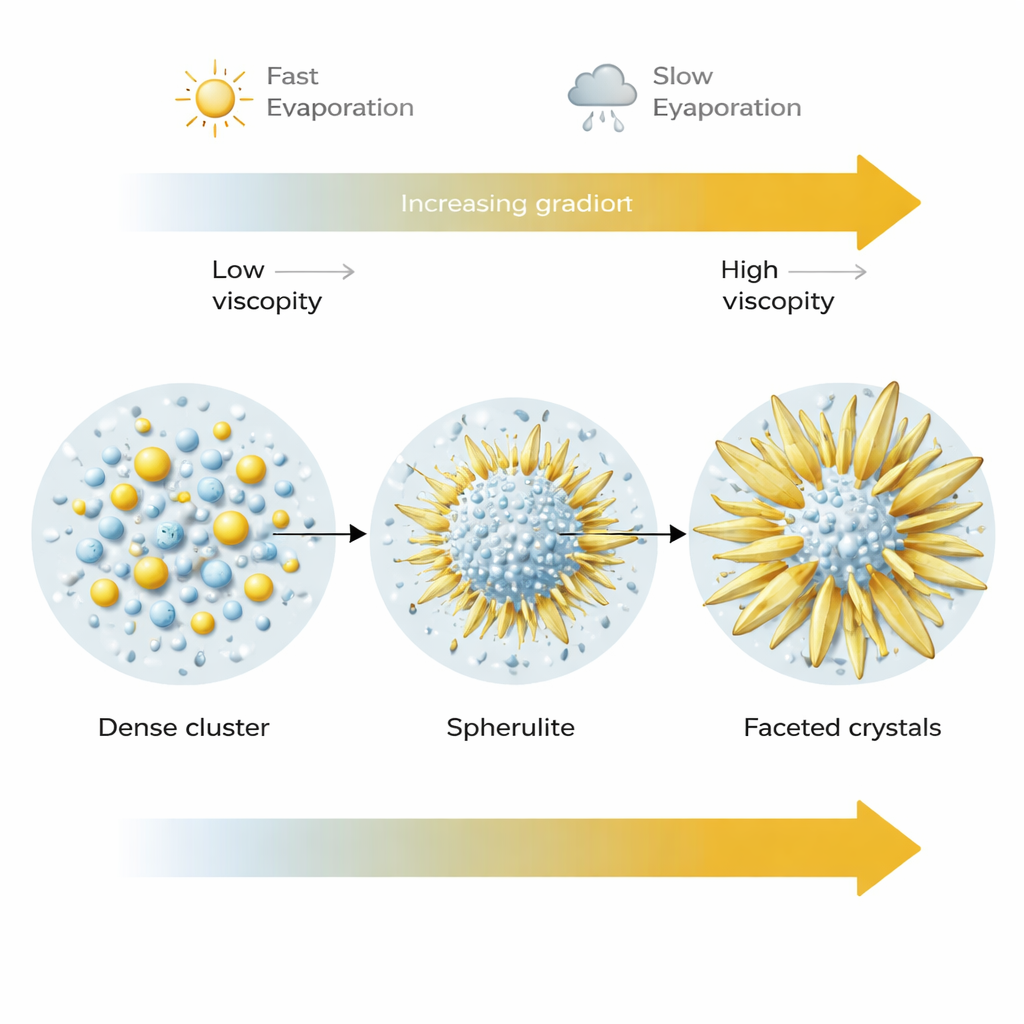
Wie die Trocknungsgeschwindigkeit die Endkristalle formt
Die Verdampfungsrate erwies sich als ein weiterer wirkungsvoller Stellhebel. Bei schnellerer Trocknung (niedrigere Luftfeuchte) nukleierten viele Spherulite, blieben aber relativ klein und in ihrer metastabilen Kugelform eingeschlossen, da die umgebende Flüssigkeit rasch eindickte. Bei langsamerer Trocknung (höhere Luftfeuchte) hatten die gleichen anfänglichen Kugeln mehr Zeit und Zugang zu gelösten Ionen. Ihre winzigen Bausteine konnten sich neu anordnen und zu größeren, glatteren und stärker facettierten Kristallen verschmelzen, die oft klingenartige Auswüchse bildeten, die schließlich in die thermodynamisch stabile Form von Natriumsulfat übergingen. Mit anderen Worten: Die kugelförmigen Strukturen fungieren als ein vorübergehendes Stadium auf einer Wachstumspath, die je nach Trocknungsgeschwindigkeit und Beweglichkeit der Materie zu sehr unterschiedlichen Endformen führen kann.
Warum das über hübsche Kristalle hinaus wichtig ist
Einfach gesagt zeigt die Studie, dass schöne, blütenartige Salz-Kugeln entstehen, wenn konzentrierte Gemische einfacher Salze so dickflüssig werden, dass alles verlangsamt wird, aber nicht so sehr, dass das Wachstum ganz stoppt. Unter diesen „gerade richtig“-Bedingungen bauen sich dichte Flüssigkeitstaschen und Schwärme winziger Kristalle zu kugelförmigen Clustern zusammen, die sich später in stabilere, facettierte Körner umwandeln können. Das Verstehen und Kontrollieren dieses sensiblen Gleichgewichts zwischen Zusammensetzung, Viskosität und Verdampfung öffnet die Tür zur Gestaltung maßgeschneiderter Kristalltexturen für Anwendungen von widerstandsfähigeren Baustoffen und verbesserten Arzneimitteln bis hin zu besseren Modellen geologischer und biologischer Kristallbildungsprozesse.
Zitation: Heeremans, T., Lépinay, S., Le Dizès Castell, R. et al. Controlled spherulitic crystal growth from salt mixtures. Commun Chem 9, 90 (2026). https://doi.org/10.1038/s42004-026-01892-0
Schlüsselwörter: Spherulite, Natriumsulfat, Kristallwachstum, nicht-klassische Keimbildung, Salzlösungen