Clear Sky Science · de
Erste Kristallstruktur eines Addukts, das bei der Reaktion einer Vanadiumverbindung mit humanem Serumtransferrin entsteht
Warum ein Blutprotein und ein Metalldrug wichtig sind
Viele experimentelle Wirkstoffe enthalten Metallatome, die helfen können, Krankheiten von Diabetes bis Krebs zu behandeln. Sobald diese metallbasierten Arzneien jedoch in den Blutkreislauf gelangen, müssen sie sich an die natürlichen Transportproteine des Körpers anlagern. Diese Studie untersucht, wie eines dieser Proteine, humanes Serumtransferrin – der Haupttransporter für Eisen im Blut – mit einer vielversprechenden Vanadiumverbindung interagiert. Das liefert Einblicke, wie Metalldrugs im Körper transportiert werden und wie sie für sicherere, effektivere Therapien verbessert werden könnten.
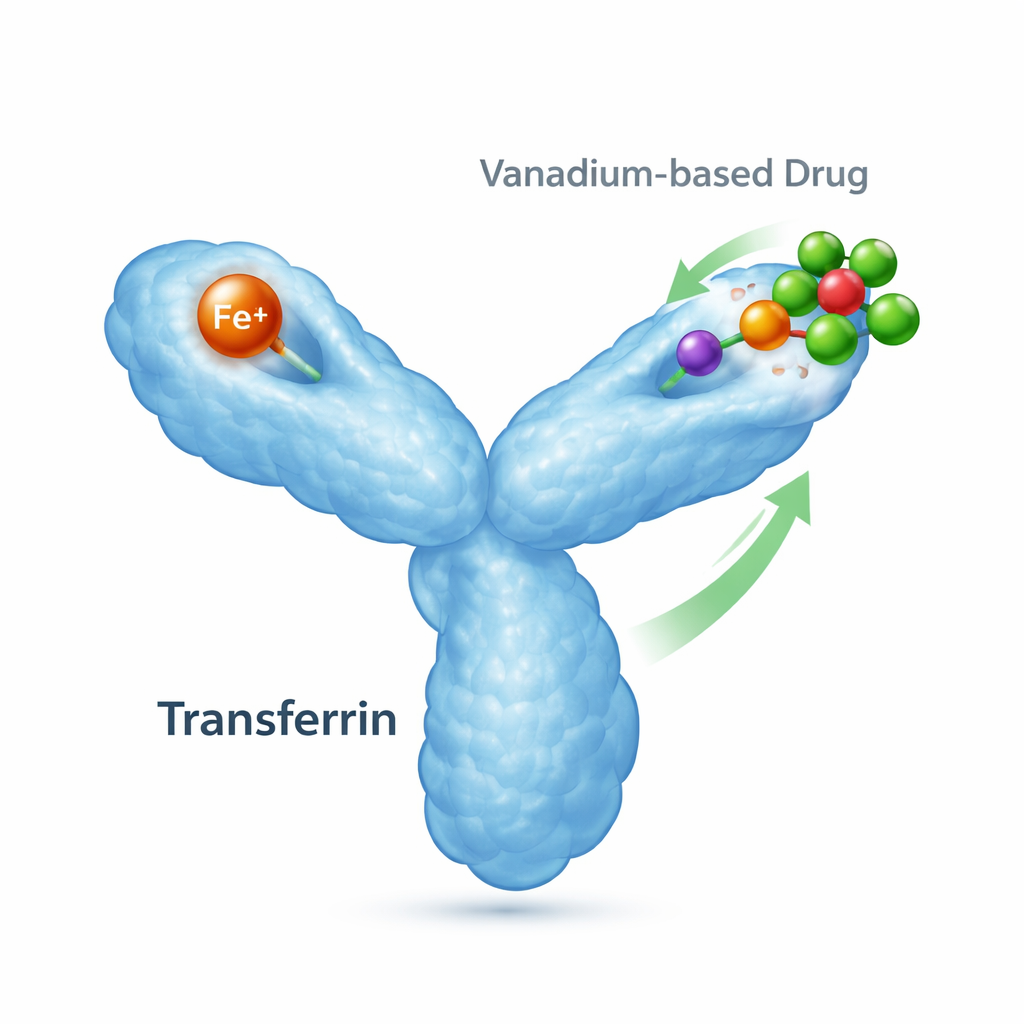
Der Eisenkurier des Körpers und seine Nebenaufgaben
Transferrin ist ein etwa 80‑Kilodalton großes Protein, dessen Hauptaufgabe darin besteht, Eisen aufzunehmen und an bedürftige Zellen zu liefern. Es besitzt zwei „Lappen“, von denen jeder ein Eisenion binden kann, und es ändert seine Form abhängig davon, ob Eisen gebunden ist. Wenn Eisen bindet, schließt sich ein Lappen; ohne Eisen bleibt er offen. Spezialisierte Rezeptoren auf Zelloberflächen erkennen diese eisenbeladenen Formen und nehmen sie auf, wodurch Transferrin zentral für das Eisen‑Gleichgewicht und die Gesundheit der Zellen ist. Transferrin kann jedoch auch andere Metalle binden, einschließlich solcher aus medizinischen Behandlungen, und beeinflusst damit möglicherweise, wohin metallbasierte Medikamente gelangen und wie sie wirken.
Ein Form‑Schnappschuss von Vanadium auf Transferrin
Die Forschenden konzentrierten sich auf einen gut untersuchten Vanadium‑Wirkstoffkandidaten, genannt bis(acetylacetonato)oxovanadium(IV), meist geschrieben als [VIVO(acac)₂]. Frühere Arbeiten zeigten, dass diese Verbindung oder in Wasser entstehende Spezies an Transferrin binden können, doch war nie genau sichtbar, wie das geschieht. Mithilfe der Röntgenkristallographie erhielten die Autorinnen und Autoren hochaufgelöste Strukturen von Transferrin, das nur im C‑terminalen Lappen Eisen trägt (die sogenannte „FeC“-Form), jeweils vor und nach der Exposition gegenüber dem Vanadiumwirkstoff. In den mit Vanadium behandelten Kristallen beobachteten sie nicht das ursprüngliche Molekül, sondern einen umgewandelten Vanadium‑Sauerstoff‑Cluster, der im eisenfreien N‑terminalen Lappen gebunden war. Damit liegt nun das erste direkte strukturelle Bild eines Vanadium‑Fragments an humanem Transferrin vor.
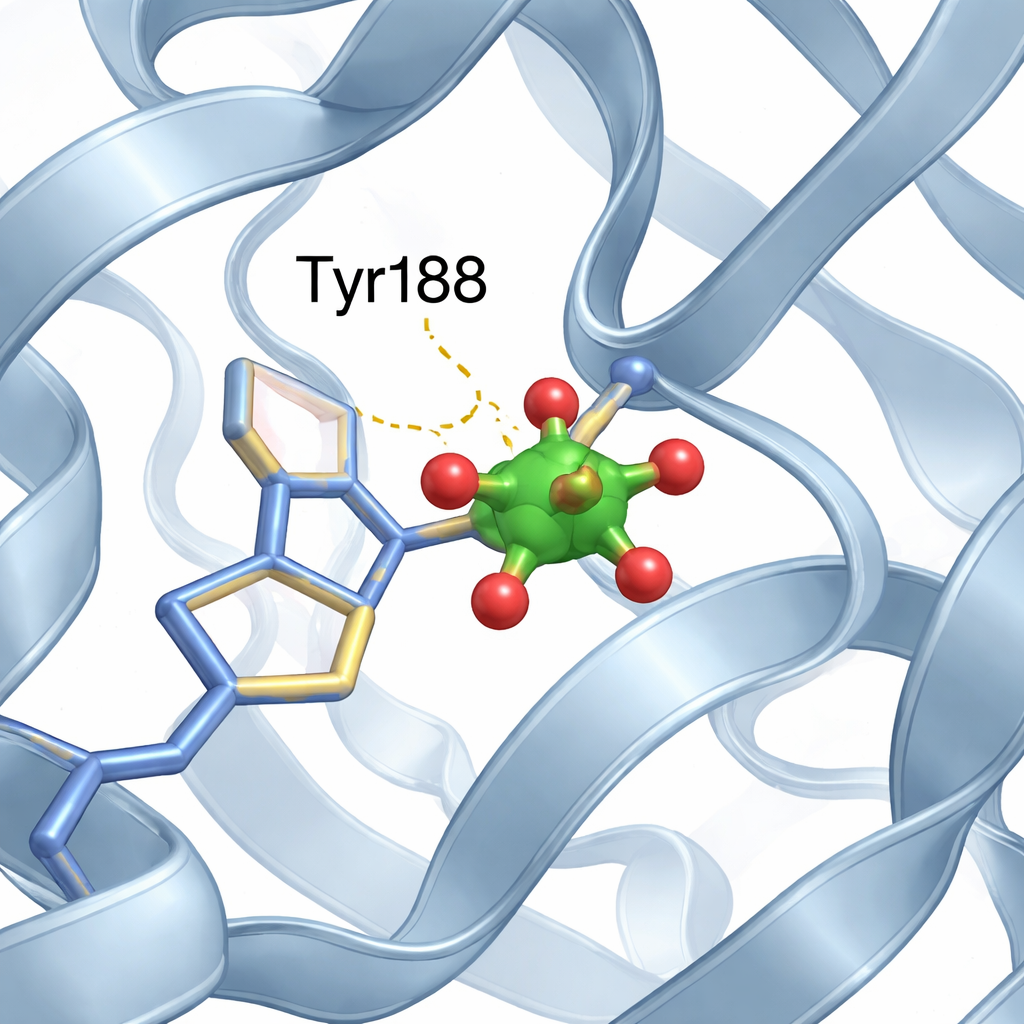
Ein winziger Vanadium‑Cluster findet eine Nische
Im Eisenbindungsplatz des N‑Lappens identifizierte das Team einen kleinen Cluster aus zwei Vanadiumatomen und Sauerstoffatomen, am besten als modifizierte „Divanadat“‑Einheit beschrieben. Eine der Sauerstoffpositionen des Clusters wird von dem Sauerstoff einer bestimmten Aminosäure, Tyrosin‑188 (Tyr188), eingenommen, wodurch eine direkte Bindung zwischen Protein und Metallcluster entsteht. Zusätzliche milde Wechselwirkungen, etwa Wasserstoffbrücken von benachbarten Proteinteilen, stabilisieren den Cluster weiter. Wichtig ist, dass trotz dieses neu gebundenen Metallgasts, der einen Eisenbindungsplatz belegt, das Protein insgesamt seine übliche offene N‑Lappen‑ und geschlossene C‑Lappen‑Anordnung beibehält, fast identisch mit der vanadiumfreien Struktur.
Wie Transferrin die Chemie von Vanadium umformt
In Lösung unter den für die Kristallisation verwendeten pH‑ und Konzentrationsbedingungen ist die in der Kristallstruktur beobachtete Zwei‑Vanadium‑Spezies normalerweise nur eine Minorität; größere Vanadium‑Sauerstoff‑Cluster dominieren eher. Spektroskopische Messungen und theoretische Speziationsberechnungen legen nahe, dass der ursprüngliche Vanadiumwirkstoff langsam in Wasser oxidiert und zerfällt, einfache Vanadat‑Ionen bildet, die sich dann zu verschiedenen Clustern zusammensetzen. Die Kristallstruktur zeigt, dass Transferrin dieses kleine divanadat‑ähnliche Fragment gegenüber den größeren Clustern selektiv stabilisiert und damit quasi eine chemische Form aus einem vielgestaltigen Lösungsgemisch „auswählt“, indem es einen passenden Bindungsplatz an Tyr188 und ein unterstützendes Wasserstoffbrückennetzwerk bereitstellt.
Die Handreichung zum Zellrezeptor bleibt erhalten
Da Transferrin einen Rezeptor auf Zelloberflächen binden muss, um Eisen zu liefern, prüften die Forschenden, ob die Anlagerung dieses Vanadiumclusters diesen wichtigen „Handschlag“ stören würde. Mit nicht‑denaturierender Gelelektrophorese und einer empfindlichen Methode namens Biolayer‑Interferometrie maßen sie, wie gut vanadiumbehandeltes Transferrin an den Transferrinrezeptor bindet verglichen mit der unbehandelten, nur eisenhaltigen Form. Beide zeigten nahezu identisches Verhalten mit sehr starker Bindung im niedrigen Nanomolarbereich. Das bestätigt, dass der Vanadiumcluster, obwohl er im N‑Lappen sitzt, die Form von Transferrin an der Rezeptor‑Interaktionsstelle nicht wesentlich verändert und daher die Erkennung des Proteins durch Zellen nicht verhindern sollte.
Was das für metallbasierte Medikamente bedeutet
Für Nicht‑Fachleute ist die Kernbotschaft, dass diese Studie einen molekularen Schnappschuss liefert, wie ein Vanadium‑Derivat an den wichtigsten Eisenkurier des Körpers bindet, ohne seine normale Funktion zu entgleisen. Transferrin kann einen spezifischen kleinen Vanadium‑Sauerstoff‑Cluster in einem Eisenbindungsplatz einfangen, während die Gesamtgestalt des Proteins und seine Fähigkeit, den Rezeptor zu binden, im Wesentlichen erhalten bleiben. Dies erklärt, wie Vanadiummedikamente möglicherweise an Transferrin im Blutkreislauf gebunden zirkulieren und macht deutlich, dass verschiedene Proteine unterschiedliche Vanadiumclustergrößen bevorzugen können. Solche Einsichten sind entscheidend, um intelligentere metallbasierte Therapeutika zu entwerfen, deren Verhalten im Blut – welche Formen sie annehmen, wohin sie gelangen und wie lange sie bestehen – vorhergesagt und gesteuert werden kann.
Zitation: Banneville, AS., Lucignano, R., Paolillo, M. et al. First crystal structure of an adduct formed upon reaction of a vanadium compound with human serum transferrin. Commun Chem 9, 89 (2026). https://doi.org/10.1038/s42004-026-01891-1
Schlüsselwörter: Vanadium‑Medikamente, humanes Serumtransferrin, metallbasierte Therapeutika, Protein‑Metall‑Bindung, Strukturelle Biologie