Clear Sky Science · de
Lactam ermöglicht entfernte Boronat‑Umlagerungen zu C═N‑Bindungen
Eine neue Abkürzung zum Bau arzneimittelähnlicher Moleküle
Chemiker suchen ständig nach schnelleren, saubereren Wegen, die komplexen Moleküle in Arzneimitteln und High‑Tech‑Materialien herzustellen. Diese Studie stellt eine clevere Abkürzung vor: ein häufiges ringförmiges Gerüst, das Lactam, fungiert vorübergehend als Reaktionsleiter und zieht sich danach leise zurück – so lassen sich einfache, leicht verfügbare Bausteine in wertvolle Vorstufen für die Pharmaindustrie verwandeln, ohne teure Metalle oder aufwendige Vorbereitungen.
Ein stiller Helfer wird zum temporären Lotse
Viele moderne Medikamente und funktionale Materialien beruhen auf Reaktionen von Boronsäuren, einer Gruppe borhaltiger Verbindungen, die wegen ihrer Zuverlässigkeit und milden Reaktivität geschätzt werden. Traditionell müssen Chemiker spezielle „dirigierende Gruppen“ in die Edukte einbauen, um Boronsäuren dazu zu bewegen, neue Bindungen mit C═N‑Doppelbindungen zu bilden. Diese Gruppen wirken wie Griffe, die die Reaktion lenken, verursachen aber zusätzlichen Zeit‑ und Kostenaufwand und funktionieren oft nur mit sehr reaktiven Partnern. Die Autoren erkannten, dass Lactame – ringförmige Verwandte der in Proteinen verbreiteten Amidbindung – als eingebaute, temporäre Lotse dienen können. Indem das Lactam‑Sauerstoffatom an das Bor bindet, entsteht ein geordnetes, vierkoordiniertes Bor‑Zentrum, das ein gebundenes Fragment über eine entfernte Position im Molekül umschichten kann und so neue C‑N‑Bindungen ermöglicht, ohne eine permanente dirigierende Gruppe zu hinterlassen.
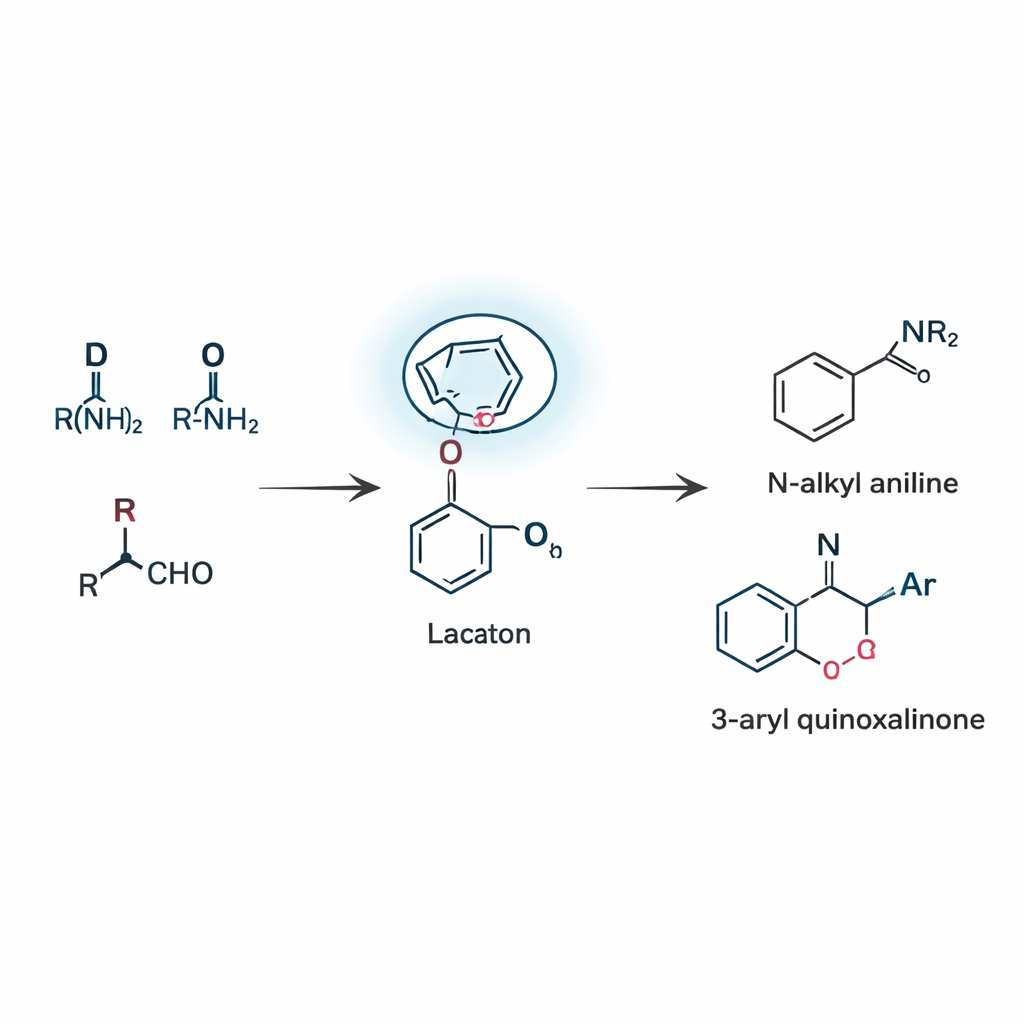
Zwei Produktfamilien mit einer Strategie aufbauen
Auf Basis dieses Konzepts entwickelten die Forscher zwei verwandte Reaktionsmodi, die beide auf dieser lactam‑geführten Umlagerung beruhen, genannt remote boronate rearrangement. Im ersten Fall verbinden sich drei einfache Bausteine – ein Aldehyd, ein Amin und eine Boronsäure – zu N‑alkyl‑Anilinen, einem Grundmotiv, das in unzähligen Arzneimittelkandidaten und Farbstoffen vorkommt. Die Reaktion verläuft über einen seltenen 1,5‑Shift, bei dem eine Arylgruppe am Bor über fünf Atome hinweg zur C═N‑Stelle springt. Durch sorgfältige Abstimmung von Katalysator, Lösungsmittel und Temperatur erzielten die Forscher annehmbare Ausbeuten und zeigten, dass viele verschiedene Substituenten – darunter Halogene, Alkylgruppen und Heterocyclen – toleriert werden. Im zweiten Reaktionsmodus wird die gleiche Leitidee auf Quinoxalinone angewandt, eine Klasse stickstoffreicher Ringe, die in der medizinischen Chemie häufig vorkommt. Hier kommt die Reaktion ganz ohne zugesetzten Metallkatalysator aus und liefert trotzdem 3‑arylierte Quinoxalinone effizient, dank der Fähigkeit des Lactams, mit Bor zu interagieren und das Schlüsselintermediat zu stabilisieren.
Grüne Bedingungen und spätes Editieren von Arzneimitteln
Neben der breiten Anwendbarkeit zeigen die Autoren, dass die Strategie auch für praxisnahe Moleküle geeignet ist. Da die 1,4‑Umlagerung an Quinoxalinonen unter metallfreien Bedingungen in einem speziellen Alkohollösungsmittel abläuft, entfällt der Bedarf an teuren oder toxischen Übergangsmetallen. Das Team wandte die Methode auf komplexe Fragmente an, die aus zugelassenen Arzneimitteln wie Ibuprofen und anderen Therapeutika abgeleitet sind und das Quinoxalinon‑Gerüst tragen. In jedem Fall wurde eine neue Arylgruppe an einer spezifischen Position eingeführt, ohne empfindliche andere funktionelle Gruppen zu stören. Diese Form der „Late‑Stage‑Funktionalisierung“ erlaubt es Chemikern, bestehende Wirkstoffkerne rasch mit neuen Seitenketten zu versehen und so die Suche nach verbesserter Wirksamkeit, Sicherheit oder physikalischen Eigenschaften zu beschleunigen.
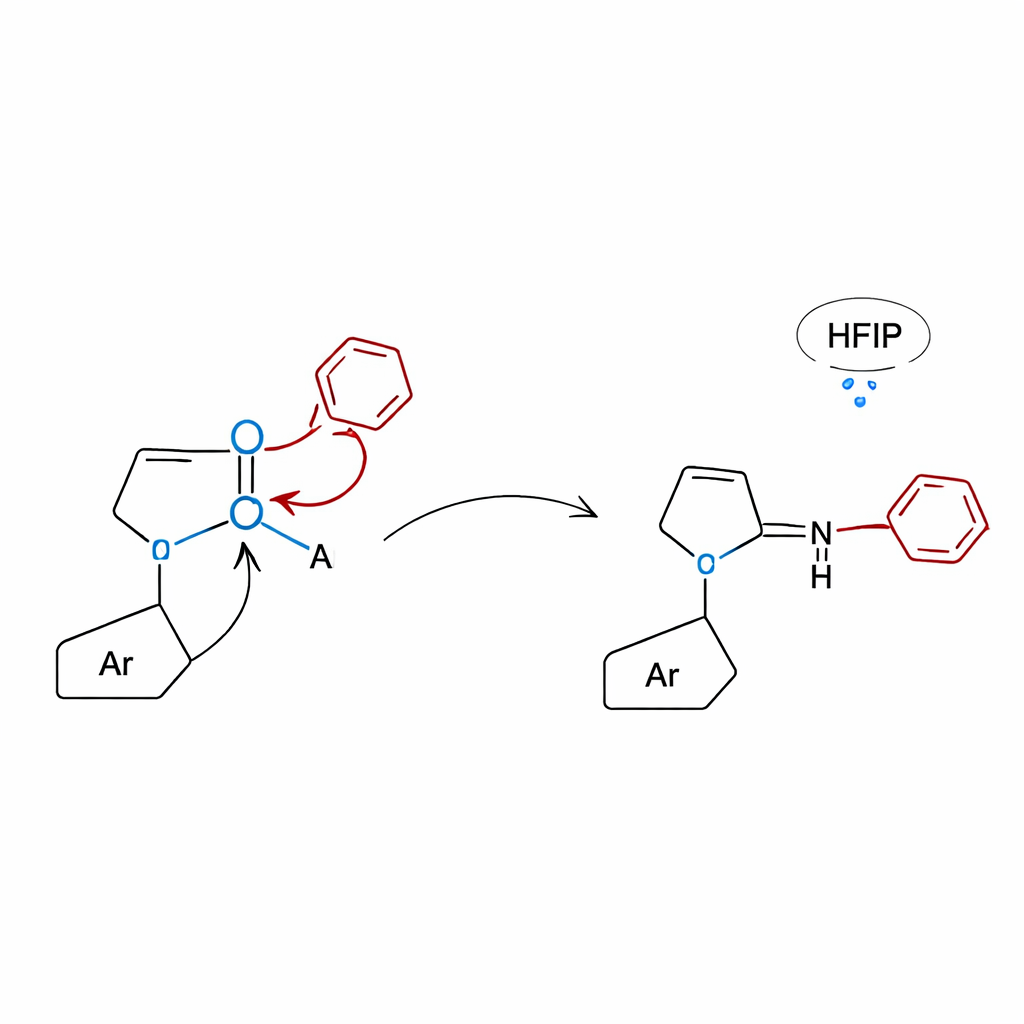
Ein Blick unter die Haube mit Theorie und Kontrolltests
Um zu verstehen, warum der Lactam‑Ansatz so gut funktioniert, kombinierten die Forscher gezielte Kontrollexperimente mit Computersimulationen. Bei Molekülen ohne Lactam‑Fragment liefen die Reaktionen praktisch nicht, was bestätigt, dass der Lactamring entscheidend für die Aktivierung der Boronsäure und die Steuerung der Umlagerung ist. Quantenchemische Rechnungen zeigten, dass das Lactam‑Sauerstoffatom an Bor bindet und eine kompakte, vierkoordinierte Struktur bildet, von der die Arylgruppe entweder über fünf Atome (1,5‑Shift) zu N‑alkyl‑Anilinen oder über vier Atome (1,4‑Shift) zu 3‑aryl‑Quinoxalinonen migrieren kann. Im Fall der Quinoxalinone senkt das durch HFIP bereitgestellte Wasserstoffbrückungsnetzwerk zusätzlich die Aktivierungsbarriere und ermöglicht so den Ablauf der Reaktion unter vergleichsweise milden thermischen Bedingungen ganz ohne zugesetzten Katalysator.
Warum das für zukünftige Medizin wichtig ist
Insgesamt zeigt die Arbeit, dass ein einfaches Lactam‑Ringgerüst als dynamischer, wiederverwendbarer Lotse wirken kann, der zuvor unzugängliche Bindungsbildungsmodi in der Boronsäuren‑Chemie erschließt. Für Nicht‑Spezialisten lautet die Kernbotschaft: Chemiker verfügen nun über einen direkteren, effizienteren Weg, einfache Bausteine in zwei wichtige Klassen stickstoffhaltiger Moleküle zu verwandeln, die vielen Arzneimitteln zu Grunde liegen. Da die Methode auf Edelmetalle verzichtet, eine breite Palette funktioneller Gruppen toleriert und an fortgeschrittenen, arzneimittelähnlichen Strukturen funktioniert, ist sie gut geeignet, das Design und die Optimierung künftiger Wirkstoffe – und möglicherweise auch neuer Agrochemikalien – zu vereinfachen.
Zitation: Lei, J., Xu, J., Li, X. et al. Lactam enables remote boronate rearrangements to C═N bonds. Commun Chem 9, 88 (2026). https://doi.org/10.1038/s42004-026-01890-2
Schlüsselwörter: Boronsäuren, Lactam‑Chemie, C–N‑Bindungsbildung, Quinoxalinone, Medizinische Chemie