Clear Sky Science · de
Enzymsuche mittels Orthologen-Inferenz zur Diversifizierung des anti‑kanzerogenen Evodiamin-Skaffolds
Pflanzenchemikalien in bessere Medikamente verwandeln
Viele heutige Medikamente stammen ursprünglich von Abwehrstoffen aus Pflanzen. Diese natürlichen Moleküle zeigen oft starke Wirkungen gegen Krebs, Infektionen oder Schmerzen, sind aber selten „perfekte“ Arzneistoffe. Chemiker möchten ihre Strukturen gezielt verändern, um sie sicherer und wirksamer zu machen, doch die Moleküle sind häufig so komplex, dass selbst kleine Modifikationen schwierig sind. Diese Studie zeigt, wie Forschende Pflanzenenzyme als winzige molekulare Werkzeuge nutzen können, um gezielte Änderungen an einem krebsbekämpfenden Molekül namens Evodiamin vorzunehmen und damit potenziell neue Wege zu verbesserten Therapien zu eröffnen.
Warum dieses Pflanzenmolekül wichtig ist
Evodiamin ist eine natürliche Verbindung, die in den Früchten eines in der traditionellen chinesischen Medizin verwendeten Baums vorkommt. Es gehört zu einer Familie ringförmiger Moleküle, die bereits die Grundlage wichtiger Medikamente gegen Krebs, Bluthochdruck und Infektionen bilden. Evodiamin selbst zeigte antikanzerogene, entzündungshemmende, schmerzstillende und antimikrobielle Eigenschaften, und einige seiner modifizierten Varianten erscheinen besonders vielversprechend als Multitarget-Krebswirkstoffkandidaten. Die Herausforderung besteht darin, an dieser dicht gepackten Struktur neue chemische „Griffe“, etwa sauerstoffhaltige Gruppen, an sehr spezifischen Positionen anzubringen, ohne aggressive Chemikalien oder mehrstufige Synthesen zu verwenden.
Die harten chemischen Aufgaben den Enzymen überlassen
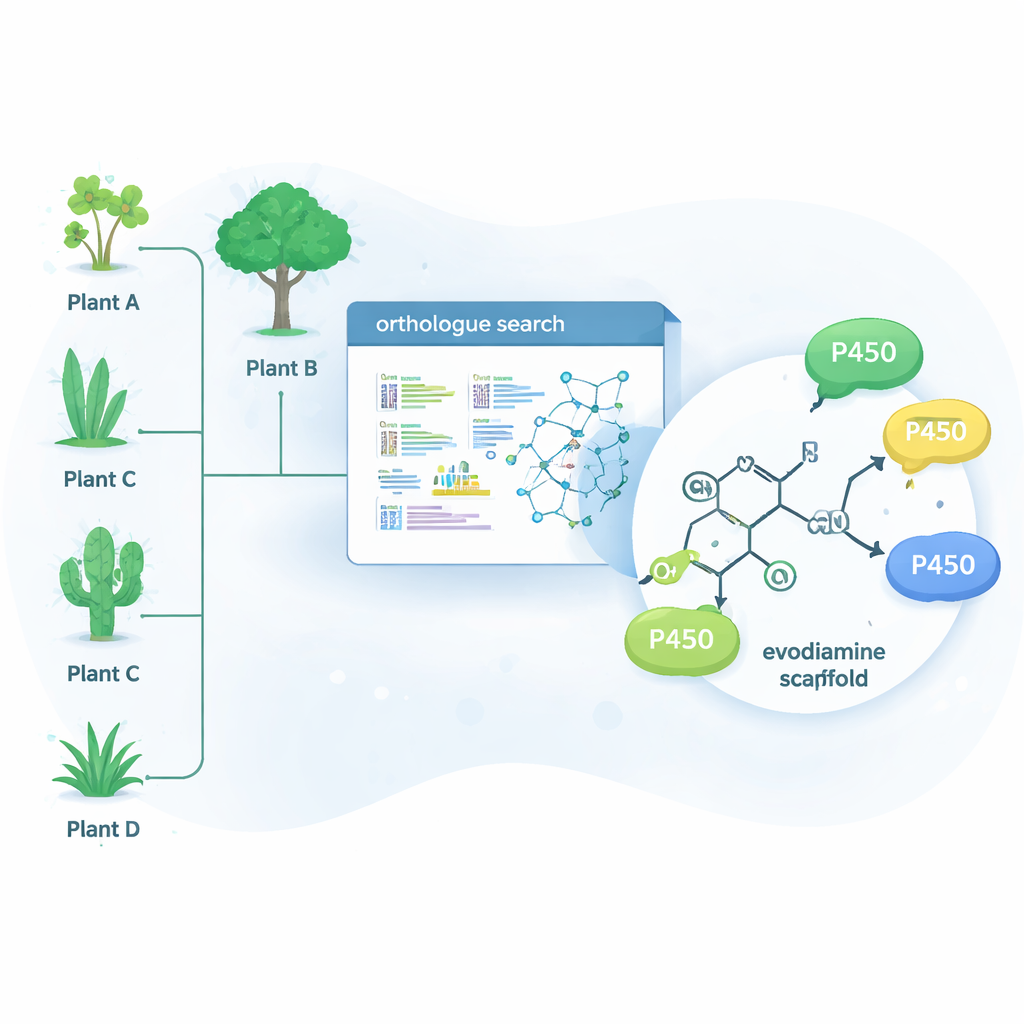
Die Natur hat viele dieser schwierigen chemischen Probleme bereits gelöst — mit Enzymen, Proteinen, die bestimmte Reaktionen katalysieren. Eine große Enzymfamilie, die Cytochrom‑P450s, ist besonders gut darin, Sauerstoff an sonst unreaktive Kohlenstoff‑Wasserstoff‑Bindungen anzufügen. Dieser einzelne Schritt kann das Verhalten eines Moleküls im Körper dramatisch verändern und zugleich einen Ansatzpunkt für weitere chemische Modifikationen schaffen. Statt nur in Pflanzen zu suchen, die natürlich Evodiamin produzieren, nutzten die Forschenden ein Bioinformatik‑Werkzeug namens OrthoFinder, um genetische Daten von 15 verschiedenen alkaloidproduzierenden Pflanzen zu durchsuchen. Sie suchten nach P450‑Enzymen, die nahe „Orthologe“ bekannter alkaloidmodifizierender Enzyme sind — in der Annahme, dass Verwandte dieser Enzyme verwandte, wirkstoffähnliche Moleküle feinabstimmen könnten.
Neue Enzyme in unerwarteten Pflanzen finden
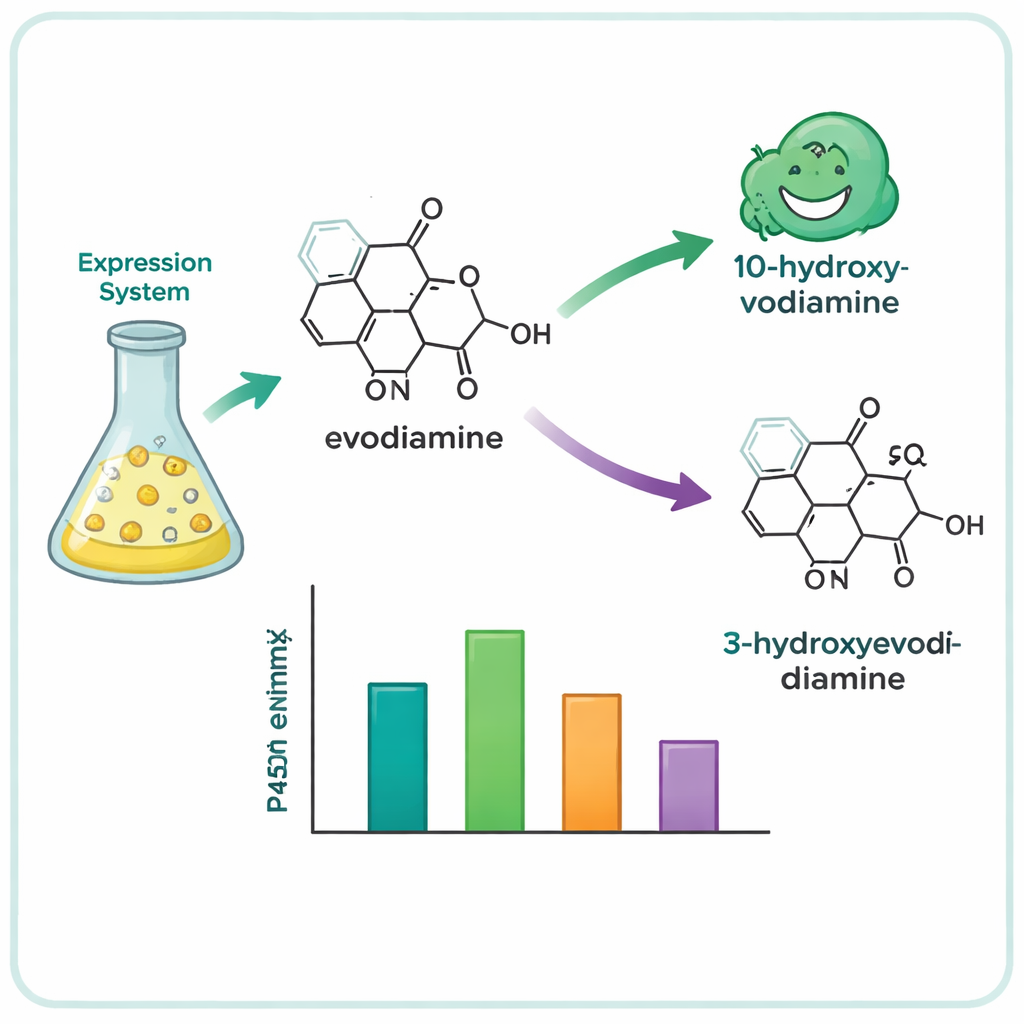
Aus hunderten Kandidatengenen reduzierte das Team die Liste auf 15 vielversprechende P450s und exprimierte sie in Hefezellen, die als kleine Enzymfabriken dienten. Diese Hefen wurden dann mit einer Sammlung komplexer Pflanzenmoleküle gefüttert und untersucht, welche davon chemisch verändert wurden. Vier Enzyme — drei aus dem Baum Camptotheca acuminata und eines aus dem Strauch Tabernaemontana elegans — wirkten auf Evodiamin, obwohl keine dieser Pflanzen bekanntermaßen Evodiamin produziert. Diese Enzyme setzten selektiv ein Sauerstoffatom an einer von zwei Positionen des Evodiamin‑Ringsystems ein und erzeugten zwei Hauptprodukte: 10‑Hydroxyevodiamin und 3‑Hydroxyevodiamin. Solche oxygenierten Varianten lassen sich leichter weiter in wasserlösliche oder wirksamere Arzneistoffkandidaten überführen, wobei schonendere Chemie ausreicht im Vergleich zu traditionellen Syntheserouten.
Ein Blick ins molekulare Werkzeugkasten
Um zu verstehen, warum diese eng verwandten Enzyme unterschiedlich reagierten, erstellten die Forschenden dreidimensionale Modelle des aktivsten Enzyms und seiner Verwandten mithilfe moderner Proteinstruktur‑Vorhersagewerkzeuge. Anschließend nutzten sie Computer‑Docking, um zu sehen, wie Evodiamin in den aktiven Taschen der Enzyme liegen könnte, nahe dem eisenhaltigen Zentrum des P450, wo die Reaktion stattfindet. Die Modelle hoben mehrere sperrige, wasserabweisende Aminosäuren—insbesondere Phenylalanin‑Reste—hervor, die nahe an den aromatischen Ringen von Evodiamin positioniert sind. Durch gezielte Mutationen dieser Positionen zeigte das Team, dass die Veränderung der Größe und Form dieser Tasche die Aktivität abschwächen, die Substratpassung verändern oder sogar den bevorzugten Oxygenierungsort von einem Ring des Moleküls zum anderen verschieben kann. In einem Fall kehrte eine einzelne Mutation die Enzympräferenz von der Bildung des 10‑Hydroxyprodukts zur Bildung des 3‑Hydroxyprodukts um.
Was das für zukünftige Medikamente bedeutet
Für Nicht‑Spezialisten ist die wichtigste Erkenntnis, dass die Autorinnen und Autoren einen praktischen Fahrplan vorgeführt haben, wie Pflanzenenzyme entdeckt und feinabgestimmt werden können, um präzise, „chirurgische“ Änderungen an komplexen wirkstoffähnlichen Molekülen vorzunehmen. Durch die Kombination groß angelegter genetischer Suche mit Enzymtests und Strukturmodellierung entdeckten sie eine Reihe von Biokatalysatoren, die das Evodiamin‑Scaffold selektiv an schwer zugänglichen Positionen umgestalten können. Das bietet nicht nur eine sauberere, nachhaltigere Möglichkeit, fortgeschrittene Evodiamin‑Varianten herzustellen — etwa wasserlösliche krebsbekämpfende Kandidaten —, sondern zeigt auch, dass nützliche Enzyme in Pflanzen zu finden sind, die das Zielmolekül selbst nie produzieren. Dieselbe Strategie lässt sich nun auf viele andere Naturstoffe anwenden und könnte die Entwicklung der nächsten Generation pflanzenbasierter Medikamente beschleunigen.
Zitation: Kwan, B.D., Kim, T., Nguyen, H.H. et al. Orthologue inference-based enzyme mining for diversification of the anti-cancer evodiamine scaffold. Commun Chem 9, 73 (2026). https://doi.org/10.1038/s42004-025-01876-6
Schlüsselwörter: evodiamin, Pflanzenenzyme, Cytochrom P450, Biokatalyse, Wirkstoffforschung