Clear Sky Science · de
PACS1-Syndrom‑Mutation stört dyneinvermittelten Frachttransport über HDAC6 und BICD2
Warum das für die Gehirnentwicklung wichtig ist
PACS1‑Syndrom ist eine seltene genetische Erkrankung, die geistige Behinderung, Anfälle und charakteristische Gesichtszüge verursacht. Familien und Kliniker kennen die Symptome, doch bis vor Kurzem war unklar, was genau in den Zellen der Betroffenen schiefläuft. Diese Studie lüftet das Rätsel, indem sie zeigt, wie eine Einzelbasenänderung im PACS1‑Gen das zelluläre Transportsystem durcheinanderbringt, besonders in Neuronen, und wie sich daraus eine Verbindung zwischen dem PACS1‑Syndrom und einer größeren Gruppe von „Verkehrs“erkrankungen des Nervensystems ergibt. 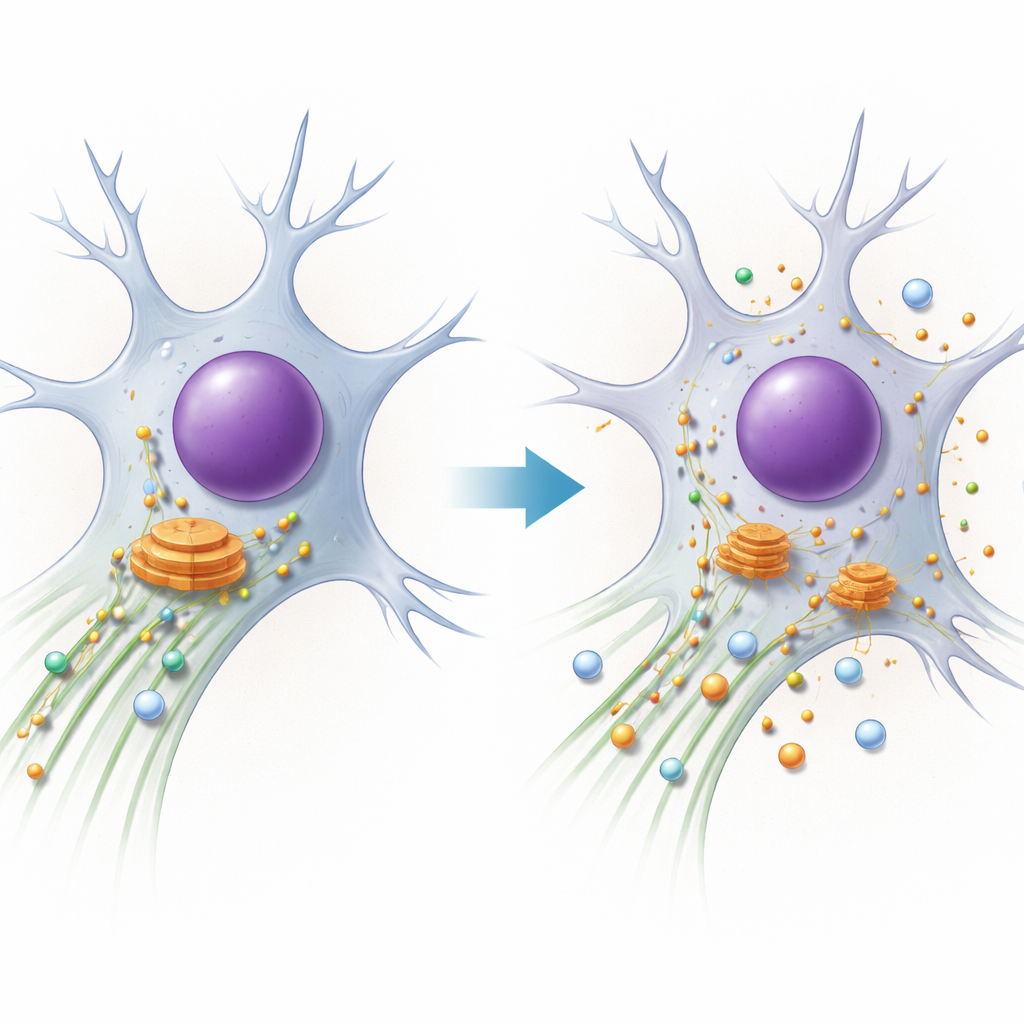
Die Lieferautobahnen der Zelle
Jede Zelle ist auf mikroskopische Autobahnen aus Proteinröhren angewiesen, den Mikrotubuli. Molekulare Motoren fahren auf diesen Schienen und transportieren Fracht wie Enzyme und Membrankompartimente zu ihren Zielorten. Ein Motor, Dynein, ist für weite „Rückfahrten“ verantwortlich und zieht Fracht vom Zellrand zurück zur Mitte, wo sich eine wichtige Sortierstation, das Golgi‑Apparat, befindet. Die Autoren konzentrieren sich auf PACS1, ein Protein, das mitbestimmt, welche Fracht Dynein mitnimmt, und außerdem den Zustand der Schienen über ein anderes Protein, HDAC6, beeinflusst, das die chemische Markierung (Acetylierung) der Mikrotubuli steuert. Neuronen mit ihren sehr langen Ausläufern sind gegenüber selbst kleinen Störungen in diesem System besonders empfindlich.
Ein mutierter Koordinator, der zu fest zupackt
Das PACS1‑Syndrom wird durch die wiederkehrende R203W‑Mutation in PACS1 verursacht. Das Team fand heraus, dass sowohl das normale als auch das mutierte PACS1 physisch an die schwere Kette von Dynein binden, die mutierte Form sich jedoch stärker anheftet. An Patientenhaut‑Zellen und gentechnisch veränderten Zelllinien zeigten sie, dass dieses Überengagement das gleiche Ergebnis liefert wie ein teilweiser Funktionsverlust von Dynein: Das Golgi zerfällt in verstreute Mini‑Stacks, und ein wichtiges Enzym namens Furin, das normalerweise an der trans‑Seite des Golgi sitzt, wird fehlgeleitet in andere Kompartimente. Durch Analyse der PACS1‑Struktur identifizierten sie einen kurzen Beta‑Strang‑„Fleck“, der spezifisch Kontakt zu Dynein aufnimmt. Wenn sie diesen Fleck veränderten, ohne andere PACS1‑Funktionen zu stören, verlor Furin erneut seine richtige Adresse, was bestätigt, dass der Dynein–PACS1‑Handschlag für korrekte Frachtplatzierung entscheidend ist. 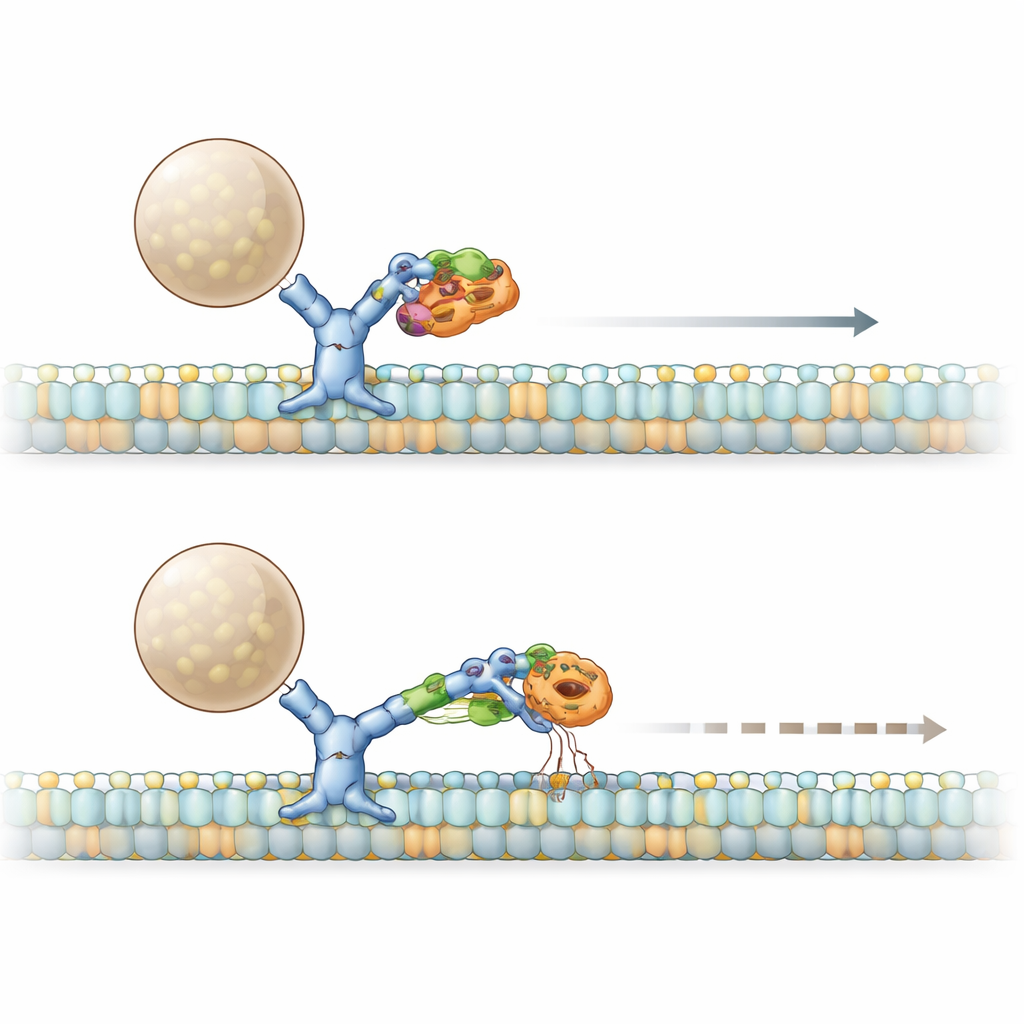
Wie eine Dreier‑Allianz den Motor blockiert
Die Geschichte vertieft sich durch zwei weitere Akteure: HDAC6 und einen Adapter namens BICD2, der beim Aufbau aktiver Dynein‑Komplexe hilft. Das mutierte PACS1 erhöht nicht nur die HDAC6‑Aktivität und reduziert so die Acetylierung der Mikrotubuli, sondern bildet auch einen vergrößerten Komplex mit HDAC6 und BICD2. Biochemische Tests zeigten, dass mutantiertes PACS1 und HDAC6 zusammen BICD2 von Dynein wegziehen, während dessen Partnerschaft mit einem vorwärtsgerichteten Motor (Kinesin) erhalten bleibt. In lebenden Zellen verlangsamte sich eine künstliche Fracht, die normalerweise flott entlang von Dynein transportiert wird, und weniger Frachtbewegungen fanden statt, wenn mutiertes PACS1 anwesend war. Die Blockade der HDAC6‑Aktivität stellte sowohl Geschwindigkeit als auch die Anzahl bewegter Partikel wieder her und zeigt, dass der mutierte PACS1–HDAC6–BICD2‑Komplex wie eine Bremse auf Dyneins Fähigkeit wirkt, Transport zu initiieren und aufrechtzuerhalten.
Verkehr mit einem natürlichen Dynein‑Helfer retten
Die Forschenden prüften anschließend, ob Dynein trotz des mutierten Komplexes „re‑aktiviert“ werden kann. Sie wandten sich Lis1 zu, einem bekannten Dynein‑Helfer, der aktive Motorassemblies stabilisiert. In Patienten‑Zellen waren Lis1‑Spiegel etwas reduziert. Als das Team zusätzliches Lis1 einbrachte, verbesserten sich zwei Dinge: Das Golgi reclusterte wieder nahe der Zellmitte, und Lysosomen, eine weitere Organelgruppe, die nach außen gedriftet war, kehrten zurück an ihren Platz. Im selben Mobilitätsassay steigerte Lis1 sowohl Häufigkeit als auch Geschwindigkeit dyneinvermittelter Frachtbewegung in Anwesenheit von mutiertem PACS1. Diese Ergebnisse zeigen, dass Dynein nicht fehlt, sondern in einem schlecht aktiven Zustand gefangen ist — ein Zustand, der teilweise durch Abschwächung von HDAC6 oder durch Stärkung der Dynein‑Aktivierung korrigiert werden kann.
Ein seltenes Syndrom mit einem breiteren Erkrankungsspektrum verknüpfen
Durch die Kombination aus Strukturanalyse, Zellbiologie und Live‑Bildgebung schlagen die Autoren ein klares Modell vor: Normalerweise verbindet PACS1 ausgewählte Fracht mit Dynein und justiert die Motorleistung über HDAC6 und Mikrotubulus‑Acetylierung. Die R203W‑Mutation erweitert die Interaktionsfläche von PACS1 und rekrutiert zu viel HDAC6 und BICD2 in einen Komplex, der Dyneins Fähigkeit, Mikrotubuli zu erfassen und effizient zu bewegen, untergräbt. Das Ergebnis ist weit verbreitete Fehlplatzierung von Golgi, Lysosomen und anderer Fracht, besonders in Neuronen, in denen Langstreckentransport lebenswichtig ist. Dieser Mechanismus hilft zu erklären, warum das Herabsetzen von PACS1 oder HDAC6 mit Antisense‑Therapien Gehirndefekte in Mausmodellen behebt und inzwischen auch bei Patientinnen und Patienten erforscht wird. Breiter betrachtet ordnet dies das PACS1‑Syndrom in das wachsende Spektrum der Mikrotubulus‑Transportstörungen ein, neben Erkrankungen, die durch Mutationen in Dynein, BICD2 und verwandten Transportfaktoren verursacht werden.
Zitation: Yang, Y., Thomas, L., Chen, K. et al. PACS1 syndrome mutation disrupts dynein-mediated cargo transport via HDAC6 and BICD2. Commun Biol 9, 450 (2026). https://doi.org/10.1038/s42003-026-09924-0
Schlüsselwörter: PACS1-Syndrom, dyneintransport, Mikrotubulus‑Transport, Golgi‑Organisation, neurale Entwicklung