Clear Sky Science · de
Das Typ‑VI‑Sekretionssystem von Acinetobacter: Mechanismen, Biologie und therapeutisches Potenzial
Versteckte Waffen in Krankenhauskeimen
Viele Menschen wissen, dass einige Krankenhauskeime Antibiotika entgegentreten können, doch weniger ist bekannt, dass diese Mikroben auch heftige Kämpfe untereinander ausfechten. Dieser Übersichtsartikel beleuchtet einen mikroskopischen „federgespannten Speer“ in Acinetobacter, einer Gruppe von Bakterien, zu der auch der berüchtigte Krankenhauskeim Acinetobacter baumannii gehört. Zu verstehen, wie diese eingebaute Waffe funktioniert, wann sie aktiviert wird und wie sie Infektionen fördert, könnte neue Wege für die Diagnostik und Entwaffnung lebensbedrohlicher, medikamentenresistenter Infektionen eröffnen.
Eine Überlebensmaschine, nicht nur ein Giftpfeil
Acinetobacter‑Arten leben im Boden, im Wasser und auf unserer Haut, doch einige haben sich zu sehr erfolgreichen Krankenhauspathogenen entwickelt. Ein wichtiges Werkzeug in ihrem Arsenal ist das Typ‑VI‑Sekretionssystem (T6SS), eine winzige kontraktile Maschine, die in der Zellhülle verankert ist. Bei Auslösung feuert sie einen nadelartigen Spike mit toxischen Proteinen in benachbarte Zellen und tötet oft konkurrierende Bakterien praktisch auf Kontakt. Anders als manche Keime, die mehrere Versionen dieses Systems tragen, besitzen krankheitserregende Acinetobacter in der Regel nur ein T6SS; dennoch hat es diese einzelne Plattform so umgestaltet, dass sie vielen Zwecken dient — vom Abwehren von Rivalen bis zur Gestaltung von Infektionen.
Umgebaute Hardware: eine ungewöhnliche Startplattform
Die meisten Bakterien bauen ihr T6SS um einen standardisierten Satz von Teilen herum, doch Acinetobacter hat mehrere Schlüsselkomponenten neu gestaltet. Es fehlt ein gängiger Außenmembrananker namens TssJ; stattdessen verlässt man sich auf ein Trio spezialisierter Helfer: TsmK bildet ein Fundament in der Innenmembran, TslA stabilisiert ein langes „Tunnel“‑Protein (TssM), während TagX die Zellwand lokal durchschneidet, um der Waffe Platz zu machen. Darüber hinaus muss ein bestimmtes Spike‑Protein, VgrG1, nahezu perfekt geformt sein, damit das System überhaupt feuert — einzelne Aminosäureänderungen können es deaktivieren. Zusammengenommen zeigen diese Anpassungen, wie die Evolution fehlende Teile durch neue Lösungen ersetzen kann, während das grundlegende Abschussprinzip erhalten bleibt.
Intelligente Steuerung: wann Angriffsmodus Sinn ergibt
Der Aufbau und das Abfeuern dieser Nanomaschine sind energieaufwendig, daher hält Acinetobacter sie streng unter Kontrolle. Ein global bindendes DNA‑Protein (H‑NS) und spezielle Repressoren, die auf multiresistenten Plasmiden getragen werden, können das System in der „Aus“‑Position verriegeln, besonders wenn Resistenzgene zwischen Zellen ausgetauscht werden. Bei hoher Zelldichte können chemische Quorum‑Signale es einschalten und die Bakterien auf Konkurrenz im Nahbereich vorbereiten. Metallionen spielen ebenfalls eine Rolle: Unter oxidativem Stress aktiviert aufgenommenes Mangan eine kleine RNA, die dafür sorgt, dass zentrale T6SS‑Botschaften abgebaut werden, wodurch die Waffe zugunsten des Überlebens im Wirt heruntergeregelt wird. Sogar die Kapsel — ein zuckerreicher Außenmantel — wirkt sowohl als Schild als auch als Bremse: Sie blockiert eintreffende Angriffe, dämpft aber gleichzeitig mechanisch das eigene Abschussvermögen von Acinetobacter.
Ein vielfältiger Werkzeugkasten mikroskopischer Schläge
Wenn Acinetobacter den Abzug betätigt, kann es eine breite Palette von Toxinen ausliefern. Manche Enzyme zersetzen die robuste Zellwand von Rivalen; andere nagen still an Zellmembranen, und wieder andere zerschneiden DNA in Zielzellen. Jedes Toxin ist mit einem passenden „Immunitäts“‑Protein gepaart, das den Angreifer vor Freund‑Feuer schützt. Ein DNA‑schneidendes Toxin, inzwischen TafE genannt, kann sogar Pilze töten, was auf überreichstumliche Gefechte in Bereichen wie Darm oder Lunge hindeutet. Genomische Studien deuten darauf hin, dass Acinetobacter noch viele weitere, bislang uncharakterisierte Toxine kodiert, oft gebündelt in großen Rhs‑Proteinen, die als modulare Träger fungieren. Statt sich auf einen einzelnen Schlag zu verlassen, scheinen diese Bakterien geschichtete Angriffe zu nutzen, die gleichzeitig mehrere lebenswichtige Strukturen schädigen.
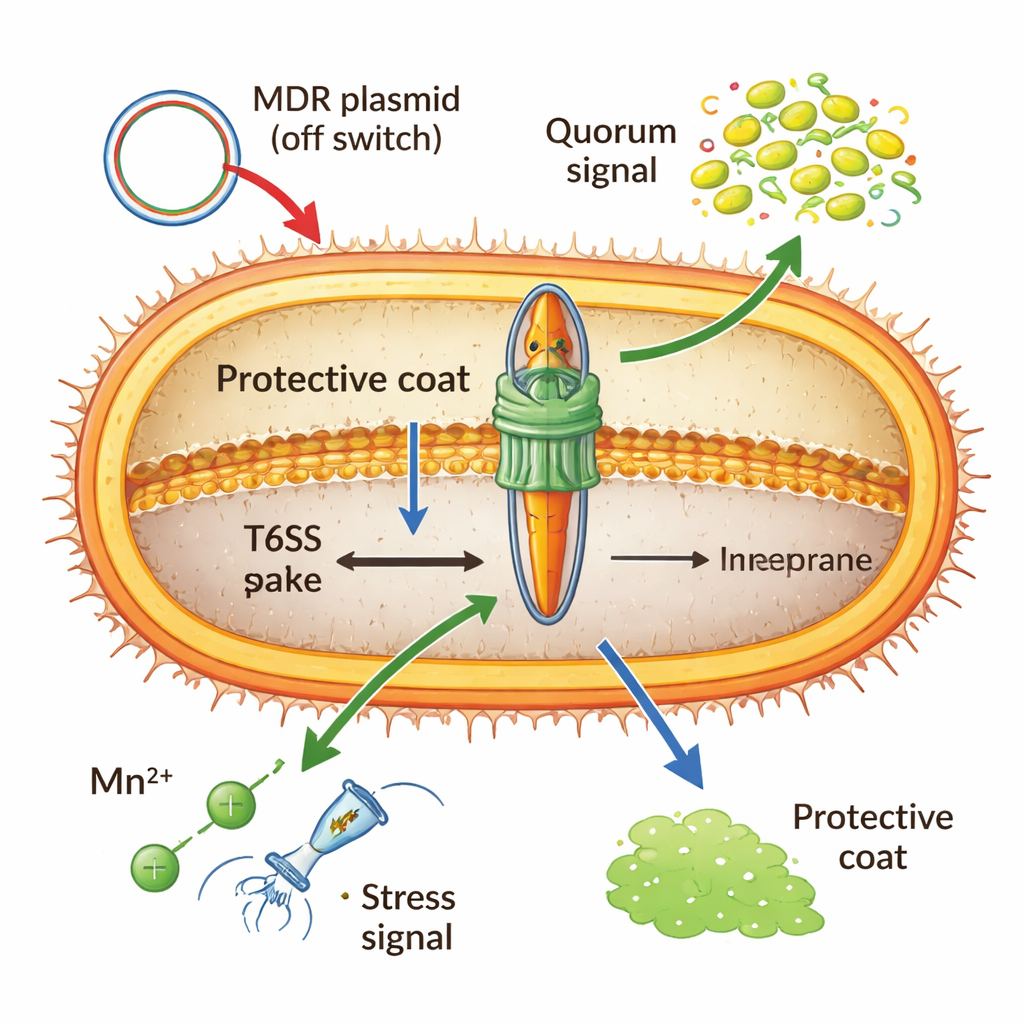
Infektionen, Gene und künftige Behandlungen formen
Erkenntnisse aus Patientenisolaten und Tiermodellen legen nahe, dass ein aktives T6SS häufig mit schwereren Erkrankungen, stärkerer Entzündung und verbessertem Überleben der Bakterien im Wirt einhergeht. Indem es benachbarte Mikroben tötet, setzt das System zudem DNA frei, die von natürlicherweise kompetenten Acinetobacter‑Zellen aufgenommen werden kann und so die Verbreitung von Eigenschaften wie Antibiotikaresistenz beschleunigt. Gleichzeitig ist die dauerhafte Aktivität der Waffe kostspielig, weshalb viele erfolgreiche Krankenhausstämme Plasmide oder Mutationen tragen, die sie stummschalten, sobald die Resistenz gesichert ist. Insgesamt argumentieren die Autoren, dass dieses Sekretionssystem nicht als einfacher Virulenzfaktor, sondern als flexibles „Fitness‑Modul“ zu sehen ist, das Acinetobacter je nach Bedarf hoch- oder herunterregelt, um Aggression, Persistenz und Energieverbrauch auszubalancieren. Diese neue Sichtweise weist auf praktische Anwendungen hin — von Impfstoffen, die konservierte T6SS‑Teile anvisieren, bis zu Wirkstoffen, die gezielt den Abschussmechanismus blockieren und Ärzten helfen könnten, einem gefährlichen und anpassungsfähigen Krankenhausgegner zuvorzukommen.
Zitation: Jie, J., Gu, S., Li, D. et al. The type VI secretion system of Acinetobacter: mechanisms, biology and therapeutic potential. Commun Biol 9, 327 (2026). https://doi.org/10.1038/s42003-026-09782-w
Schlüsselwörter: Acinetobacter, Typ‑VI‑Sekretionssystem, Antibiotikaresistenz, bakterielle Konkurrenz, Krankenhausinfektionen