Clear Sky Science · de
Glykosylierung als dynamischer Regulator der RLR- und cGAS-STING-Weg der angeborenen Immunität
Wie Zuckeretiketten Zellen helfen, Viren zu erkennen
Unsere Zellen sind ständig auf der Hut vor eindringenden Viren, und ein großer Teil dieser Abwehr beruht auf winzigen Zuckeretiketten, die an Proteine hängen. Diese Übersichtsarbeit erklärt, wie diese Zuckeranhängsel, bekannt als Glykosylierung, eher wie Dimmer denn als einfache Ein/Aus-Schalter für zentrale antivirale Signalwege wirken. Das Verständnis dieser zuckerbasierten Feinabstimmung könnte neue Wege eröffnen, Impfstoffe zu verbessern, virale Infektionen zu behandeln und das Immunsystem gegen Krebs zu nutzen.
Der Frühwarnalarm der Zelle
Wenn Viren in eine Zelle eindringen, hinterlassen sie charakteristische RNA- oder DNA-Stränge. Spezialisierte „Alarm“-Systeme durchkämmen das Zellinnere nach diesem genetischen Abfall. Ein System, das RIG-I-like receptor (RLR)-System genannt wird, erkennt virale RNA. Ein anderes, bekannt als cGAS–STING-Weg, nimmt DNA wahr, die am falschen Ort innerhalb der Zelle erscheint. Einmal ausgelöst, schalten beide Wege chemische Kaskaden ein, die in der Freisetzung von Typ-I-Interferonen und entzündungsfördernden Molekülen münden — starke Signale, die benachbarte Zellen warnen und Immunabwehr mobilisieren. Da zu viel oder zu wenig dieser Antwort gefährlich sein kann, muss die Zelle diese Alarme sorgfältig justieren, und Glykosylierung ist eine der Schlüsselmethoden, mit denen sie das tut. 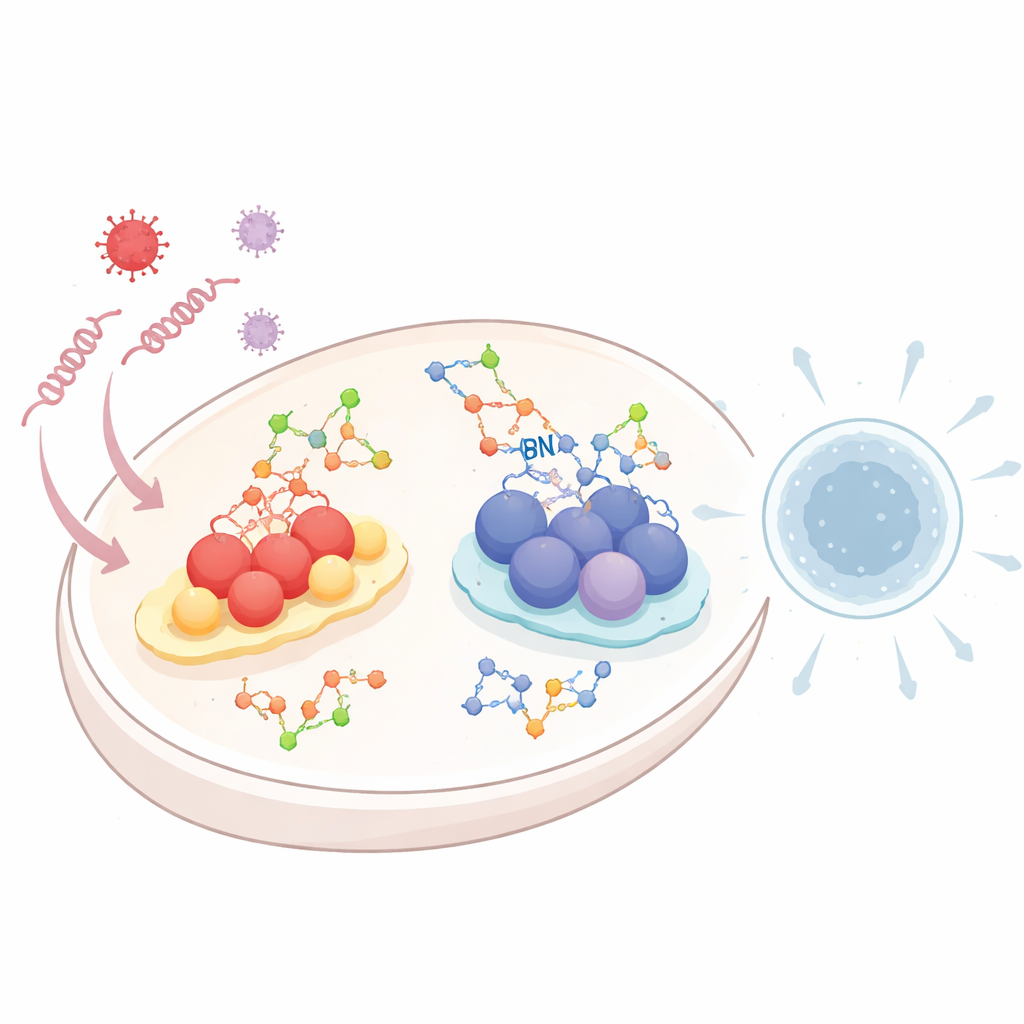
Zuckerschichten als Präzisionskontrollen
Glykosylierung fügt Proteinen in verschiedenen Zellkompartimenten kleine Zuckerbausteine hinzu. Im internen Versandnetz der Zelle, dem endoplasmatischen Retikulum und Golgi-Apparat, helfen sperrige N-gebundene Zuckerketten Proteinen, korrekt zu falten, stabil zu bleiben und zur richtigen Membran zu gelangen. Im Gegensatz dazu platziert eine schlankere Form, die O-GlcNAcylierung, einen einzelnen Zucker auf Proteinen im Zytoplasma und Zellkern. Dieses minimalistische Etikett ist hochdynamisch und wird schnell umgeschlagen, da zwei Enzyme es in Reaktion auf Nährstofflage und Stress hinzufügen oder entfernen. Die Übersicht beschreibt, wie diese unterschiedlichen Zuckertypen Sensoren nicht einfach an- oder ausschalten; stattdessen regulieren sie, wie leicht Sensoren sich zusammenlagern, wie lange sie bestehen bleiben und wie stark sie Signale aussenden. Auf diese Weise verbindet Glykosylierung den Stoffwechselzustand der Zelle direkt mit ihrer Bereitschaft, Infektionen zu bekämpfen.
Feinabstimmung des RNA-Erkennungsweges
Im RNA-erkennenden RLR-System sitzt ein zentrales Relaisprotein namens MAVS auf den Mitochondrien und fungiert als wichtiger Knotenpunkt. Die Übersichtsarbeit zeigt, dass O-GlcNAcylierung an MAVS die antivirale Signalgebung je nach Position der Zuckeranlagerung sowohl beschleunigen als auch bremsen kann. Zuckeretiketten an bestimmten Stellen fördern weitere Proteinmodifikationen, wie eine spezifische Form von Ubiquitinketten, die MAVS helfen, große Signalaggregate zu bilden und starke Interferonantworten gegen RNA-Viren zu treiben. Andere Zuckerstellen halten MAVS im Ruhezustand verteilt und inaktiv, um unnötige Entzündungen zu verhindern. Virusinfektion und Veränderungen im zellulären Zucker-produzierenden Stoffwechselweg können das Gleichgewicht zwischen diesen aktivierenden und hemmenden Etiketten verschieben. Verwandte Modifikationen an einem anderen Faktor, IRF5, können das Immunsystem in Richtung schädlicher „Zytokinstürme“ treiben, was verdeutlicht, dass mehr Zucker nicht immer besser ist. Parallel dazu können Viren N-gebundene Zucker auf zelloberflächenständigen Proteinen wie dem Wachstumsfaktor-Rezeptor EGFR ausnutzen, um vorgeschaltete Sensoren wie RIG-I zur Degradation zu kennzeichnen und so antivirale Abwehrkräfte abzuschwächen.
Feinabstimmung des DNA-Erkennungsweges
Der DNA-erkennende cGAS–STING-Weg wird ebenfalls stark durch Glykosylierung geprägt. STING, ein Membranprotein des endoplasmatischen Retikulums, benötigt N-gebundene Zuckerketten, um korrekt zu falten, stabil zu bleiben und sich nach Aktivierung durch DNA-abgeleitete Botenstoffe in Signalaggregate zusammenzubauen. Ohne diese Zucker kann STING nicht die höhergeordneten Strukturen bilden und durch die Zellkompartimente transportiert werden, die für eine robuste Interferonfreisetzung erforderlich sind. Gleichzeitig fördert O-GlcNAcylierung von STING an einer bestimmten Stelle eine andere Reihe chemischer Markierungen, die seine Aggregation und Bewegung unterstützen und antivirale Signale gegen DNA-Viren verstärken. Zuckerketten, sogenannte sulfatisierte Glykosaminoglykane, die im Golgi aufgebaut werden, helfen zusätzlich, indem sie aktiviertes STING zur Polymerisation in lange Strukturen unterstützen, die nachgeschaltete Enzyme rekrutieren. Viren kontern, indem sie ihre eigenen Glykoproteine verändern oder Abbauwege auslösen, die STING anvisieren, häufig in denselben zellulären Bereichen, in denen diese Zuckerdekorationen beigefügt oder verarbeitet werden. 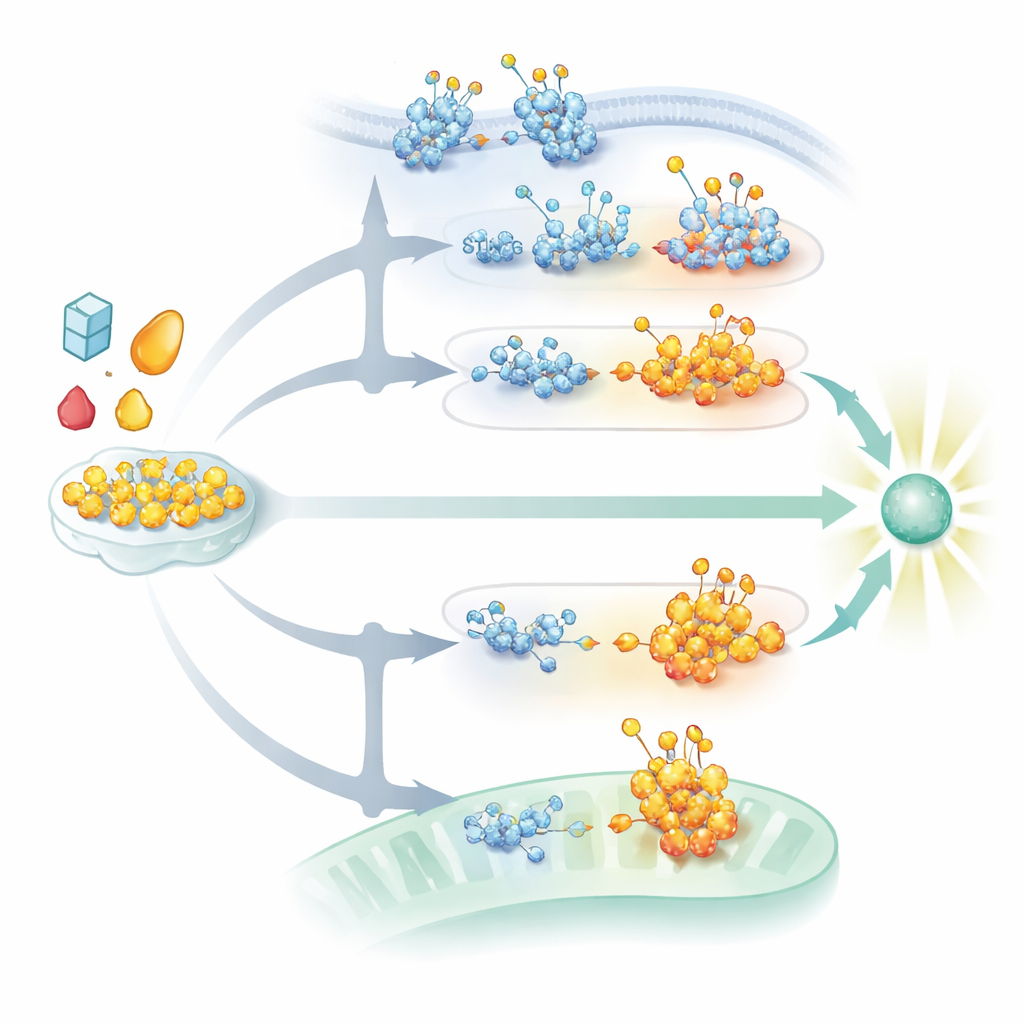
Stoffwechsel, Krankheit und zukünftige Therapien
Da der Haupt-Zuckerspender für O-GlcNAcylierung über einen Stoffwechselweg hergestellt wird, der als hexosamin-Biosyntheseweg bekannt ist, formen Verschiebungen in der Nährstoffnutzung die antivirale Signalgebung direkt. Viele Viren treiben diesen Weg zu ihrem Vorteil an, während experimentelles Verstärken oder Blockieren des Hexosaminflusses antivirale Antworten in Tiermodellen stärken oder abschwächen kann. Die Übersichtsarbeit verknüpft diese Mechanismen mit menschlichen Krankheiten: Tumoren verdrahten Glykosylierung häufig um, um Interferon-Signale zu dämpfen und der Immunerkennung zu entgehen, während chronischer metabolischer Stress oder vererbte Defekte in der Glykane-Verarbeitung das Gleichgewicht in Richtung schädlicher Autoimmunreaktionen kippen können. Die Autorinnen und Autoren argumentieren, dass Enzyme, die Glykosylierung steuern — insbesondere solche, die O-GlcNAc hinzufügen oder entfernen oder Schlüssel-N-gebundene Strukturen aufbauen — vielversprechende, aber anspruchsvolle Wirkstoffziele sind. Zukünftige Therapien werden wahrscheinlich ortsspezifisch und kontextsensitiv wirken müssen, um den „Glyko-Code“ so zu beeinflussen, dass er besseren Schutz vor Infektionen, Krebs und entzündlichen Erkrankungen bietet, ohne neue Formen der Immunfehlregulation auszulösen.
Das große Ganze für die Gesundheit im Alltag
Alltäglich gesprochen zeigt dieser Artikel, dass die vordersten antiviralen Alarmsysteme des Körpers nicht isoliert funktionieren — sie sind in den Energiehaushalt und die Zuckerchemie der Zelle integriert. Winzige Zuckeretiketten an einer Handvoll kritischer Proteine entscheiden darüber, ob ein fehlplatziertes virales Genom eine maßvolle Warnung, eine umfassende Abwehr oder eine gefährliche Überreaktion auslöst. Indem Forscher dieses zuckerbasierte Kontrollsystem entschlüsseln und schließlich zu justieren lernen, hoffen sie, Behandlungen zu entwickeln, die Impfstoffe wirksamer machen, hartnäckige Infektionen besser beseitigen, Tumoren für das Immunsystem sichtbar machen und außer Kontrolle geratene Entzündungen bei Autoimmunerkrankungen beruhigen.
Zitation: Tong, J., Zhang, W., Xue, M. et al. Glycosylation as a dynamic regulator of RLR and cGAS-STING innate immune signalling pathways. Commun Biol 9, 422 (2026). https://doi.org/10.1038/s42003-026-09767-9
Schlüsselwörter: angeborene Immunität, Glykosylierung, RLR-Signalweg, cGAS-STING, O-GlcNAcylierung