Clear Sky Science · de
Strukturelle Einblicke in die Typ-IV-Pilus-Maschinerie von Thermus thermophilus, die zwei unterschiedliche Pili zusammenbaut
Kleine bakterielle Haare mit großen Aufgaben
Bakterien sind zwar mikroskopisch klein, doch viele tragen bemerkenswerte Oberflächen»haare«, die ihnen Bewegung, Haftung an Oberflächen und sogar das Aufnehmen fremder DNA aus der Umgebung ermöglichen. In dieser Studie untersuchen die Forschenden, wie ein thermophiles Bakterium, Thermus thermophilus, eine hochentwickelte Nanomaschine baut und betreibt, die diese Haare – so genannte Pili – durch die Zellhülle nach außen schiebt. Das Verständnis dieser Maschinerie zeigt nicht nur, wie Mikroben sich anpassen und entwickeln, sondern liefert auch Inspiration für künftige Nanotechnologien und neue Ansätze, schädliche Bakterien zu deaktivieren.
Zwei verschiedene Haare aus einer Maschine
Thermus thermophilus produziert zwei unterschiedliche Pilustypen: einen breiteren, dickeren Filamenttyp und einen schmaleren, feineren. Frühere Arbeiten zeigten, dass diese Filamente aus unterschiedlichen Bausteinen bestehen und vermutlich verschiedene Aufgaben erfüllen, etwa Fortbewegung entlang von Oberflächen oder das Aufnehmen von DNA. Beide werden jedoch von derselben mehrteiligen Maschine gebaut, die sich von der inneren bis zur äußeren Zellmembran erstreckt. Die zentrale Frage dieser Studie lautet, wie ein einziges System zwei verschiedene Filamente zusammensetzen und sie durch die Schutzschichten der Zelle nach außen führen kann.
Die verborgene Hardware kartieren
Um aufzudecken, wie die Maschine zusammengesetzt ist, nutzten die Forschenden Kryo-Elektronentomographie, eine Technik, die Zellen sehr schnell einfriert und bei tiefen Temperaturen in 3D abbildet. Sie kombinierten diese Aufnahmen mit gezielten genetischen Eingriffen, die bestimmte Maschinenteile entfernten oder veränderten. Durch den Vergleich normaler Zellen mit Mutanten, denen bestimmte Komponenten fehlten, konnten sie erkennen, welche unscharfen Formen in ihren 3D-Karten zu welchen Proteinen gehören. Fortschrittliche Strukturvorhersagewerkzeuge dienten dann als molekulare Baupläne, um diese Proteinmodelle in die beobachteten Dichten einzupassen und ein hypothetisches Vollmodell der Maschinerie zusammenzustellen.
Eine flexible Verbindung, die alles zusammenhält
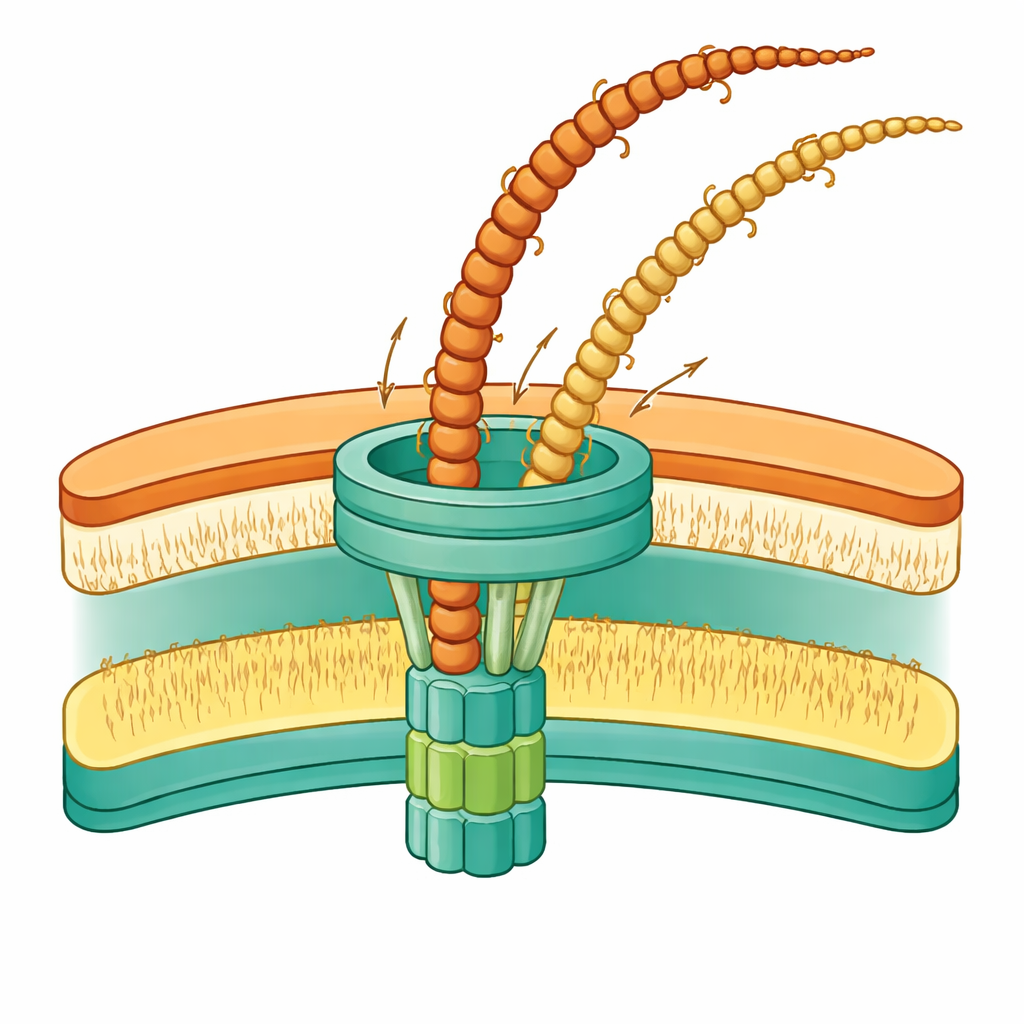
Ein auffälliges Ergebnis betrifft ein Protein namens PilW. Diese Komponente sitzt zwischen einem Tor in der äußeren Membran und einer inneren Plattform, die in der inneren Membran verankert ist. Fehlt PilW vollständig, erreichen die Pili nicht die Außenfläche, sondern sammeln sich im Raum zwischen den Membranen. Wird nur ein Teil von PilW abgeschnitten, funktioniert die Maschine zwar weiterhin, doch ihre inneren Bestandteile verschieben sich und die umgebenden Membranen biegen sich nach innen. Diese Beobachtungen deuten darauf hin, dass PilW wie eine flexible Leine wirkt, die das äußere Tor mit der inneren Plattform verbindet und ihre Länge und Form anpasst, während die Maschine zwischen Ruhezustand und Aktivität wechselt. Die Modelle des Teams zeigen, dass diese Flexibilität es dem System ermöglicht, mit dem ungewöhnlich großen Abstand zwischen den beiden Membranen bei Thermus umzugehen und dabei dennoch alle Teile ausreichend auszurichten, um Pili zusammenzubauen und auszuwerfen.
Die Filamente und ihre Zuckerschichten beobachten
Zusätzlich zur In‑Zell‑Bildgebung isolierten die Forschenden die beiden Pilustypen und untersuchten sie mit Einzelpartikel-Kryo-Elektronenmikroskopie detaillierter. Dieser höher auflösende Ansatz zeigte die präzise Anordnung der Bausteine und erlaubte es dem Team vor allem, die Zuckermoleküle zu modellieren, die die Oberfläche der Filamente schmücken. Der breitere Pilus trägt drei Zuckeransatzstellen pro Baustein und erzeugt so einen dichten Kohlenhydrat‑Halo. Der schmalere Pilus hat nur eine solche Stelle, doch sein Zuckerglied ragt weiter heraus, wodurch das Gesamtfilament größer erscheint, als es sein Proteinkern vermuten lässt. Computersimulationen untersuchten dann, wie sich diese Zucker biegen und schwanken, wenn das Filament durch das Tor der äußeren Membran passiert.
Ein gemeinsames Tor für zwei sehr unterschiedliche Kabel
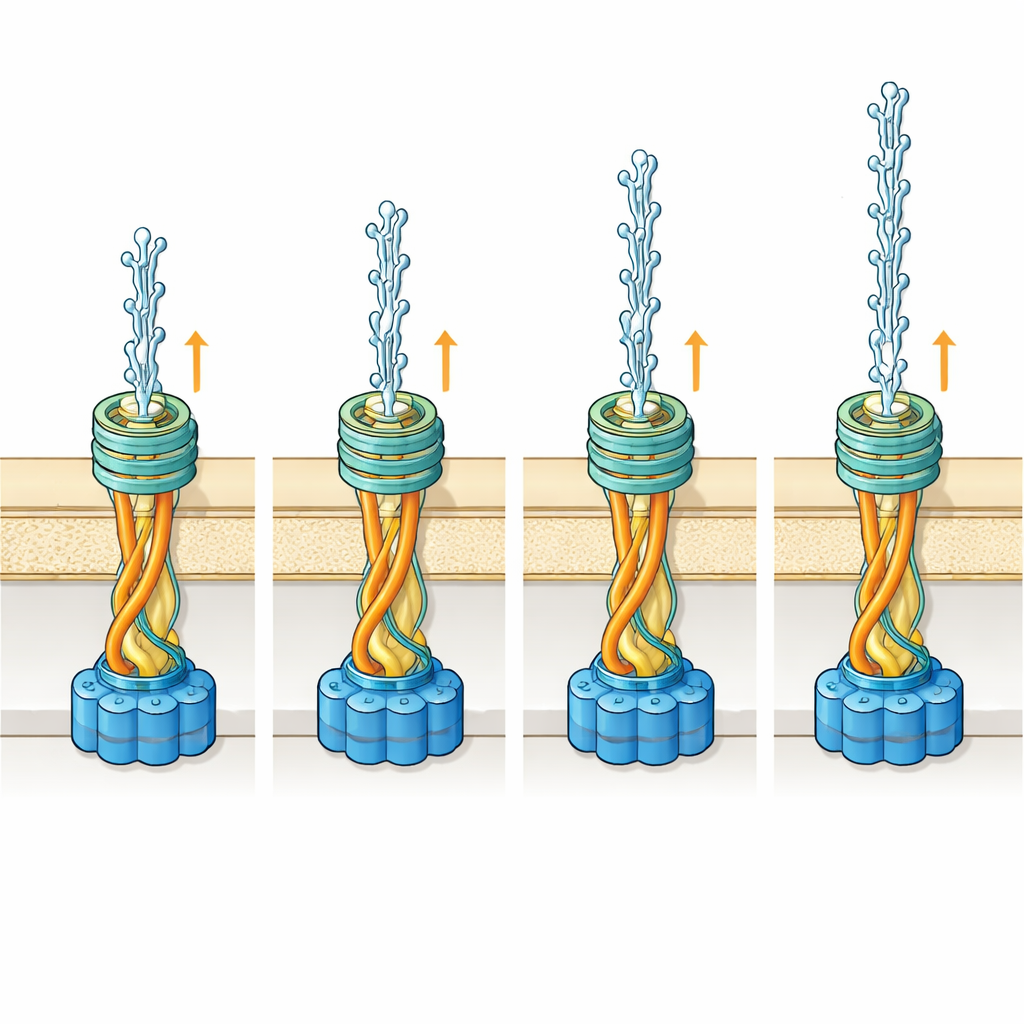
Indem sie ihre detaillierten Pilusstrukturen in ein Modell des äußeren Membrantors, genannt PilQ, einpassten, fanden die Forschenden heraus, dass grundsätzlich beide Filamenttypen durch dieselbe Öffnung gleiten können. Für das breitere Filament haben die zahlreichen Zucker genug Raum, um beim Durchtritt viele Konformationen einzunehmen. Beim schmaleren Filament wird es an einer Stelle im Kanal enger, sodass einige Zucker‑Konformationen mit den Wänden kollidieren würden. Simulationen legen nahe, dass in diesem Fall die Zuckerketten im Inneren des Tors näher am Filament anliegen und sich erst außerhalb der Zelle auffächern. Anstatt ein größeres, aufwändigeres Tor zu entwickeln, scheint das Bakterium also auf die natürliche Flexibilität dieser Zuckerketten zu bauen, um das System effizient funktionieren zu lassen.
Was das für das mikrobielle Leben bedeutet
Insgesamt zeichnet die Studie ein schlüssiges Bild davon, wie eine einzige anpassungsfähige Maschine in einem Thermenbakterium zwei sehr verschiedene Pili herstellt und exportiert. Ein flexibles Verbindungsprotein hält offenbar die Innen‑ und Außenkomponenten ausgerichtet, während der Motorzyklus abläuft und die Struktur sich bei aktivem Filamentwachstum leicht verkürzt. Gleichzeitig verleihen die Zuckerschichten den Pili sowohl Schutz als auch Reichweite, bleiben aber flexibel genug, um durch einen relativ engen Ausgangskanal zu passen. Für Nicht‑Spezialisten lautet die Kernaussage: Selbst einfache Mikroben verlassen sich auf hochkoordinierte, bewegliche Assemblies zum Überleben und zur Evolution – molekulare Geräte, deren Eleganz und Effizienz mitunter menschgemachten Nanomaschinen ebenbürtig oder überlegen ist.
Zitation: Neuhaus, A., McLaren, M., Isupov, M.N. et al. Structural insights into the Thermus thermophilus type IV pilus machinery assembling two distinct pili. Commun Biol 9, 474 (2026). https://doi.org/10.1038/s42003-026-09762-0
Schlüsselwörter: Typ-IV-Pili, bakterielle Nanomaschinen, Kryo-Elektronenmikroskopie, Protein-Glykosylierung, Thermus thermophilus