Clear Sky Science · de
Modellierung, die von Wachstumsraten ausgeht, legt nahe, dass phänotypische Anpassung die Arzneimittelresistenz bei BRAFV600E‑mutiertem Melanom antreibt
Krebszellen, die lernen, mit Medikamenten zu leben
Zielgerichtete Medikamente haben die Behandlung für viele Menschen mit Melanom, einer ernsthaften Form von Hautkrebs, verändert. Trotzdem hören diese Medikamente fast immer irgendwann auf zu wirken: Tumoren, die sich zuvor verkleinerten, beginnen wieder zu wachsen. Diese Studie stellt eine einfache, aber folgenreiche Frage: Können sich Melanomzellen statt ausschließlich durch genetische Mutationen auch durch Verhaltensänderungen an die Behandlung „anlernen“ — und könnte dieses Lernen erklären, warum manche Verabreichungs‑Schemata besser funktionieren als andere?
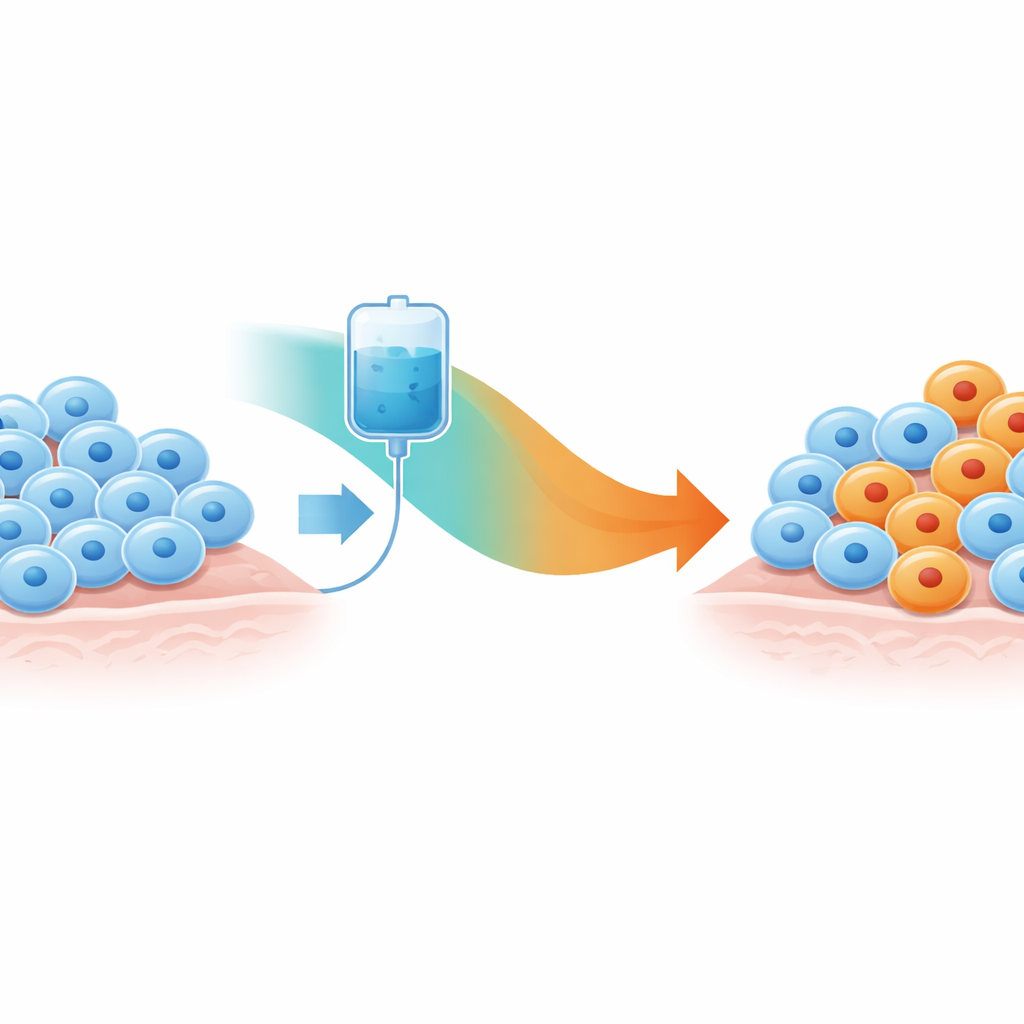
Von empfindlichen Zellen zu Überlebenden
Die Forschenden konzentrierten sich auf Melanomzellen mit einer häufigen Veränderung im BRAF‑Gen, die sie besonders sensibel für eine Klasse von Wirkstoffen macht, den BRAF‑Inhibitoren. In Laborversuchen aus früheren Arbeiten wurden diese Zellen über verschiedene Dosen und Zeiträume dem Wirkstoff Encorafenib ausgesetzt. Durch genaue Messungen, wie schnell die Zellen unter jeder Bedingung wuchsen oder abstürben, teilten die Autorinnen und Autoren die Zellen in zwei grobe Kategorien: medikamenten‑naive Zellen, die das Mittel nie gesehen hatten, und medikamenten‑adaptierte Zellen, die mindestens eine Woche im Wirkstoff gelebt hatten. Medikationsnaive Zellen wuchsen ohne Behandlung gut, wurden durch das Medikament jedoch stark verlangsamt oder abgetötet. Medikationsadaptierte Zellen hingegen wuchsen in Gegenwart des Medikaments besser, verloren diesen Vorteil aber, wenn das Medikament entfernt wurde — ein Hinweis darauf, dass ihr Überleben mit einem flexiblen, reversiblen Zustandswechsel verbunden ist und nicht mit dauerhaften genetischen Veränderungen.
Eine Karte verborgener Zellverhalten
Um diese Veränderungen zu erklären, bauten die Forschenden ein mathematisches Modell, in dem jeder Krebszelle ein „Phänotypzustand“ zugewiesen wird — eine abstrakte Position auf einer Skala von sehr medikamentensensibel bis sehr medikamentenresistent. Statt nur zwei Zelltypen anzunehmen, erlaubten sie viele Zwischenzustände, die graduelle Verschiebungen im Verhalten widerspiegeln, wie sie an biologischen Markern der Resistenz beobachtet werden. Für jede Kombination aus Zustand und Wirkstoffdosis schätzten sie eine Nettowachstumsrate, die positiv (mehr Zellteilungen als Zelltod) oder negativ (mehr Zelltod als Teilung) sein konnte. All diese Raten wurden in einer Matrix, einer „Fitness‑Matrix“, angeordnet, die wie eine Landschaft wirkt: Einige Zustände bei bestimmten Dosen sind gute Orte zum Gedeihen, andere tödlich. Zellen im Modell können sich Schritt für Schritt über diese Landschaft bewegen, wenn die Behandlung an- oder abgeschaltet wird.
Treiben Zellen dahin oder klettern sie zum Vorteil?
Die entscheidende Unbekannte war, wie sich Zellen über diese Landschaft bewegen. Die Autorinnen und Autoren prüften vier mögliche Strategien. In einer ändern sich Zellen nie ihren Zustand, sodass resistente Zellen von Anfang an vorhanden sein müssten. In einer anderen wandern Zellen zufällig zwischen benachbarten Zuständen, wie bei einem taumelnden Spaziergang, unabhängig davon, ob sich ihre Lage verbessert. In den beiden verbleibenden Strategien neigen Zellen dazu, in Zustände zu wechseln, in denen ihre Wachstumsrate höher ist — entweder mit Rauschen und Fehltritten oder stark gerichtet, immer hin zu besserer Überlebensfähigkeit. Als das Team Computersimulationen durchführte und mit realen Labordaten verglich, insbesondere mit Experimenten, in denen das Medikament entweder kontinuierlich oder in einem An‑Aus‑Muster (eine Woche an, eine Woche aus) verabreicht wurde, konnten nur die Strategien, in denen Zellen zu höherer Fitness hinaufklettern, die beobachteten Ergebnisse reproduzieren: Intermittierende Behandlung mit hoher Dosis unterdrückte die Zellzahlen besser als kontinuierliche Behandlung mit derselben Gesamtzeit und einer insgesamt höheren Medikamentenmenge.
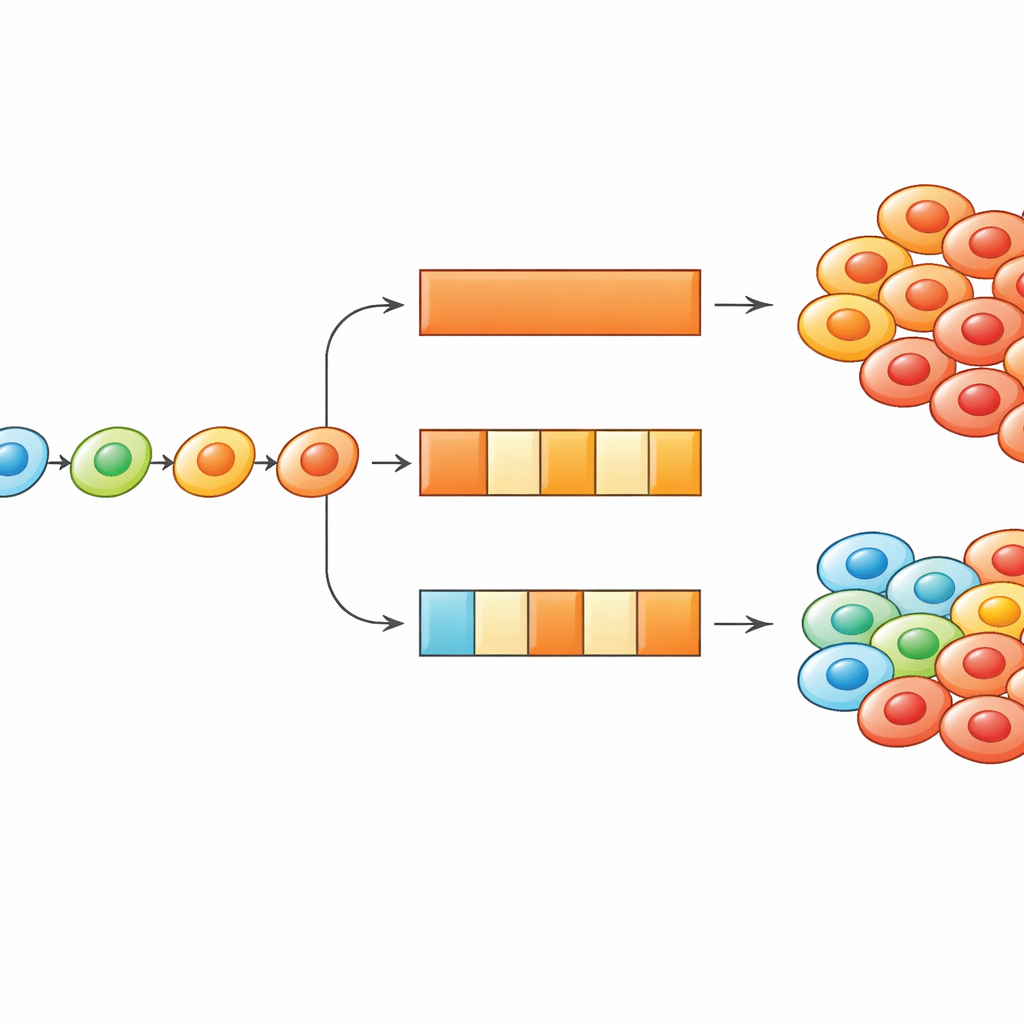
Mit An‑Aus‑Dosierung die Anpassung gegen den Krebs wenden
Die Forschenden gingen weiter und nutzten sowohl Simulationen als auch einfachere Gleichungen, um zu untersuchen, wie häufig Zellen ihren Zustand ändern dürfen und wie lange Phasen mit und ohne Medikament dauern. Sie fanden heraus, dass bei gerichteter Anpassung die Behandlungspläne so abgestimmt werden können, dass diese Anpassung entweder verlangsamt oder ausgenutzt wird. Eine Verringerung der Frequenz, mit der Zellen ihren Zustand aktualisieren können — konzeptionell das Verlangsamen der biologischen Mechanismen, die phänotypische Veränderungen ermöglichen — macht intermittierende Behandlungen tendenziell wirksamer, weil Zellen nicht so schnell zu hochresistenten Zuständen klettern können. Umgekehrt können, falls Zellen in einem stark resistenten Zustand beginnen, Medikamentenpausen ihnen Zeit geben, wieder in sensiblere Zustände zurückzurutschen, sodass die Wiedereinführung des Medikaments einen Anstieg des Zelltods auslöst. Die Studie zeigt, wie die zeitliche Abstimmung der Dosierung und die Geschwindigkeit der zellulären Anpassung zusammen bestimmen, welcher Zeitplan am besten wirkt.
Was das für die zukünftige Krebsversorgung bedeutet
Für Laien lautet die zentrale Botschaft, dass Krebszellen nicht nur feste Feinde sind; sie sind Formwandler. In diesem Melanomsystem scheinen die Zellen aktiv in Richtungen zu wandern, die ihnen helfen, unter den jeweiligen Bedingungen zu wachsen. Das Modell der Autorinnen und Autoren legt nahe, dass diese gerichtete Anpassung allein — ohne die Annahme unterschiedlicher dauerhafter Klone — erklären kann, warum An‑Aus‑Medikationen manchmal konstante Dosierung übertreffen, selbst wenn sie insgesamt weniger Wirkstoff verwenden. Obwohl diese Ergebnisse aus im Labor gezüchteten Zellen stammen und noch weitere Arbeit benötigen, bevor sie die Patientenversorgung leiten können, bietet der Ansatz einen praktischen Rahmen: Indem man misst, wie schnell und in welche Richtung Krebszellen sich anpassen, könnten Ärztinnen und Ärzte künftig Behandlungspläne entwerfen, die das phänotypische „Lernverhalten“ der Tumoren nicht nur angreifen, sondern in Sackgassen lenken statt in Fluchtrouten.
Zitation: Hamis, S., Browning, A.P., Jenner, A.L. et al. Growth rate-driven modelling suggests that phenotypic adaptation drives drug resistance in BRAFV600E-mutant melanoma. Commun Biol 9, 385 (2026). https://doi.org/10.1038/s42003-026-09760-2
Schlüsselwörter: Melanom, Arzneimittelresistenz, Zellplastizität, intermittierende Therapie, mathematische Modellierung