Clear Sky Science · de
Strukturelle Grundlage der Aktivierung der quinolabhängigen Stickstoffmonoxid-Reduktase von Neisseria meningitidis durch Dimerisierung
Wie Bakterien unsere Immunabwehr überlisten
Wenn schädliche Bakterien in den Körper eindringen, setzen unsere Immunzellen toxische Moleküle wie Stickstoffmonoxid frei, um sie zu töten. Manche Krankheitserreger haben jedoch molekulare Tricks entwickelt, um diesen Angriff zu neutralisieren und zu überleben. Diese Studie zeigt auf atomarer Ebene, wie ein zentrales bakterielles Enzym seine Form in Paare umstellt, um deutlich effizienter beim Entgiften von Stickstoffmonoxid zu werden, und warum das Verständnis dieses Formwandels neue Wege für die Entwicklung von Antibiotika eröffnen könnte.
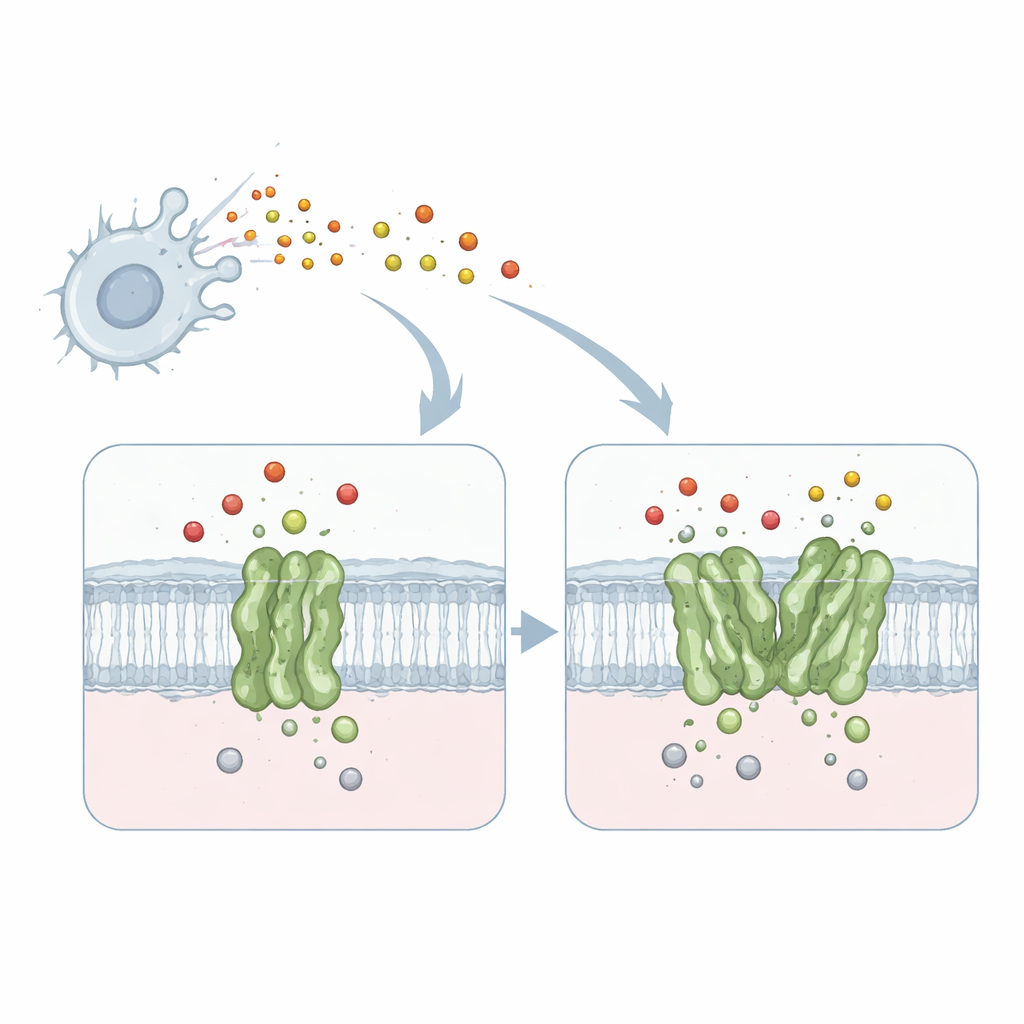
Eine winzige Maschine, die ein giftiges Gas außer Gefecht setzt
Die Arbeit konzentriert sich auf ein Membranprotein namens quinolabhängige Stickstoffmonoxid-Reduktase, kurz qNOR, aus dem Meningitis-auslösenden Bakterium Neisseria meningitidis. qNOR sitzt in der bakteriellen Zellmembran und wandelt Stickstoffmonoxid – ein von unserem Immunsystem erzeugtes giftiges Gas – in weniger schädliche Produkte um. Diese Entgiftung ermöglicht es dem Mikroben, weiter zu atmen und zu wachsen, selbst in feindlichen Umgebungen wie menschlichen Makrophagen. Da Atmung und Entfernung von Stickstoffmonoxid für das Überleben des Erregers entscheidend sind, ist qNOR ein attraktives Ziel für neue antimikrobielle Wirkstoffe.
Einzelne sind gut, Paare sind besser
Frühere biochemische Studien zeigten, dass qNOR entweder als Einzelbaustein (Monomer) oder als Paar (Dimer) existieren kann und dass das Dimer zwei- bis viermal schneller bei der Neutralisierung von Stickstoffmonoxid arbeitet. Bis jetzt war unklar, warum das bloße Zusammenfügen zweier identischer Enzymkopien eine so dramatische Leistungssteigerung bewirkt. Um dies zu klären, nutzten die Forscher hochauflösende Einzelpartikel-Kryo-Elektronenmikroskopie, um detaillierte dreidimensionale Strukturen sowohl des monomeren als auch des dimeren qNOR aus demselben Bakterienstamm zu erfassen. Sie erhielten nahezu atomare Auflösungen – 1,89 Å für das Dimer und 2,25 Å für das Monomer – scharf genug, um einzelne Aminosäure-Seitenketten, Metallionen und viele Wassermoleküle zu lokalisieren.
Eine flexible Helix wird zur stabilisierenden Klammer
Überraschenderweise wirkte das katalytische Zentrum des Enzyms – das Metallzentrum, in dem Stickstoffmonoxid umgewandelt wird – in beiden Formen fast identisch. Die entscheidenden Unterschiede traten stattdessen etwas weiter entfernt auf, in einer transmembranären Helix namens TM10 und in der Art, wie sie bei der Paarung zweier qNOR-Moleküle eine andere Helix (TM2) berührt. Im Monomer ist TM10 lose verankert und kann stark schwingen und sich biegen, wie computergestützte Analysen der Kryo-EM-Daten zeigten. Im Dimer riegelt TM10 jedes Partners gegen den Nachbarn ab und bildet ein Bündel aus vier Helices, das seine Beweglichkeit stark einschränkt. Diese Stabilisierung verschiebt subtil eine entscheidende Aminosäure, ein Glutamat namens Glu563, bringt sie in die Nähe eines anderen Glutamats (Glu494) in der Nähe des aktiven Zentrums und formt eine fokussiertere Route für eintreffende Protonen, die für die Reaktion benötigt werden.
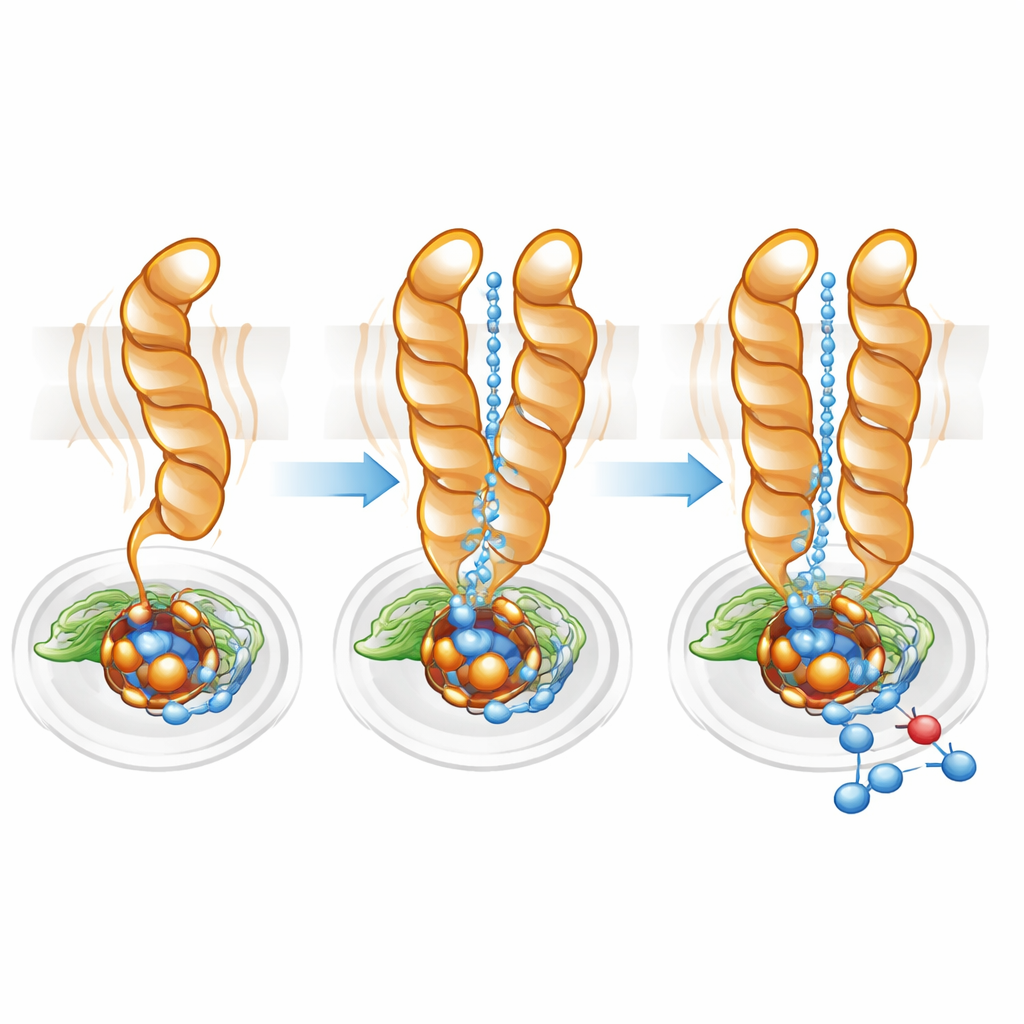
Feinabstimmung der Protonenautobahn
Protonen – positiv geladene Wasserstoffionen – müssen effizient vom Zellinneren zum verborgenen aktiven Zentrum transportiert werden, damit die Reduktion von Stickstoffmonoxid ablaufen kann. Mithilfe von Pfadkartierungssoftware fand das Team eine hydrophile Höhlung, die das Cytoplasma mit dem aktiven Zentrum sowohl im Monomer als auch im Dimer verbindet. Im Monomer war dieser Kanal jedoch breiter und diffuser, was mit der größeren Beweglichkeit von TM10 übereinstimmt. Im Dimer half die verriegelte Position von TM10 und die günstige Orientierung von Glu563, einen direkteren, besser organisierten Pfad zu definieren. Die Mutation von Glu563 in Aminosäuren, die nicht dieselben Wechselwirkungen eingehen können, reduzierte die Enzymaktivität auf unter 10 % des Normalwerts und destabilisierte zudem das Dimer, während Mutationen an verwandten Positionen die Menge des für das aktive Zentrum essentiellen Nicht-Häm-Eisens verringerten. Zusammengenommen zeigen diese Ergebnisse, dass Dimerbildung und die präzise Positionierung von Glu563 und Glu494 eng mit sowohl struktureller Integrität als auch katalytischer Effizienz verknüpft sind.
Von strukturellen Erkenntnissen zu neuen Therapien
Die Befunde legen eine klare Verbindung offen: vom Zusammenklappen der Proteine an der Membranoberfläche bis zu feinen Anpassungen tief im aktiven Zentrum, die steuern, wie effektiv qNOR Stickstoffmonoxid entfernt. Vereinfacht gesagt, wenn sich zwei Enzymkopien zusammenschließen, richten sie ein flexibles Segment auf und versteifen es, sodass Protonen gezielter in das Reaktionszentrum gelenkt werden und die Enzymausbeute steigt. Für die Wirkstoffentwicklung schlägt dies eine unkonventionelle Strategie vor: Statt direkt das aktive Zentrum zu blockieren, könnte man Moleküle entwerfen, die das Dimer auseinanderdrängen oder die Glu563–Glu494-Interaktion stören und das Enzym in seinen langsamen monomeren Zustand zwingen. Da qNOR und verwandte Enzyme für das Überleben mehrerer gefährlicher, medikamentenresistenter Erreger entscheidend sind, könnten solche strukturgeleiteten Ansätze zur nächsten Generation gezielter antimikrobieller Mittel beitragen.
Zitation: Gopalasingam, C.C., Egami, H., Shigematsu, H. et al. Structural basis of Neisseria meningitidis quinol dependent nitric oxide reductase activation by dimerization. Commun Biol 9, 433 (2026). https://doi.org/10.1038/s42003-026-09754-0
Schlüsselwörter: Entgiftung von Stickoxid, bakterielle Atmung, Membranenzyme, Kryo-Elektronenmikroskopie, antimikrobielle Wirkstoffziele