Clear Sky Science · de
Räumliche Multiomik enthüllt immun‑metabolische Eigenschaften des entzündlichen Rands nach irreversibler Elektroporation bei Leberkrebs
Warum eine neue Behandlung von Leberkrebs genauer betrachtet werden muss
Irreversible Elektroporation (IRE) ist eine neuere Methode zur Zerstörung von Lebertumoren, die kurze Hochspannungsimpulse anstelle von Hitze verwendet. Da sie nahe gelegene Blutgefäße und Gallengänge schonen kann, ist sie besonders nützlich bei Tumoren in empfindlichen Lagen. Trotzdem tritt bei bis zu einem Drittel der Patienten der Tumor unmittelbar neben dem behandelten Bereich wieder auf. Diese Studie untersucht, was in dieser schmalen Randzone nach IRE geschieht — und ob verborgene Veränderungen in Immunzellen und im Zellstoffwechsel dort stillschweigend den Nährboden für ein Wiederauftreten des Krebses bereiten könnten.
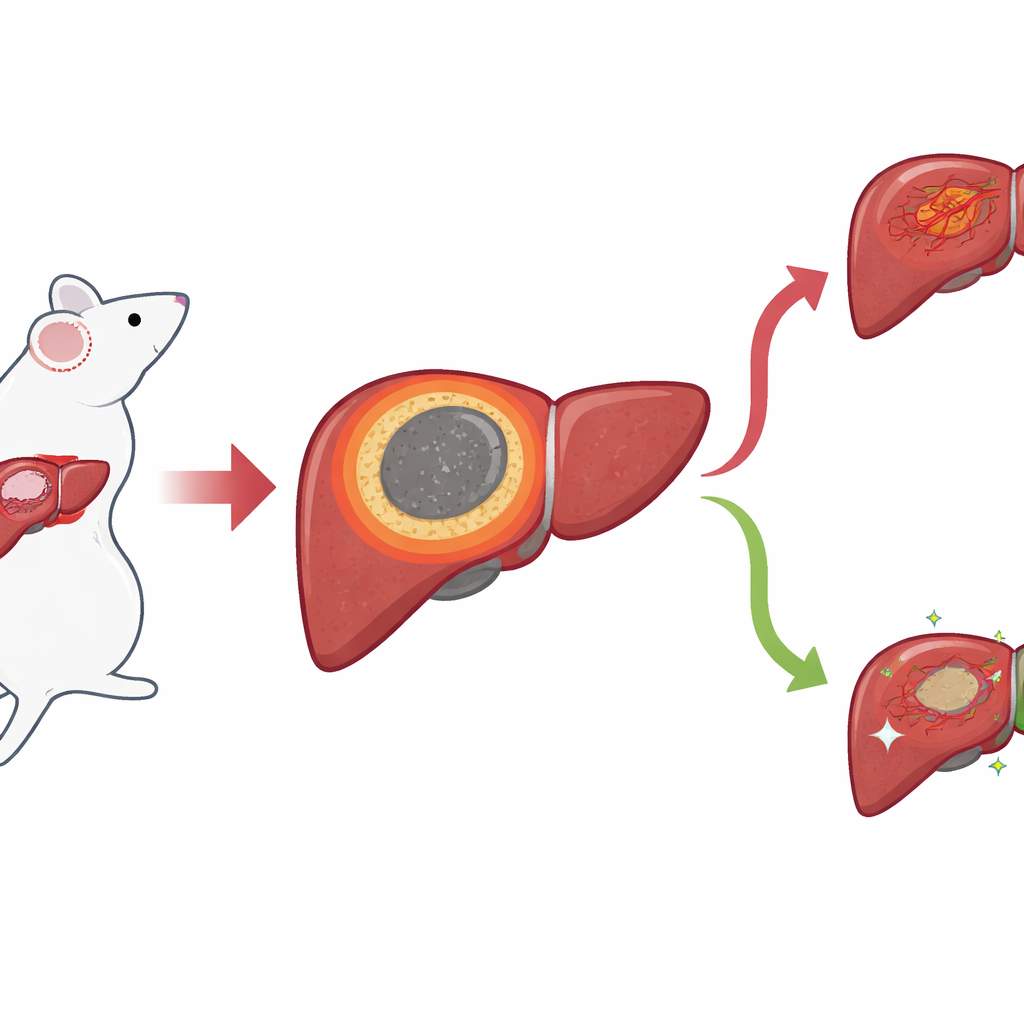
Ein schmaler Rand mit großen Folgen
Anhand eines Mausmodells für Leberkrebs konzentrierten sich die Forschenden auf den dünnen Gewebering, der sich zwischen dem abgestorbenen, ablatieren Zentrum und der umliegenden gesunden Leber nach IRE bildet. Sie bezeichnen diesen Bereich als entzündlichen Rand (inflammatory margin, IM). Standard-Mikroskopaufnahmen zeigten, dass diese Zone genau dort liegt, wo lokale Rezidive typischerweise auftreten, doch waren ihre Grenzen mit bloßem Auge schwer zu fassen. Um ein schärferes Bild zu erhalten, wandte das Team räumliche Methoden an, die erfassen, welche Gene und kleine Moleküle vorhanden sind, während ihre Lage im Gewebe erhalten bleibt. Mit spatialer Transkriptomik kartierten sie die Genaktivität punktgenau und entdeckten einen separaten Cluster von Punkten, der genau mit dem IM zusammenfiel und das nekrotische Zentrum von normaler Leber und Tumorbereichen trennte.
Immunzellen sammeln sich — doch viele bremsen die Attacke
Die Wissenschaftler nutzten anschließend Einzelzell- und Einzelnukleus-RNA-Sequenzierung zusammen mit einer leistungsstarken Profiling-Methode namens CyTOF, um die einzelnen Zelltypen in der Leber zu katalogisieren. Sie fanden heraus, dass der IM von einer Art Immunzellen dominiert wird, die Makrophagen genannt werden. Insbesondere strömte kurz nach IRE eine Untergruppe, die „lipid‑assoziierten Makrophagen“ (LAMs) ähnelte, in den IM ein. Diese Zellen tragen Oberflächenmarker und Gen-Signaturen, die mit Immunsuppression verbunden sind, darunter hohe Werte von PD‑L1, einem Molekül, das die T‑Zell‑Antworten dämpft. Genexpressionsanalysen deuteten darauf hin, dass diese Makrophagen gut darin sind, Material aufzunehmen, auf chemische Lockstoffe zu reagieren und Signale auszusenden, die die T‑Zellen hemmen können, die nötig wären, um Krebszellen zu töten. Bildgebende Verfahren bestätigten, dass PD‑L1‑positive Makrophagen im IM deutlich häufiger vorkamen als im umliegenden normalen Gewebe.
Ein Brennpunkt veränderter Fettchemie
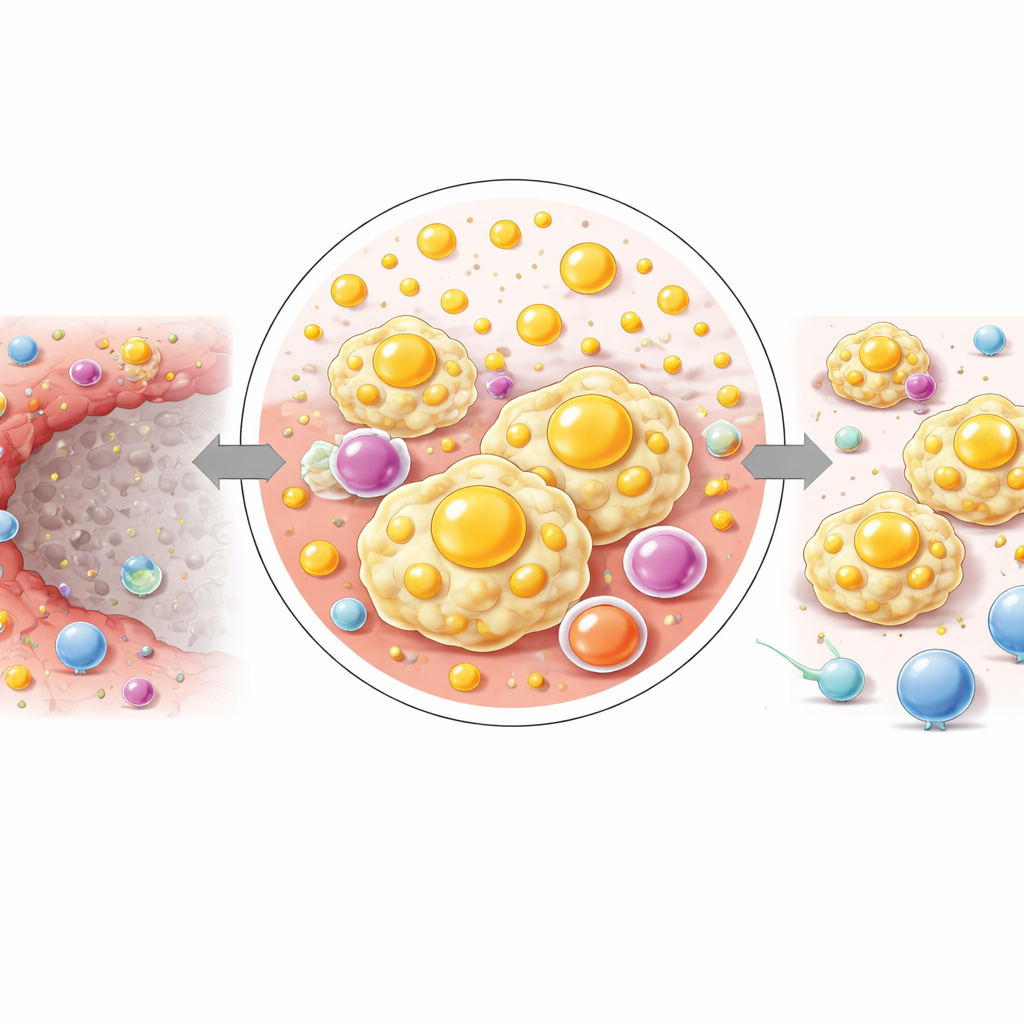
Als Nächstes überlagerten die Forschenden diese Immunlandschaft mit spatialer Metabolomik, einer massenspektrometrischen Bildgebungsmethode, die die Verteilung von Hunderten kleiner Moleküle kartiert. Sie zeigten, dass der IM ein metabolisches Fingerprint besitzt, der weder dem toten Kern noch der umliegenden Leber gleicht. In diesem schmalen Band waren viele Lipid‑(fettbezogene) Stoffwechselwege stark erhöht, darunter die Produktion ungesättigter Fettsäuren, Arachidonsäure‑Derivate und Sphingolipide. Wichtige Signalfette wie Prostaglandine und Leukotriene, die von Arachidonsäure abgeleitet sind, waren im IM angereichert, während andere enzymatische Wege zur Verarbeitung desselben Moleküls relativ gedämpft waren. Eine weitere Lipidfamilie, die Sphingolipide — einschließlich Ceramiden und Sphingomyelinen — akkumulierte ebenfalls, unterstützt durch eine erhöhte Expression der Enzyme, die diese herstellen und umbauen.
Ein schrittweiser Wandel von Schaden zu einer kraftstoffreichen Nische
Durch die Unterteilung des entzündlichen Rands in drei dünne Schichten von der nekrotischen Mitte nach außen beobachteten die Forschenden eine allmähliche chemische Verschiebung. Am nächsten zur toten Zone waren komplexe Lipide und cholesterinähnliche Moleküle am höchsten, weiter außen stiegen kleine energierelevante Moleküle wie Glukose und bestimmte Aminosäuren an. Dieses Muster deutet darauf hin, dass sich das Gewebe über eine kurze Strecke von einer lipidgeladenen, signalreichen Umgebung in eine hin verwandelt, die auf die Energieversorgung von Zellen und deren Wachstum ausgerichtet ist. Die Autoren schlagen vor, dass diese schrittweise Umlenkung dazu beiträgt, die lipidhungrigen, immunsuppressiven Makrophagen im IM zu erhalten und stillschweigend den Boden für eine Wiederetablierung von Tumorzellen vorzubereiten.
Was das für die zukünftige Behandlung von Leberkrebs bedeutet
Einfach gesagt zeigt diese Arbeit, dass IRE mehr bewirkt als nur das Abtöten von Tumorzellen: Sie schafft auch einen schmalen Gewebering, in dem Immunzellen und Fettchemie zusammen ein abgeschirmtes, tumorfreundliches Viertel bilden. Makrophagen in dieser Zone sind zahlreich, mit Lipiden beladen und darauf ausgerichtet, T‑Zellen auszuschalten, anstatt ihnen zu helfen. Da diese Veränderungen eng mit bestimmten Stoffwechselwegen verknüpft sind, eröffnen sie neue therapeutische Ansätze. Die Kombination von IRE mit Wirkstoffen, die den Lipidstoffwechsel angreifen oder PD‑L1 in diesem Randblockieren, könnte theoretisch eine rezidivanfällige Grenze in eine Zone verwandeln, die den Kampf gegen Leberkrebs wirklich abschließt.
Zitation: Liu, J., Guan, S., Sun, Z. et al. Spatial multiomics reveals irreversible electroporation-induced immuno-metabolic characteristics of the inflammatory margin in liver cancer. Commun Biol 9, 458 (2026). https://doi.org/10.1038/s42003-026-09742-4
Schlüsselwörter: Leberkrebs, Tumorablation, Immunmikroumgebung, Makrophagen, Lipidstoffwechsel