Clear Sky Science · de
Oberflächenmodifikation von Bakterien erzeugt robuste lebende Therapeutika zur verbesserten Therapie der Colitis ulcerosa
Freundliche Keime als winzige Leibwächter
Colitis ulcerosa ist eine schmerzhafte Darmerkrankung, bei der der eigene Darm chronisch entzündet ist, was zu heftigem Durchfall, Blutungen und einer stark verminderten Lebensqualität führt. Ärztinnen, Ärzte und Patientinnen, Patienten hoffen auf „gute Bakterien“-Präparate, die diese Entzündung von innen heraus dämpfen könnten, doch die meisten Mikroben sterben auf der harten Reise durch Magen und Dünndarm, bevor sie den Dickdarm erreichen, wo sie gebraucht werden. Die vorliegende Studie beschreibt eine neue Methode, Probiotika mit einer schützenden Hülle auszustatten, damit sie sicher den Verdauungstrakt passieren, sich im Dickdarm ansiedeln und bei der Reparatur des geschädigten Darms helfen können.
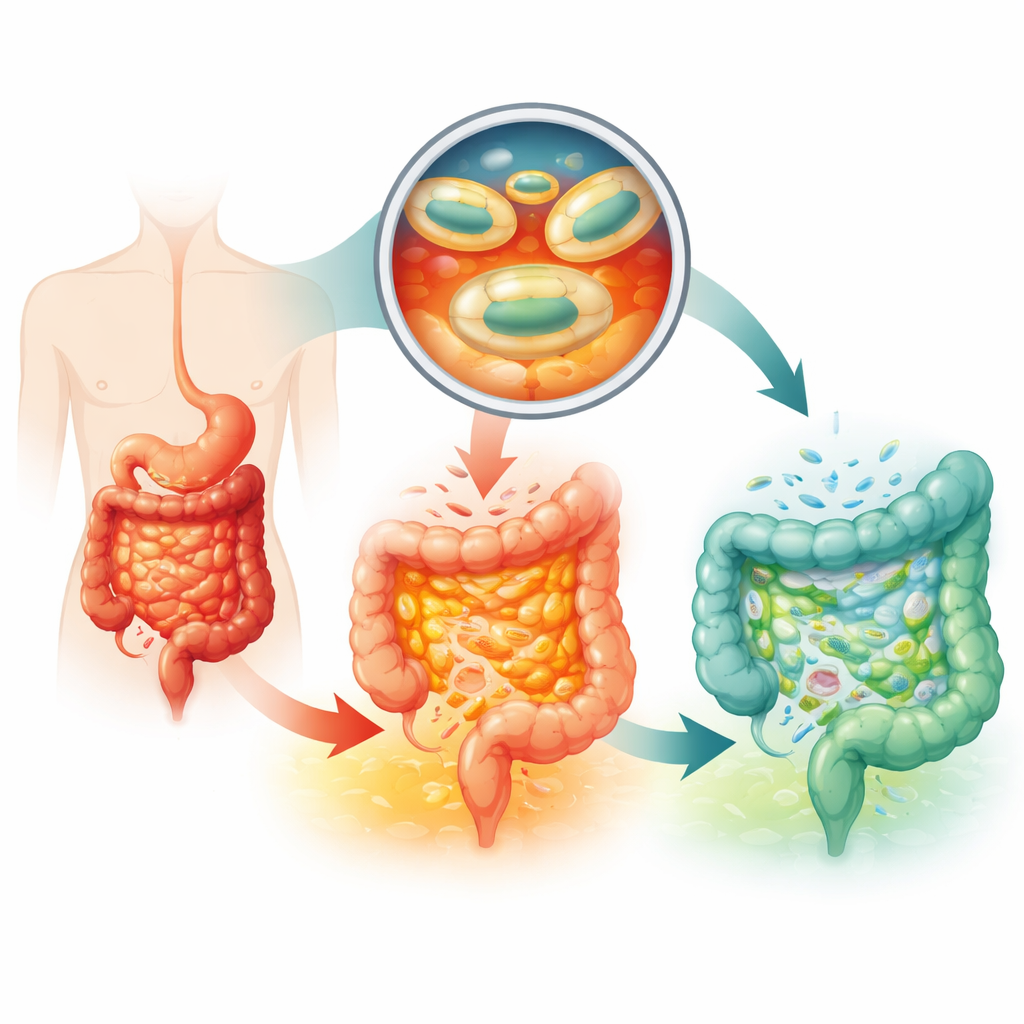
Warum gängige Probiotika oft versagen
Standardbehandlungen der Colitis ulcerosa stützen sich auf entzündungshemmende und immunsuppressive Medikamente, die schwere Nebenwirkungen haben können und nicht bei allen wirken. Probiotika bieten einen schonenderen Ansatz, indem sie das mikrobielle Gleichgewicht im Darm wiederherstellen. Ein spezieller Stamm von Escherichia coli, Nissle 1917, ist bereits als Arzneimittel für diese Erkrankung zugelassen, doch Patientinnen und Patienten müssen sehr hohe Dosen täglich einnehmen, und selbst dann sind die Effekte nur begrenzt. Das Hauptproblem ist Überleben und gezielte Abgabe: Magensäure, Verdauungsenzyme und die schnelle Passage durch den oberen Darmteil töten oder ausgespülen die meisten Bakterien, bevor sie sich im Dickdarm ansiedeln und vermehren können — dort leben normalerweise über 99 % der Darmmikroben.
Eine schützende Hülle um nützliche Bakterien bauen
Um dieses Problem zu lösen, entwickelten die Forschenden eine dünne, intelligente Beschichtung um jede Probiotika-Zelle aus einem pflanzlichen Material namens Lignin. Sie modifizierten das Lignin chemisch, um es besser löslich und empfindlich gegenüber pH-Änderungen zu machen, sodass das Material in starker Säure stabil bleibt, sich aber in der neutraleren Umgebung des Dickdarms auflöst. In einem schonenden Schicht-für-Schicht-Verfahren brachten sie zunächst Calciumionen auf die Bakterienoberfläche auf und umhüllten diese dann mit dem modifizierten Lignin, wodurch eine glatte „Rüstung“ von etwa einem Zehntausendstel Millimeter Dicke entstand. Mikroskopie und Partikelgrößenmessungen zeigten, dass diese Hülle die Bakterien schützte, ohne sie abzutöten. Dieselbe Methode funktionierte bei mehreren sehr unterschiedlichen Bakterienarten, was darauf hindeutet, dass sie als allgemeine Plattform für viele probiotische Therapien dienen könnte.
Gezielte Ablieferung im Dickdarm und Unterstützung der Heilung
In simulierten Verdauungsflüssigkeiten wurden ungeschützte Bakterien schnell von Magensäure zerstört, während die umhüllten Bakterien stundenlang überlebten und ihre Fracht erst bei dickdarmähnlichen pH-Werten effizient freisetzten. Bei Mäusen mit chemisch induzierter Colitis ulcerosa sammelten sich die beschichteten Bakterien stark im Dickdarm an, wohingegen unbeschichtete Bakterien oder einfache Mischungen mit dem Beschichtungsmaterial dies größtenteils nicht schafften. Das Team nutzte Fluoreszenzbildgebung, Gentests und mathematische Modellierung, um zu zeigen, dass die geschützten Bakterien nicht nur unversehrt im Dickdarm ankamen, sondern sich dort auch vermehrten und etwa eins von tausend aller Darmmikroben stellten. Behandelte Mäuse verloren weniger Gewicht, behielten längere Därme und zeigten unter dem Mikroskop deutlich gesünderes Darmgewebe mit dichteren Zellverbindungen und einer wiederhergestellten Schleimschicht — zusammen eine entscheidende Barriere zwischen Körper und Darminhalt.
Beruhigung des Immunsystems und Wiederherstellung des Mikrobioms
Über die physische Reparatur hinaus veränderten die gepanzerten Probiotika das immunologische und mikrobielle Umfeld im kranken Darm. Im Blut und im Dickdarm der erkrankten Mäuse waren Entzündungsmarker erhöht und ein wichtiger anti-entzündlicher Botenstoff vermindert; die neue Behandlung kehrte diese Trends um und verschob das Immunsystem in einen ruhigeren Zustand. Detaillierte Zellanalysen zeigten Veränderungen in der Zusammensetzung der Immunzellen sowohl im Dickdarm als auch in der Milz. Gleichzeitig enthüllte die DNA-Sequenzierung der Darmmikroben, dass die Therapie die mikrobielle Diversität insgesamt erhöhte und mehrere Bakteriengruppen förderte, die mit Darmgesundheit in Verbindung stehen, darunter Akkermansia und Muribaculum. Metabolitprofiling zeigte darüber hinaus weitreichende Veränderungen kleiner Moleküle im Zusammenhang mit Vitamin-, Fettsäure- und Aminosäurestoffwechsel, was darauf hindeutet, dass das neu ausbalancierte Mikrobiom ein chemisches Milieu produziert, das die Heilung begünstigt.
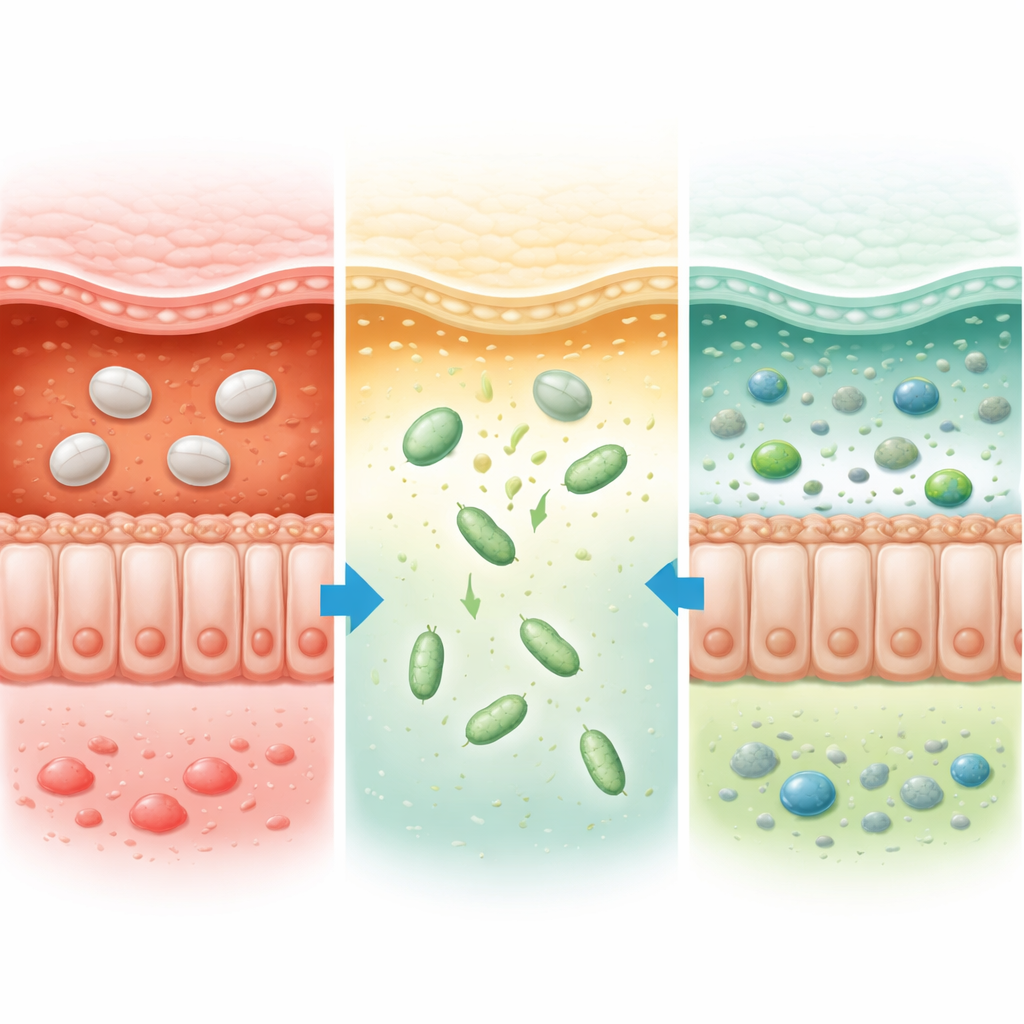
Von der Mausstudie zu künftigen lebenden Arzneimitteln
Insgesamt zeigen die Ergebnisse, dass eine pH-empfindliche Rüstung Probiotika zuverlässig durch das Verdauungsfeuerwerk transportieren und sie dort absetzen kann, wo Colitis ulcerosa den größten Schaden anrichtet. Bei Mäusen ermöglichte diese Strategie, dass deutlich geringere Bakteriendosen den Dickdarm besiedelten, die Darmbarriere repariert, schädliche Entzündungen reduziert und eine gesündere mikrobielle Gemeinschaft sowie ein verbessertes Stoffwechselprofil wiederhergestellt wurden. Da die pflanzliche Beschichtung größtenteils unverändert durch den Körper passiert und die Methode auf viele Bakterientypen anwendbar ist, argumentieren die Autorinnen und Autoren, dass ihr Ansatz einen breit nutzbaren Bauplan zur Entwicklung nächster Generationen „lebender“ Arzneimittel für Colitis ulcerosa und andere Erkrankungen des Dickdarms bietet.
Zitation: Liu, J., Fang, Z., Li, X. et al. Surface decoration of bacteria generates robust living therapeutics for improved ulcerative colitis therapy. Commun Biol 9, 428 (2026). https://doi.org/10.1038/s42003-026-09732-6
Schlüsselwörter: Colitis ulcerosa, Probiotika, Darmmikrobiom, Wirkstofffreisetzung, Darmbarriere