Clear Sky Science · de
Einzelkern-RNA-Sequenzierung und funktionelle Studien zu akut methamphetamin‑induziertem kognitiven Defizit
Warum das für die Gehirngesundheit wichtig ist
Methamphetamin wird oft als Droge dargestellt, die das Gehirn „ausschmort“, aber wie sieht dieser Schaden tatsächlich innerhalb unserer Zellen aus? Diese Studie blickt Zelle für Zelle in das Erinnerungszentrum der Maus — den Hippocampus — und untersucht, wie eine kurzzeitige, intensive Meth‑Exposition die Mechanik stört, die Lernen und Gedächtnis stützt. Indem sie diese Veränderungen in beispielloser Detailtiefe kartiert, weist die Arbeit auf neue biologische Schwachstellen hin, die eines Tages gezielt zum Schutz oder zur Wiederherstellung der Gehirnfunktion bei Betroffenen genutzt werden könnten.
Wie eine Binge‑Dosis Meth das Gedächtnis beeinträchtigt
Die Forscher fragten zunächst eine einfache Frage: Schadet eine intensive, kurzfristige Meth‑Gabe dem Gedächtnis von Mäusen? Die Tiere erhielten vier Injektionen Meth innerhalb eines Tages, was einem Binge‑Muster entspricht. Bei Tests hatten diese Mäuse Schwierigkeiten, neue Objekte zu erkennen, und benötigten länger, um eine versteckte Plattform in einem Wasserlabyrinth zu finden — klassische Anzeichen für Beeinträchtigungen des Lernens und des räumlichen Gedächtnisses. Selbst nachdem die Plattform entfernt wurde, suchten sie weniger an der richtigen Stelle, was darauf hindeutet, dass im Hippocampus — dem Navigations‑ und Gedächtniszentrum des Gehirns — etwas nicht mehr richtig funktioniert.
Jeden Zellkern einzeln betrachten
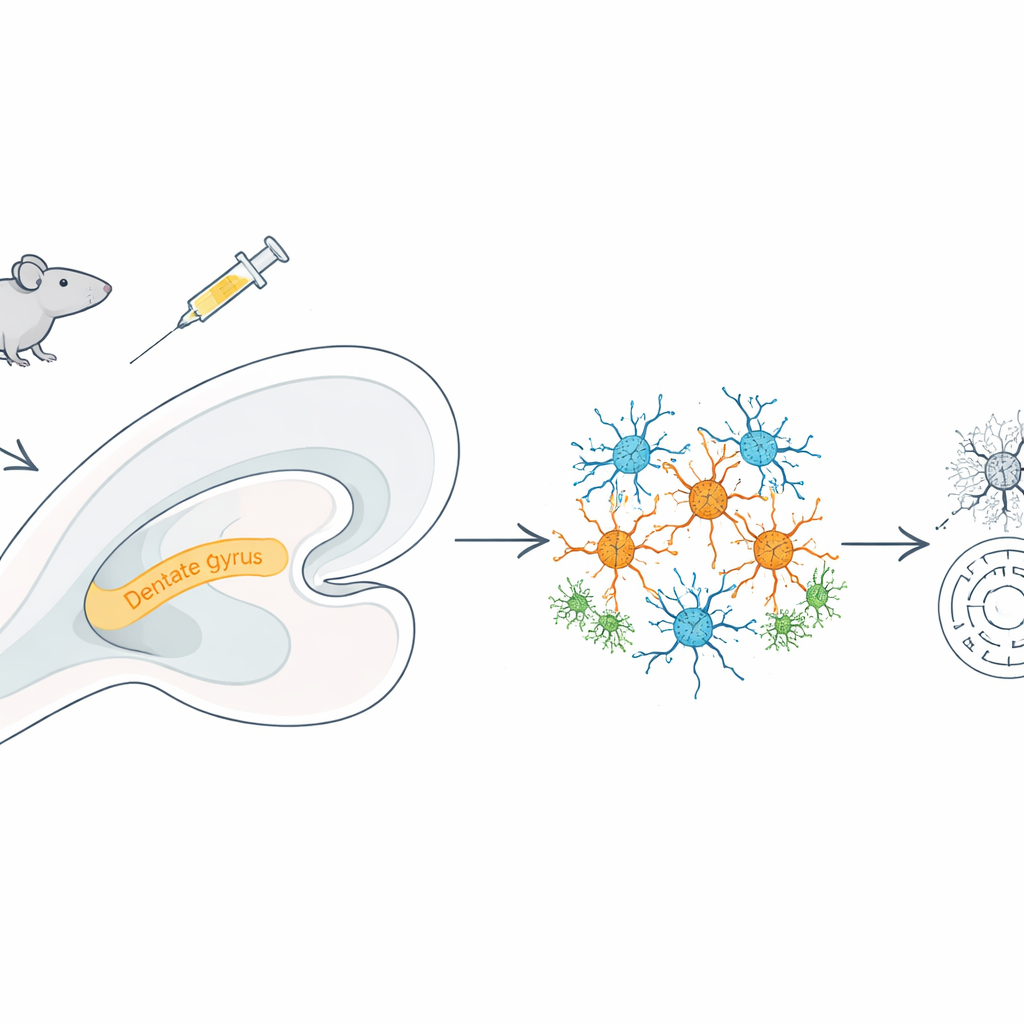
Um zu verstehen, was schieflief, nutzte das Team die Einzelkern‑RNA‑Sequenzierung, eine Methode, die liest, welche Gene in tausenden einzelnen Zellkernen gleichzeitig aktiviert sind. Aus über 36.000 hippocampalen Kernen identifizierten sie zehn Hauptzelltypen, darunter exzitatorische und inhibitorische Neurone, Astrozyten, Mikroglia, Oligodendrozyten und Gefäßzellen. Die Meth‑Exposition veränderte diese zelluläre Zusammensetzung: Es gab mehr exzitatorische Neurone, Mikroglia, Oligodendrozyten und Endothelzellen, aber weniger inhibitorische Neurone. Das verschob das Gleichgewicht in Richtung Erregung — ein Zustand, der neuronale Schaltkreise anfälliger für Stress und Schäden machen kann.
Energiezentralen unter Stress und schwindende Abwehr
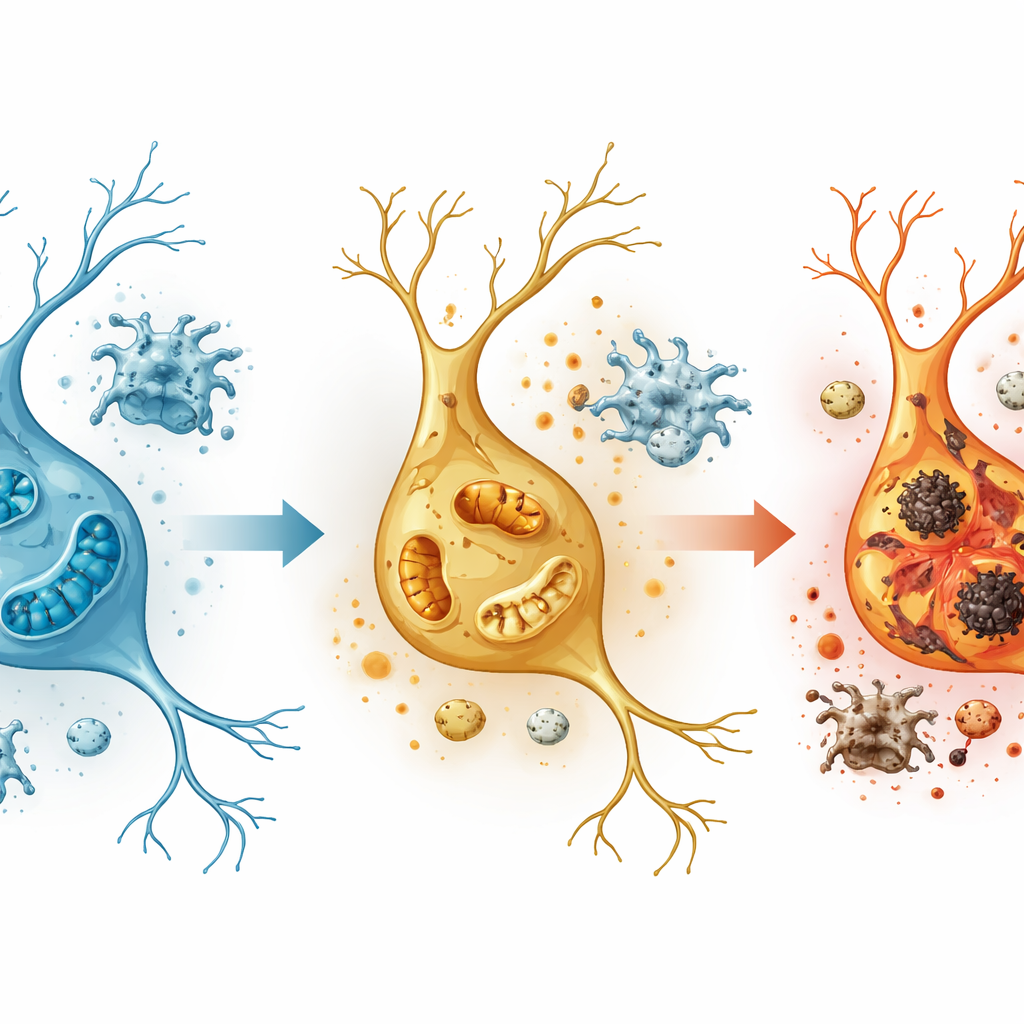
Die dramatischsten Genveränderungen traten in exzitatorischen Neuronen auf, insbesondere in einer Hippocampus‑Region namens Gyrus dentatus, die für die Bildung unterscheidbarer Erinnerungen entscheidend ist. Hier waren Gene, die mit der oxidativen Phosphorylierung — dem Prozess, durch den Mitochondrien zelluläre Energie erzeugen — verbunden sind, stark verändert, und Elektronenmikroskop‑Aufnahmen zeigten fragmentierte Mitochondrien mit zerstörter innerer Struktur. Gleichzeitig waren Signalwege aktiviert, die mit reaktiven Sauerstoffspezies und Entzündungsreaktionen verbunden sind, und eine Organellenklasse, die Peroxisomen, die bei der Kontrolle schädlicher Stoffwechselnebenprodukte hilft, zeigte Anzeichen des Versagens. Wichtige peroxisomenbezogene Gene, darunter PEX5, wiesen eine verringerte Aktivität auf, während Gene, die Entzündung und oxidativen Stress antreiben, zunahmen — was darauf hindeutet, dass Meth Neurone in eine Energiekrise treibt und gleichzeitig ihre natürlichen Entgiftungssysteme schwächt.
Verwundbare Zellgruppen und gestörte Zell‑zu‑Zell‑Kommunikation
Bei genauerer Untersuchung teilten die Forscher die exzitatorischen Neurone in fünf regionale Subtypen, wobei Zellen des Gyrus dentatus die stärksten Stresssignale zeigten: verstärkte Entzündungsreaktionen, erhöhte oxidative Belastung und eine Form des inflammatorischen Zelltods, die als Pyroptose bekannt ist. Innerhalb dieser Region identifizierten sie eine Untergruppe exzitatorischer Neurone, die bei methbehandelten Tieren stark angereichert war und die stärksten Schadenssignaturen trug — sie wurden somit als wahrscheinliche Opfer der Exposition markiert. Im gesamten Hippocampus intensivierte sich die Kommunikation zwischen exzitatorischen Neuronen und anderen Zelltypen, während Verbindungen von inhibitorischen Neuronen abgeschwächt wurden. Mikroglia, die Immunwächter des Gehirns, schalteten in einen hochentzündlichen Zustand um. Gleichzeitig verfolgte das Team Gencluster, deren Aktivität eng mit der Gedächtnisleistung verknüpft war, und hob Netzwerke in exzitatorischen Neuronen, inhibitorischen Neuronen, Astrozyten und Oligodendrozyten hervor, die den kognitiven Abbau verschlechtern oder abmildern könnten.
Neue molekulare Hinweise und mögliche neuroprotektive Ansätze
Die Studie hob auch spezifische Moleküle hervor, die zentrale Knotenpunkte der Meth‑verursachten Schädigung sein könnten. Ein RNA‑verarbeitendes Protein namens Ddx5 war in vielen Zelltypen stark erhöht, insbesondere im Gyrus dentatus, was auf eine breite Stressantwort hindeutet, deren schützende oder schädliche Rolle noch geklärt werden muss. Im Gegensatz dazu waren PEX5 und der Lipid‑regulierende Schalter PPARα — beide wichtig für das Gleichgewicht von Peroxisomen und Mitochondrien — in exzitatorischen Neuronen herunterreguliert. Zusammengenommen deuten diese Veränderungen darauf hin, dass die Wiederherstellung des Energiestoffwechsels, die Stärkung der Peroxisomenfunktion und die Beruhigung überaktiver Immunantworten vielversprechende Strategien sein könnten, um Hirnschäden nach akuter Meth‑Exposition zu begrenzen.
Was das in einfachen Worten bedeutet
Einfach ausgedrückt zeigt diese Arbeit, dass schon ein kurzlebiger Meth‑Binge im Erinnerungszentrum des Gehirns nachhaltige Spuren hinterlassen kann. Er versetzt Schlüsselneurone im Gyrus dentatus in einen Energiemangel, überlastet sie mit toxischen Nebenprodukten, schwächt ihre Reinigungsmechanismen und aktiviert benachbarte Immunzellen, die das Gewebe weiter entzünden. Indem die Studie genau kartiert, welche Zelltypen, Regionen und Gennetzwerke am stärksten betroffen sind, geht sie über die vage Vorstellung von „Gehirnschaden“ hinaus und identifiziert konkrete biologische Prozesse — etwa fehlerhafte Energieproduktion und gestörte Entgiftungswege —, die gezielt angegangen werden könnten, um das Gehirn bei von Meth Geschädigten zu schützen oder zu reparieren.
Zitation: An, D., Lu, F., Wang, Y. et al. Single-nucleus RNA sequencing and functional studies of acute methamphetamine-induced cognitive impairment. Commun Biol 9, 440 (2026). https://doi.org/10.1038/s42003-026-09728-2
Schlüsselwörter: Methamphetamin, Hippocampus, Einzelkern‑RNA‑Sequenzierung, Mitochondriale Dysfunktion, Neuroinflammation