Clear Sky Science · de
NRF2-Aktivatoren und der Inhibitor des nukleären Exports, Selinexor, begrenzen Coronaviren durch Zielsteuerung eines Netzwerks mit ACE2, TMPRSS2 und XPO1 über einen NRF2-unabhängigen Mechanismus
Medikamente, die Zellen helfen, „Nein“ zu Coronaviren zu sagen
Die meisten heutigen Coronavirus-Behandlungen zielen direkt auf das Virus. Viren sind jedoch Meister der Veränderung, und neue Varianten können solche Medikamente rasch abschwächen. Diese Studie verfolgt eine andere Strategie: sie macht unsere eigenen Zellen weniger einladend für sowohl gefährliche Coronaviren wie SARS-CoV-2 als auch für mildere saisonale Stämme. Indem die Forscher die Handhabung einiger weniger Schlüsselproteine in den Zellen veränderten, zeigen sie, dass bereits verfügbare kleine Moleküle die Infektion in Labor‑Modellen stark reduzieren können — und das auf eine Weise, die nicht auf dem für diese Substanzen bekannten antiviralen Weg beruht.
Ein neuer Blickwinkel auf den Coronavirus-Schutz
Das Team konzentrierte sich auf Verbindungen, die für die Aktivierung eines zellulären Schutzprogramms bekannt sind, das von einem Protein namens NRF2 gesteuert wird. Diese Verbindungen — 4‑Octylitaconat (4OI), Bardoxolon (BARD) und Sulforaphan (SFN) — wurden zusammen mit Selinexor (SEL) getestet, einem Wirkstoff, der ein Transportprotein namens XPO1 blockiert, das andere Proteine aus dem Zellkern hinausbefördert. In Lungen‑ und Nierenzellmodellen reduzierten alle vier Wirkstoffe die SARS‑CoV‑2‑Mengen, ohne die Zellen zu schädigen. Sie wirkten außerdem gegen mehrere besorgniserregende Varianten. Überraschenderweise replizierten die Viren bei genetischem Verlust von NRF2 sogar besser, was beweist, dass NRF2 natürlicherweise schützend wirkt — doch die Wirkstoffe blieben wirksam, was zeigt, dass ihre antivirale Kraft über einen anderen Weg vermittelt wird. 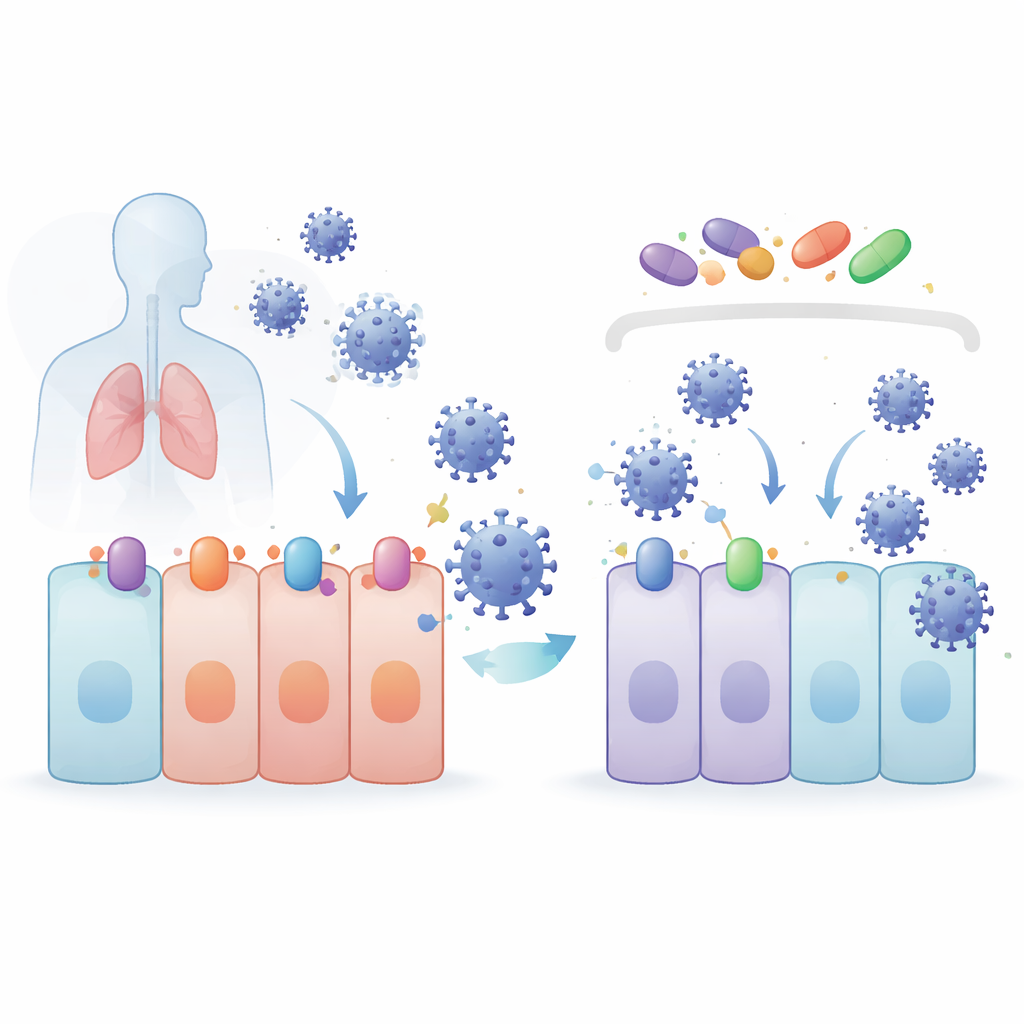
Die virale Haustür verriegeln
Coronaviren beginnen die Infektion, indem sie an Rezeptorproteine an der Zelloberfläche andocken. Bei SARS‑CoV‑2 und seinen nahen Verwandten ist die Haupttür ACE2, unterstützt von einem schneidenden Enzym namens TMPRSS2. Auch das Exportprotein XPO1 scheint die Infektion zu fördern. Die Forscher fanden heraus, dass 4OI, BARD, SFN und SEL in menschlichen Lungenzellen die Mengen an ACE2, TMPRSS2 und XPO1 alle verringerten. 4OI und SEL waren besonders wirkstark, wenn sie vor der Infektion gegeben wurden, und sie verhinderten das Eindringen von virusähnlichen Partikeln, die mit Coronavirus‑Spike‑Proteinen beschichtet waren. Mit anderen Worten: Diese Wirkstoffe verlangsamen das Virus nicht nur nachdem es eingedrungen ist — sie entfernen die Schlösser und Griffe, die das Virus braucht, um die Tür überhaupt zu öffnen.
Wie Zellen wichtige virale Helfer demontieren
Bei tiefergehenden Untersuchungen zeigten die Autoren, dass 4OI den Abbau des ACE2‑Proteins beschleunigt. Unter normalen Bedingungen hält sich ACE2 viele Stunden; mit 4OI verschwand es von der Zelloberfläche in einem Bruchteil dieser Zeit. Diese Zerstörung erforderte zwei zelluläre Markierer, NEDD4L und MDM2, die molekulare „entsorg mich“-Flaggen an Proteine anheften. Die Blockade dieser Markierer schwächte die Fähigkeit von 4OI, ACE2 zu eliminieren. Überraschenderweise war die übliche Protein‑Abbaueinheit, das Proteasom, nicht der Hauptweg. Stattdessen wurde ACE2 in das Recycling‑ und Entsorgungssystem der Zelle, die Lysosomen, geleitet. Die Wirkstoffe senkten außerdem die Genaktivität für ACE2 und XPO1, zum Teil indem sie die Aktivierung von STAT3 reduzierten — ein Protein, das normalerweise die ACE2‑Genablesung fördert. 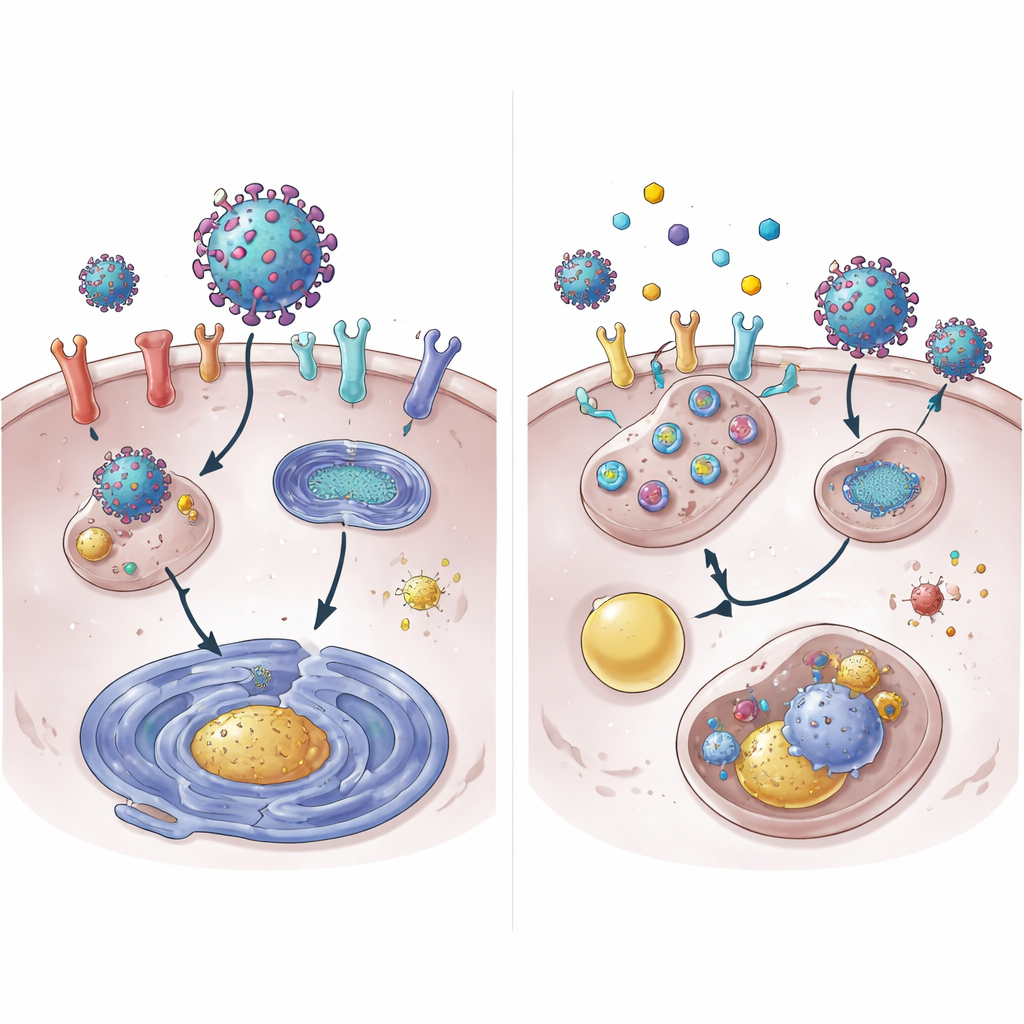
Saisonale Coronaviren und die XPO1‑Verbindung
Die Wissenschaftler wandten sich anschließend hCoV‑229E zu, einem saisonalen Coronavirus, das meist harmlose Erkältungen verursacht, aber bei Menschen mit geschwächtem Immunsystem gefährlich werden kann. Mit gentechnisch veränderten Viren, die bei Replikation leuchten, zeigten sie, dass alle vier Verbindungen 229E in Lungen‑ und Gefäßzellen stark unterdrückten — selbst ohne NRF2. Anders als SARS‑CoV‑2 nutzt dieses Virus einen anderen Rezeptor, ANPEP, den die Wirkstoffe nicht veränderten. Stattdessen korrelierte ihre Wirkung eng damit, wie stark sie XPO1 reduzierten. Die Herunterregulierung von XPO1 selbst verringerte die 229E‑Replikation deutlich, und die Wirkung von Selinexor verschwand nahezu in Zellen mit wenig XPO1. Diese Rangfolge — SEL am stärksten von XPO1 abhängig, BARD am wenigsten — deutet darauf hin, dass jede Verbindung ein leicht unterschiedliches Zielprofil hat, wobei XPO1 ein zentraler Knoten vieler ihrer antiviralen Effekte ist.
Was das für künftige Behandlungen bedeuten könnte
Für Nicht‑Fachleute ist die zentrale Botschaft: Es ist möglich, Coronaviren nicht nur durch direkten Angriff auf das Virus zu bekämpfen, sondern die eigenen Zellen so umzubauen, dass sie weniger anfällig für Infektionen sind. In im Labor gezüchteten menschlichen Zellen entfernten die untersuchten Verbindungen wichtige Andockstellen und Hilfswege, auf die SARS‑CoV‑2 und ein gewöhnliches Erkältungsvirus angewiesen sind — und das größtenteils ohne den NRF2‑Weg, der sie ursprünglich interessant machte. Obwohl diese Ergebnisse noch präklinisch sind und sich nicht direkt in Medikamente übertragen lassen, weisen sie auf einen vielversprechenden Pfad hin: Wirkstoffe, die gleichzeitig den Viruseintritt verringern, schädliche Entzündungen dämpfen und Gewebe schützen, indem sie ein gemeinsames Netzwerk von Wirtsproteinen wie ACE2, TMPRSS2 und XPO1 anvisieren.
Zitation: Waqas, F.H., Silva da Costa, L., Zapatero-Belinchón, F.J. et al. NRF2 activators and the inhibitor of nuclear export, selinexor, restrict coronaviruses by targeting a network involving ACE2, TMPRSS2, and XPO1 through an NRF2-independent mechanism. Commun Biol 9, 384 (2026). https://doi.org/10.1038/s42003-026-09724-6
Schlüsselwörter: wirtsgerichtete antivirale Mittel, Coronavirus-Eintritt, ACE2 und TMPRSS2, NRF2-Aktivatoren, XPO1-Hemmung