Clear Sky Science · de
Ultraschnelle und spezifische miRNA-Quantifizierung mittels Einzelmolekül-Fluoreszenzlöschungs‑Kinetik
Warum schnelle Krankheitstests wichtig sind
Die Diagnose von Krankheiten wie Krebs oder Virusinfektionen hängt oft davon ab, winzige Spuren genetischen Materials im Blut oder anderen Körperflüssigkeiten zu erkennen. Die heutigen Referenztests sind zwar meist sehr genau, können aber langsam, kostspielig sein oder Schwierigkeiten haben, sehr seltene Signale nachzuweisen. Diese Studie stellt eine neue mikroskopbasierte Methode vor, genannt Q‑FISH, die diese genetischen Hinweise in weniger als einer Sekunde auslesen kann. Würde man sie in klinische Werkzeuge überführen, könnten solche Geschwindigkeit und Präzision das frühere Erkennen von Krankheiten, die Verfolgung von Therapieansprechen und die individuelle Anpassung der Behandlung erleichtern.
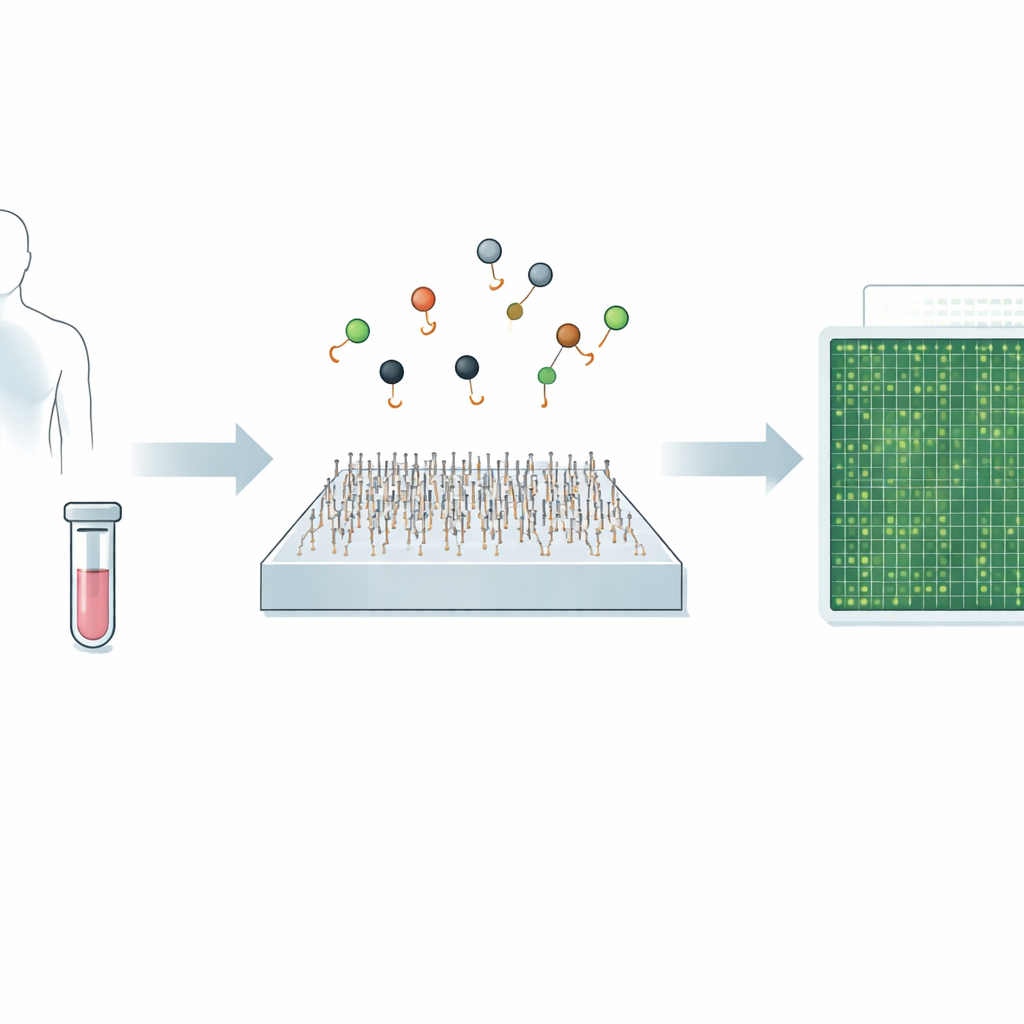
Ein neuer Weg, winzige genetische Botschaften zu sehen
Die Arbeit konzentriert sich auf microRNAs – kurze RNA-Abschnitte, die steuern, wie Gene genutzt werden, und die stark mit vielen Krebsarten, Herzkrankheiten, Infektionen und neurologischen Erkrankungen verknüpft sind. Da microRNAs sehr klein sind und sich oft nur um ein oder zwei Bausteine unterscheiden, haben Standardmethoden wie PCR und Next‑Generation‑Sequencing Schwierigkeiten, eng verwandte Typen auseinanderzuhalten, besonders wenn sie in sehr geringen Mengen vorliegen. Jüngste Einzelmolekül‑Bildgebungsansätze verbesserten diese Spezifität, indem sie verfolgten, wie einzelne Sonden binden und wieder ablösen, blieben aber relativ langsam und benötigten etwa zehn Minuten, um ein einzelnes Ziel zu analysieren.
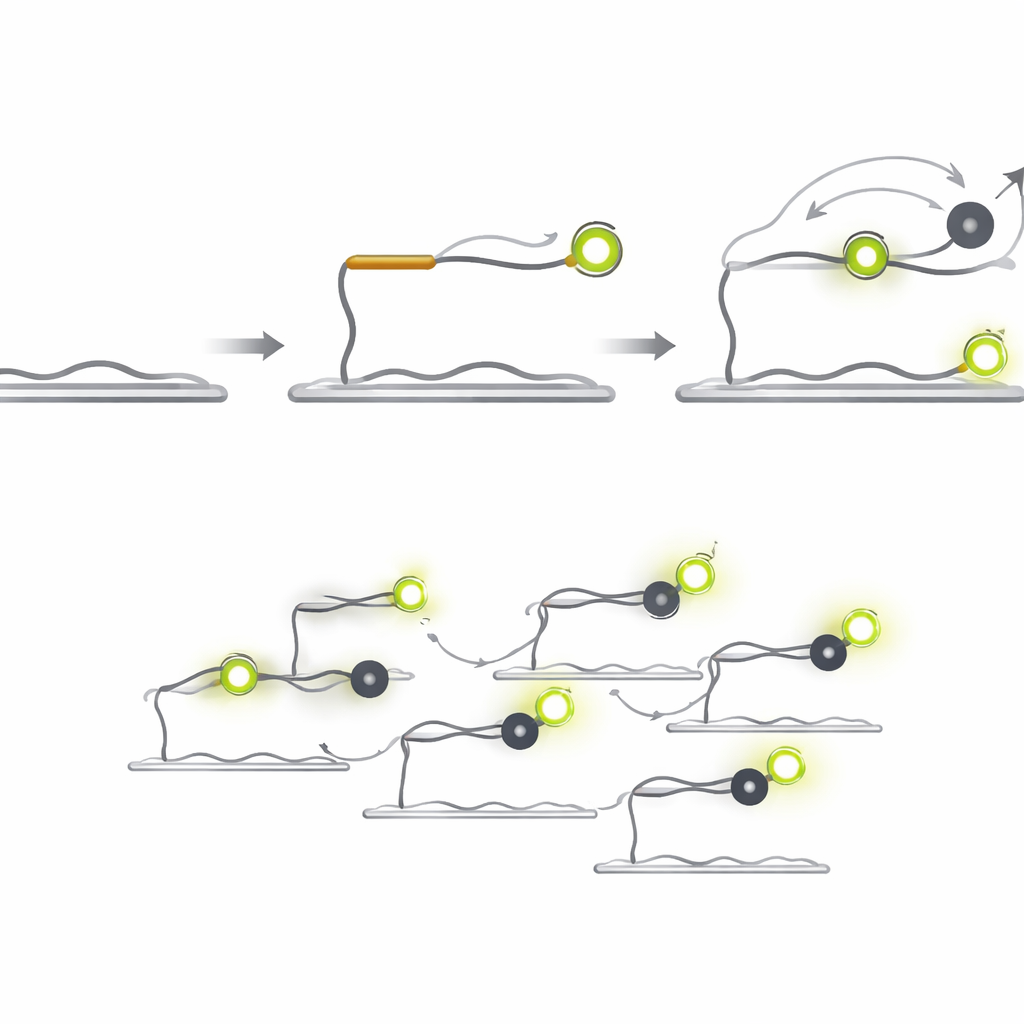
Die Zielsuche durch Lichtflackern
Q‑FISH dreht das Problem um, indem es die kurzen Lichtflacker einzelner Moleküle ausnutzt. Die Methode verwendet zwei kurze DNA-Sonden, die benachbarte Stellen einer Ziel‑microRNA erkennen. Eine Sonde trägt einen fluoreszierenden Farbstoff, der unter Laserlicht leuchtet, die andere einen „Quencher“, der das Licht absorbiert, wenn er nahekommt. Die fluoreszierende Sonde bindet an das Ziel und verharrt lange genug, um sichtbar zu sein, während die Quencher-Sonde so entworfen ist, dass sie schnell bindet und wieder ablöst. Jedes Mal, wenn der Quencher neben dem Farbstoff landet, fällt das Licht plötzlich ab; wenn er sich löst, springt die Helligkeit wieder hoch. Durch Aufzeichnen dieser raschen Ein‑Aus‑Blitze einzelner Moleküle und die Analyse der Dauer der hellen und dunklen Perioden kann das System entscheiden, ob ein echtes Ziel vorhanden ist.
Von Minuten zu Millisekunden
Da die Quencher‑Sonde selbst kein Licht aussendet, kann sie in viel höheren Konzentrationen als fluoreszierende Sonden eingesetzt werden, ohne störenden Hintergrund zu erzeugen. Eine Verkürzung der Quencher‑Sonde erhöht die Geschwindigkeit ihres Ablösens, und eine Erhöhung ihrer Konzentration steigert die Häufigkeit ihres Andockens. Zusammen führen diese Designentscheidungen zu einem dramatischen Geschwindigkeitssprung. In Tests mit einer krebsrelevanten microRNA namens let‑7a erreichte Q‑FISH mehr als 70 % seiner maximalen Nachweiseffizienz bereits nach nur einer Sekunde Beobachtungszeit. Vergleichbare Einzelmolekülmethoden benötigten dafür Dutzende bis Hunderte von Sekunden, wodurch Q‑FISH praktisch über 600‑mal schneller ist.
Nahezu identische Signale trennen und reale Proben messen
Die Forschenden zeigten außerdem, dass Q‑FISH zwischen mehreren Mitgliedern der let‑7‑microRNA‑Familie unterscheiden kann, die nahezu dieselbe Sequenz teilen, aber unterschiedliche Rollen bei der Kontrolle krebsspezifischer Gene haben. Sie nutzten zwei Multiplexierungsstrategien. In der einen wurden unterschiedliche Quencher‑Sonden nacheinander eingeführt, jeweils auf eine leicht verschobene microRNA abgestimmt; in der anderen wurden die Sonden mit verschiedenen Farben markiert und gleichzeitig abgebildet. In beiden Fällen erlaubte das Auslesen der Blinkmuster dem Team, innerhalb von etwa einer Sekunde korrekt zu bestimmen, welche microRNA vorlag. Schließlich wandten sie die Methode auf Gesamt‑RNA an, die aus menschlichem Leber‑ und Lungengewebe extrahiert wurde. Durch Zugabe bekannter Mengen synthetischer microRNAs und das Zählen der resultierenden Spots bauten sie Kalibrationskurven auf und bestimmten dann die natürlichen Gehalte in den Geweben, wobei klare Unterschiede zwischen den Organen sichtbar wurden.
Was das für zukünftige Tests bedeuten könnte
In der Summe zeigt die Studie, dass Q‑FISH spezifische microRNAs mit sehr hoher Genauigkeit herausfinden kann, selbst wenn diese sich fast nicht voneinander unterscheiden, und das in Geschwindigkeiten, die frühere Einzelmolekülmethoden deutlich übertreffen. Obwohl die Experimente an aufbereiteten Proben mit einem spezialisierten Mikroskop durchgeführt wurden, könnte die zugrunde liegende Idee – schnelle Lichtlöschereignisse statt nur langsamer Bindungsereignisse zu nutzen – auf viele Arten genetischer Marker übertragbar sein, einschließlich tumorassoziierter DNA‑Fragmente im Blut. Mit weiterer Technikentwicklung und vereinfachter Probenvorbereitung könnte dieser Ansatz dazu beitragen, schnelle, hochgradig multiplexe und extrem empfindliche molekulare Diagnostik näher an die klinische Routine zu bringen.
Zitation: Kim, J., Hohng, S. Ultrafast and specific miRNA quantification via single-molecule fluorescence quenching kinetics. Commun Biol 9, 432 (2026). https://doi.org/10.1038/s42003-026-09714-8
Schlüsselwörter: mikroRNA-Nachweis, Einzelmolekül-Bildgebung, molekulare Diagnostik, Fluoreszenzlöschung, Liquid Biopsy