Clear Sky Science · de
Eine zweistufige, von Aktin vermittelte Strategie ermöglicht es Campylobacter jejuni, mitochondriale Aggregation und Eisenhomöostase zu fördern, für intrazelluläres Überleben und Persistenz
Warum dieser kleine Kampf innerhalb von Zellen wichtig ist
Lebensmittelvergiftungen durch nicht durchgegartes Hähnchen werden häufig auf das Bakterium Campylobacter jejuni zurückgeführt. Die meisten Menschen erholen sich, doch dieses Mikroorganismus ist überraschend widerstandsfähig in vielen Umgebungen, was seine Verbreitung „vom Hof bis zur Gabel“ erleichtert. Diese Studie untersucht, was passiert, wenn das Bakterium sich in einer frei lebenden Amöbe – einem verbreiteten Süßwassermikroben – versteckt, und enthüllt einen überraschend raffinierten Überlebenstrick: Es dreht sich um die Umgestaltung des inneren Gerüsts der Zelle, das Zusammenballen der energieerzeugenden „Kraftwerke“ namens Mitochondrien und die Kontrolle von Eisen sowie reaktiver Sauerstoffchemie. Das Verständnis dieser verborgenen Phase seines Lebenszyklus könnte auf neue Wege hinweisen, Kontaminationen zu verringern, bevor das Bakterium überhaupt Menschen erreicht.
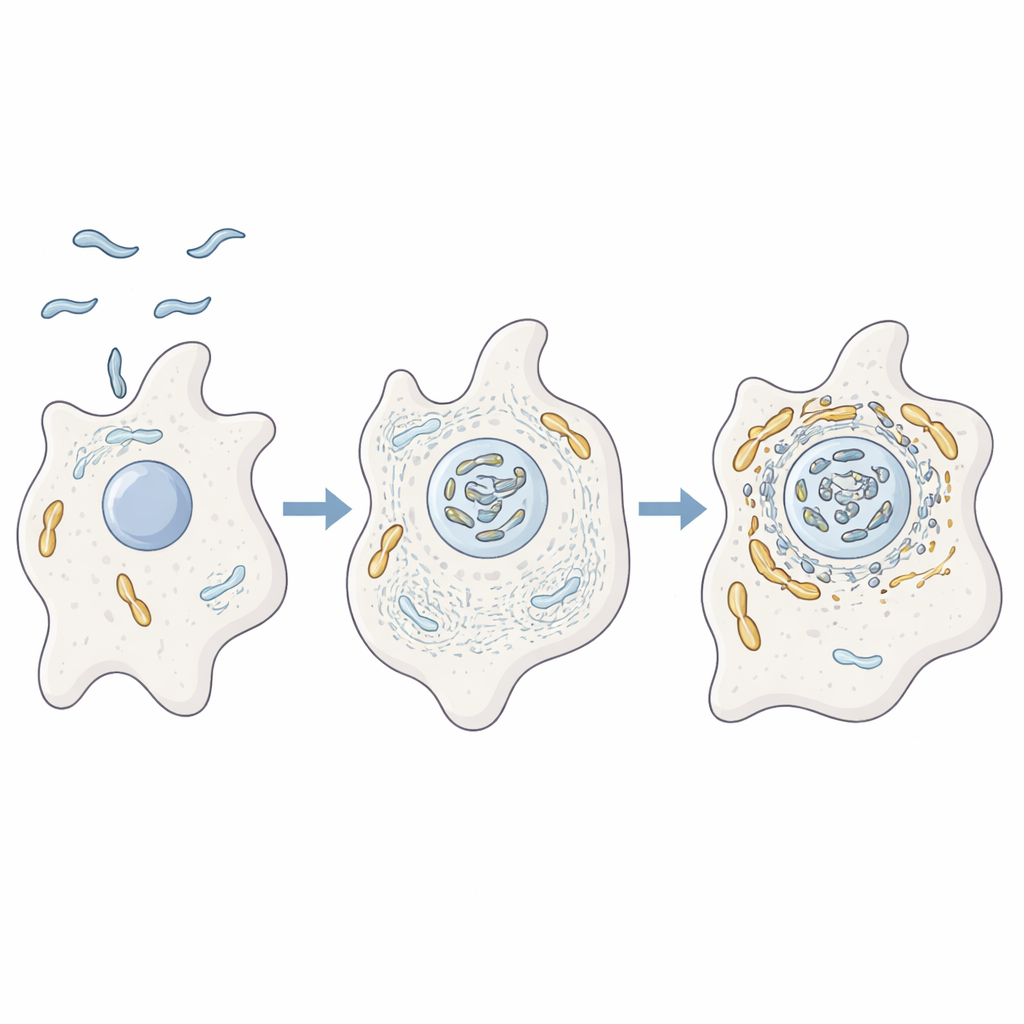
Ein Mikroorganismus, der in Amöben trainiert
Die Autoren untersuchten, wie sich C. jejuni in der Amöbe Acanthamoeba castellanii verhält, einem einzelligen Organismus, der in Boden und Wasser vorkommt. Diese Amöben dienen vielen krankheitserregenden Bakterien als Trainingsgelände, indem sie Schutz vor rauen Bedingungen und Desinfektionsmitteln bieten. Mithilfe fortschrittlicher Proteinanalyse, Mikroskopie und genetischer Mutanten zeigten die Forschenden, dass C. jejuni, wenn es Amöben infiziert, in enger Assoziation mit den Mitochondrien des Wirts endet. Gleichzeitig reichert sich das aus Aktin bestehende innere Gerüst der Amöbe sowie Proteine, die Form und Bewegung regulieren, stark in der Nähe dieser Mitochondrien an, was darauf hindeutet, dass das Bakterium aktiv die innere Zellarchitektur umgestaltet.
Das Gerüst der Zelle biegen, um Kraftwerke zu bewegen
Um zu prüfen, ob Aktin diese Interaktion tatsächlich antreibt, blockierte das Team die Bildung von Aktinfilamenten oder deren Verzweigung zu Netzwerken. Unter diesen Bedingungen sammelten sich die Mitochondrien nicht mehr in der Nähe der Bakterien, sondern blieben als verstreute Punkte, und das Überleben des Bakteriums sank. Anschließend konzentrierten sie sich auf zwei bakterielle Hilfsproteine, CiaD und CiaI, die durch das Flagellum des Bakteriums, einen peitschenartigen Schwanz, in Wirtszellen injiziert werden. CiaD erwies sich als Förderer von Aktinwachstum und begünstigte stachelige Projektionen an der Amöbenoberfläche, die der Zelle beim Aufnehmen der Bakterien halfen. Einmal im Inneren wurden Mitochondrien beobachtet, die sich in abhängiger Weise vom Aktin um das bakterielle Kompartment herum sammelten und dem Bakterium so eine privilegierte Zone mit reicher Wirtsenergieausstattung verschafften.
Ein molekularer Schalter, der Mitochondrien umgestaltet
Während CiaD für das Eindringen entscheidend ist, steuert CiaI das, was danach geschieht. Wenn die Forschenden das Gen für CiaI löschten, löste C. jejuni keine starke mitochondriale Aggregation mehr aus und überlebte in Amöben schlecht. Das Anbringen von gereinigtem CiaI an winzigen Kügelchen, ohne lebende Bakterien, reichte aus, um nahe Mitochondrien zur Fusion und Aggregation zu veranlassen und lokal Aktin zu entfernen. Biochemische Tests zeigten, dass CiaI energietragende Moleküle kooperativ bindet und sich wie ein molekularer Schalter verhält, der seine Aktivität je nach Bedingungen im Wirt an- oder ausschalten könnte. Die Autoren schlagen vor, dass nach dem durch CiaD ausgelösten Aktinwachstum, das Mitochondrien heranzieht, CiaI den lokalen Aktinabbau vorantreibt und das mitochondriale Netzwerk in dichte Aggregate umformt, die das bakterienhaltige Kompartment umschließen.
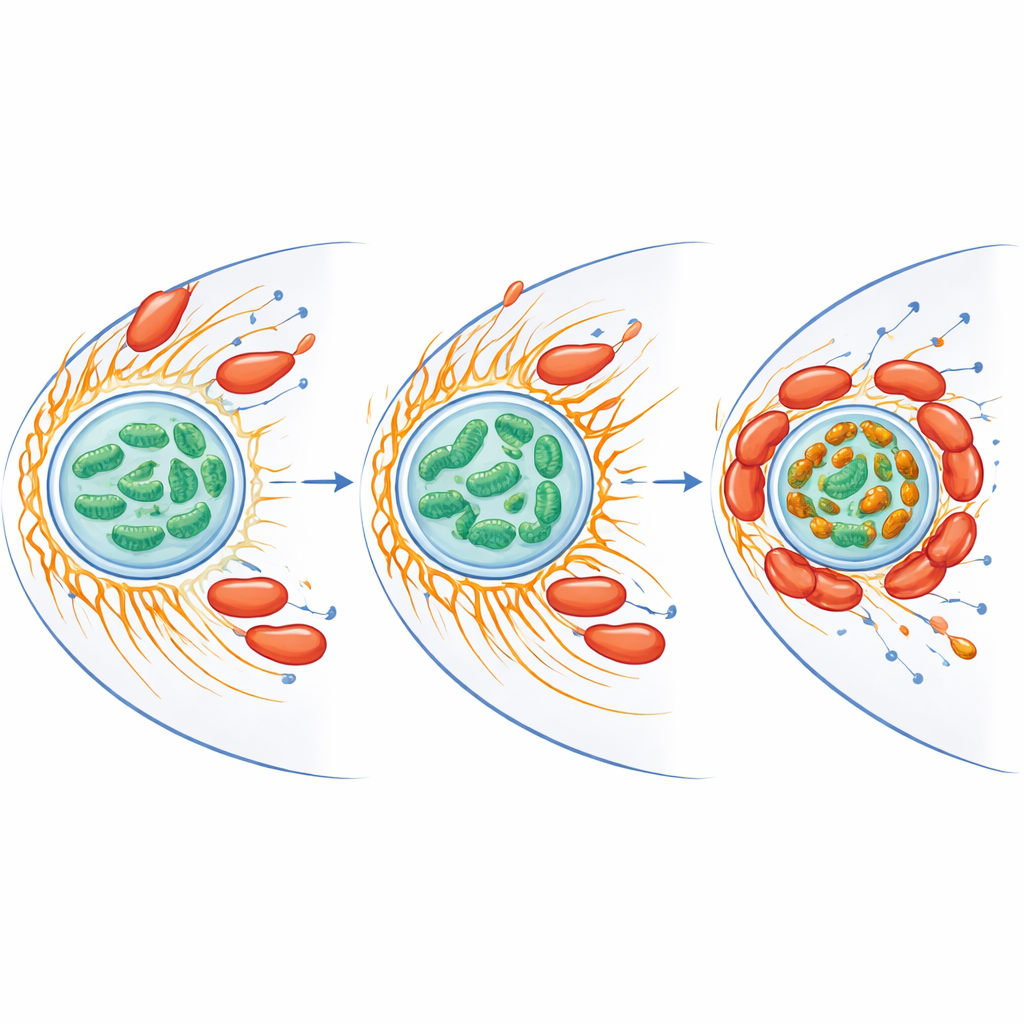
Eisen- und Stressumkehr im Wirtszellinneren
Mitochondrien machen nicht nur Energie– sie kümmern sich auch um Eisen und produzieren reaktive Sauerstoffspezies, chemisch aggressive Sauerstoffformen, die Mikroben abtöten können. Die Forschenden stellten fest, dass die Infektion die Gesamtmenge an freiem Eisen in Mitochondrien verringerte, gleichzeitig aber helle eisenreiche Cluster dort entstehen ließ, wo Mitochondrien um die Bakterien aggregierten. Proteine, die an der Eisenverarbeitung und am Schutz gegen oxidative Schäden beteiligt sind, stiegen sowohl beim Wirt als auch beim Bakterium an. Entfernte das Team freies Eisen mithilfe einer chelatbildenden Verbindung, fiel der Ausstoß reaktiver Sauerstoffspezies in der Amöbe und das Überleben von C. jejuni stieg dramatisch. Mitochondrien in infizierten Zellen zeigten außerdem ein höheres Membranpotenzial, ein Zeichen erhöhter Aktivität, was darauf hindeutet, dass das Bakterium die Kraftwerke des Wirts in einen Zustand bringt, der sein eigenes Persistieren begünstigt und gleichzeitig schädliche Sauerstoffchemie einschränkt.
Was das für Lebensmittelsicherheit und Infektionen bedeutet
Insgesamt stützen die Ergebnisse eine zweistufige Strategie: Zuerst stimuliert CiaD das Aktinwachstum, um dem Bakterium das Eindringen in Amöben zu erleichtern und Mitochondrien zur Eintrittsstelle zu ziehen; zweitens baut CiaI lokal Aktin ab und formt Mitochondrien zu eisenreichen Clustern um das bakterielle Kompartment, während es die oxidativen Abwehrmechanismen des Wirts abschwächt. Diese fein abgestimmte Kontrolle von Zellform, Energieverwendung und Metallhaushalt hilft C. jejuni, in Amöben zu überleben und trägt wahrscheinlich zu seiner Fähigkeit bei, in der Umwelt zu persistieren und später Menschen zu infizieren. Indem die Studie die Schlüsselfaktoren in diesem mikroskopischen Tauziehen offenlegt, weist sie auf neue Angriffspunkte – etwa die Cia‑Proteine, Aktin‑Mitochondrien‑Kontakte oder Eisenverarbeitungswege – die gestört werden könnten, um Kontaminationen und Krankheiten zu reduzieren.
Zitation: Nasher, F., Wren, B.W. A two-step actin-mediated strategy enables Campylobacter jejuni to promote mitochondrial aggregation and iron homeostasis, for intracellular survival and persistence. Commun Biol 9, 431 (2026). https://doi.org/10.1038/s42003-026-09713-9
Schlüsselwörter: Campylobacter, Amoeben, Mitochondrien, Aktin-Zytoskelett, Eisenhomöostase