Clear Sky Science · de
Mehrschichtige Regulation der GluK3-Kainat‑Rezeptoren wird durch Neto‑Untereinheiten und Zink vermittelt
Warum winzige Schalter im Gehirn wichtig sind
Jeder Gedanke, jedes Erinnern und jede Stimmung im Gehirn beruht auf mikroskopisch kleinen Schaltern, die den Fluss geladener Teilchen in und aus Nervenzellen erlauben. Diese Studie konzentriert sich auf einen solchen Schalter, einen wenig bekannten Rezeptor namens GluK3. Indem sie aufdeckt, wie Partnerproteine und Zinkionen das Verhalten von GluK3 feinabstimmen, liefern die Ergebnisse Hinweise darauf, wie neuronale Schaltkreise im Gleichgewicht bleiben – und wie dieses Gleichgewicht bei Erkrankungen wie Epilepsie, Depression und Schizophrenie kippen kann.
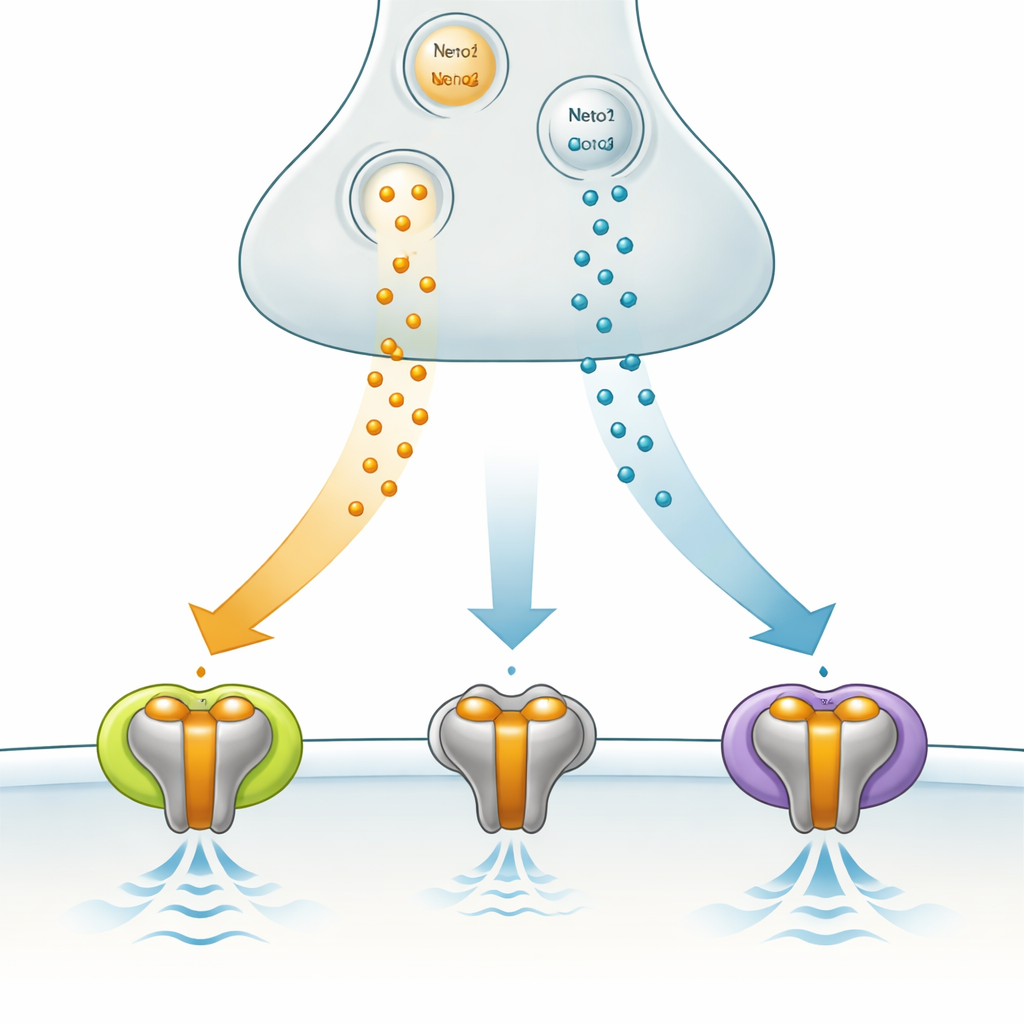
Ein spezialisierter Signalfilter im Gehirn
GluK3 gehört zur Familie der Kainat‑Rezeptoren, die zur größeren Gruppe der Glutamatrezeptoren zählen und die schnelle Kommunikation zwischen Neuronen vermitteln. Im Gegensatz zu einigen Verwandten schaltet GluK3 Signale nicht einfach ein oder aus; es wirkt eher wie ein Filter, der am besten auf kurze, starke Ausbrüche des Botenstoffs Glutamat reagiert. Es ist in Hirnregionen wie dem Hippocampus besonders stark vertreten, einem Bereich, der für Gedächtnis und die Musterung neuronaler Rhythmen wichtig ist, und Veränderungen in der GluK3‑Funktion wurden mit angst‑ähnlichem Verhalten in Verbindung gebracht. Diese Eigenschaften machen GluK3 zu einem vielversprechenden, aber noch wenig verstandenen Ziel, um die Gehirnaktivität bei Gesundheit und Krankheit zu beeinflussen.
Hilfsproteine, die die Fäden ziehen
Das Team untersuchte, wie zwei Hilfsproteine, Neto1 und Neto2, das Verhalten von GluK3 in menschlichen Zellen verändern, die so verändert wurden, dass sie diese Komponenten herstellen. Beide Helfer verlangsamen, wie schnell GluK3 nach Aktivierung wieder abschaltet, und beide verringern eine natürliche Form von innerer Blockade, die normalerweise den Stromfluss einschränkt. Sie hatten jedoch entgegengesetzte Wirkungen auf die Geschwindigkeit, mit der GluK3 wiederverwendet werden kann. Mit Neto1 erholten sich die Rezeptoren schnell und waren bereit, auf rasch wiederkehrende Signale zu reagieren. Mit Neto2 wurde die Erholung deutlich langsamer, was die Integration von Signalen über längere Intervalle begünstigt. Im Kern kann eine Synapse durch die Wahl unterschiedlicher Hilfsproteine entscheiden, ob GluK3 wie ein Schnellfeuer‑Detektor oder eher wie ein langsamer, mittelnder Sensor agiert.
Zink als zweite Kontrollebene
Viele glutamatreleasingende Nervenendigungen setzen auch Zink frei, das an Rezeptoren binden und deren Funktion verändern kann. Frühere Arbeiten zeigten, dass Zink GluK3 ungewöhnlich verstärkt, während es andere Rezeptortypen eher dämpft. Hier fanden die Autoren heraus, dass diese Verstärkung stark davon abhängt, welches Neto‑Protein vorhanden ist. Wenn GluK3 allein wirkt, verdoppelt Zink ungefähr die Zeit, die der Rezeptor aktiv bleibt, und erhöht den Strom leicht. Die Zugabe von Neto1 schwächt diesen Effekt ab. Im Gegensatz dazu verstärken sich bei einer Partnerschaft von GluK3 mit Neto2 Zink und Neto2 gegenseitig und verstärken den Strom stark, weit mehr als jeder für sich allein. Das legt nahe, dass Synapsen, die reich an Neto2 und Zink sind, GluK3‑vermittelte Signale bei intensiver Aktivität stark verstärken können, während Neto1‑reiche Synapsen zurückhaltender bleiben.
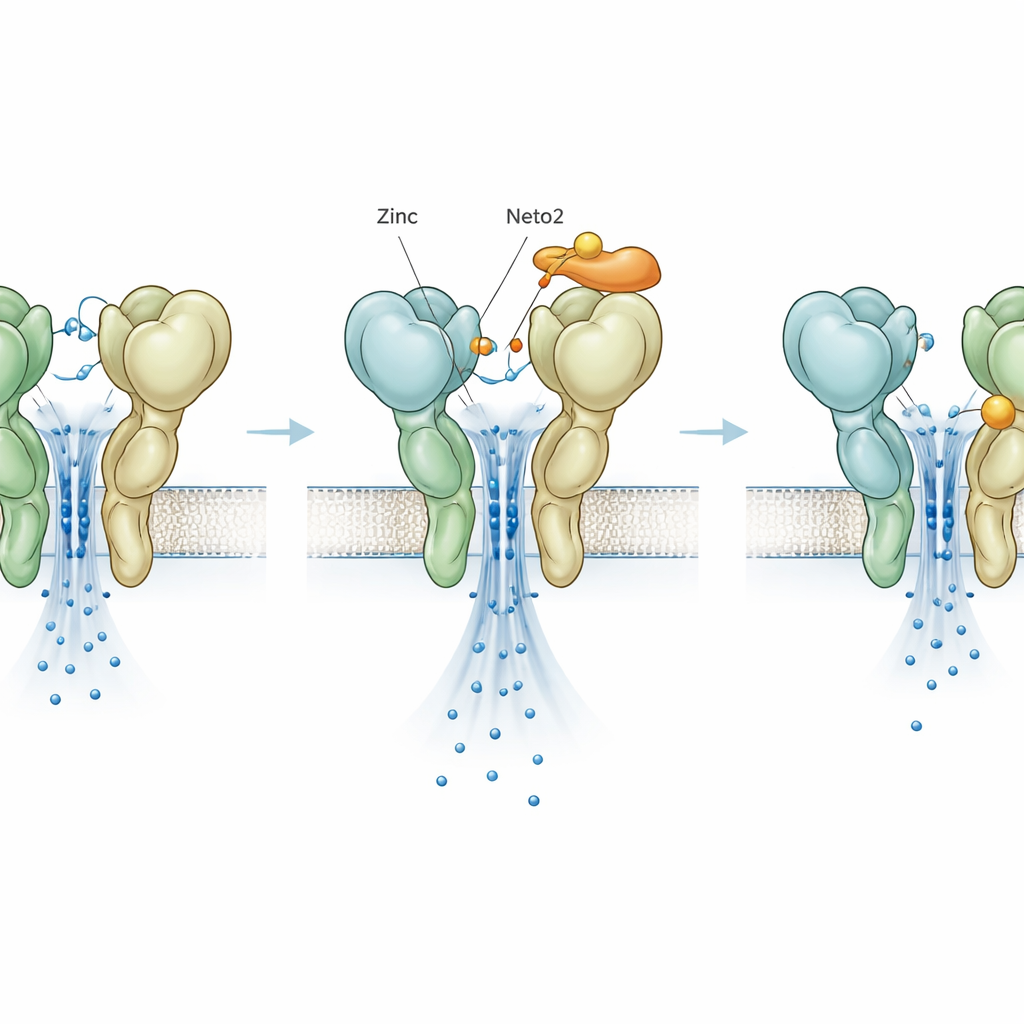
Eine verborgene Bremse, die durch Mutation offenbart wird
Um die Wirkungen des Zinks von denen der Hilfsproteine zu trennen, erzeugten die Forscher eine Einbuchstabenänderung in GluK3, genannt D759G, die eine bekannte Zinkbindungsstelle entfernt. Wie erwartet machte diese Mutation den Rezeptor stabiler und langsamer im Abschalten, was den üblichen Effekt von Zink nachahmt. Überraschenderweise bewirkte zugesetztes Zink bei diesem Mutanten keine Verstärkung der Aktivität mehr; stattdessen beschleunigte es das Abschalten und verringerte den Strom, wodurch eine zweite, zuvor verborgene Zinkstelle zu Tage trat, die als Bremse wirkt. Neto1 und Neto2 behielten ihre charakteristischen Effekte beim Mutanten bei, was zeigt, dass ihr grundlegender Einfluss nicht von der ursprünglichen Zinkstelle abhängt. Doch selbst diese neu entdeckte hemmende Zinkwirkung wurde unterschiedlich von den beiden Helfern abgestimmt, sodass dem System eine weitere einstellbare Stellschraube hinzugefügt wird.
Struktur sichtbar machen, um Verhalten zu erklären
Um Funktion und Form zu verbinden, nutzte das Team Kryo‑Elektronenmikroskopie, um den mutierten GluK3‑Rezeptor in einem nicht‑aktiven Zustand einzufrieren und sichtbar zu machen. Die Bilder zeigten, dass der Bereich, der Glutamat bindet, beim D759G‑Mutanten eine kompaktere, enger gepackte Einheit bildet im Vergleich zum normalen GluK3. Diese strukturelle Straffung erschwert wahrscheinlich das Umschwingen des Rezeptors in eine abschaltende Konformation, was erklärt, warum der Mutant, ähnlich wie das zinkgebundene GluK3, länger aktiv bleibt. Gleichzeitig zeigten die Bilder, dass nicht alle Teile des Rezeptors in einer einzigen Anordnung fixiert sind, was auf eine von Natur aus flexible Architektur hinweist, die besonders empfindlich auf kleine chemische Einflüsse reagiert.
Was das für die Gehirngesundheit bedeutet
In der Summe zeichnet die Studie GluK3 nicht als einfachen Ein‑/Aus‑Schalter, sondern als fein justierbaren Knotenpunkt, an dem Glutamat, Hilfsproteine und Zink zusammenlaufen. Neto1 und Neto2 bestimmen, wie schnell Signale verklingen und wie rasch Rezeptoren wieder reagieren können, während Zink die Aktivität über mehrere Bindungsstellen entweder weiter verstärken oder unter bestimmten Bedingungen einschränken kann. Da GluK3, Neto‑Proteine und Zink alle an Synapsen vorkommen, die am Gedächtnis beteiligt sind, und mit Epilepsie sowie psychiatrischen Störungen in Verbindung gebracht werden, könnte das Verständnis dieser mehrschichtigen Kontrolle künftige Therapien leiten, die synaptische Signale behutsam nachregulieren, statt sie komplett auszuschalten.
Zitation: Vinnakota, R., Dawath, B.K., Assaiya, A. et al. Multilayered regulation of GluK3 kainate receptors is mediated by Neto subunits and zinc. Commun Biol 9, 420 (2026). https://doi.org/10.1038/s42003-026-09707-7
Schlüsselwörter: Kainat‑Rezeptoren, GluK3, Neto‑Proteine, synaptisches Zink, synaptische Plastizität