Clear Sky Science · de
Suchtmittelmissbrauch und Depression – ein Fokus auf Epigenetik
Warum diese Forschung für den Alltag wichtig ist
Suchtmittel und Depression werden häufig als getrennte Probleme behandelt, treten jedoch oft gemeinsam bei derselben Person auf. Dieser Übersichtsartikel erklärt, wie langfristiger Konsum von Substanzen wie Methamphetamin, Kokain, Opioiden und Cannabis dauerhafte „molekulare Narben" im Gehirn hinterlassen kann, die das Depressionsrisiko erhöhen. Indem diese verborgenen Veränderungen aufgedeckt werden, weist der Artikel auf mögliche Tests hin, die vorhersagen könnten, wer am stärksten gefährdet ist — sowie auf präzisere Behandlungen, die den Schaden rückgängig machen könnten, statt nur die Symptome zu überdecken.
Wie Sucht und Niedergeschlagenheit miteinander verknüpft werden
Die Autor:innen beginnen mit der Darstellung der engen klinischen Verbindung zwischen Drogenmissbrauch und Depression. Menschen, die wiederholt suchterzeugende Substanzen konsumieren, berichten deutlich häufiger von anhaltender Traurigkeit, Verlust von Freude, Schlafstörungen und Suizidgedanken. Gehirnregionen, die Belohnung, Motivation, Erinnerung und Entscheidungsfindung steuern – die ventrale tegmentale Area, das Nucleus accumbens, der präfrontale Kortex und der Hippocampus – sind für beide Zustände zentral. Chronische Drogenexposition stört Neurotransmitter wie Dopamin und Serotonin, Stresshormone der hypothalamisch-hypophysär-adrenalen Achse, Immun-Signale und die Energieversorgung der Neurone. Zusammengenommen machen diese Veränderungen das Gehirn weniger widerstandsfähig gegen Stress und anfälliger für depressive Zustände, selbst lange nach der letzten Dosis.
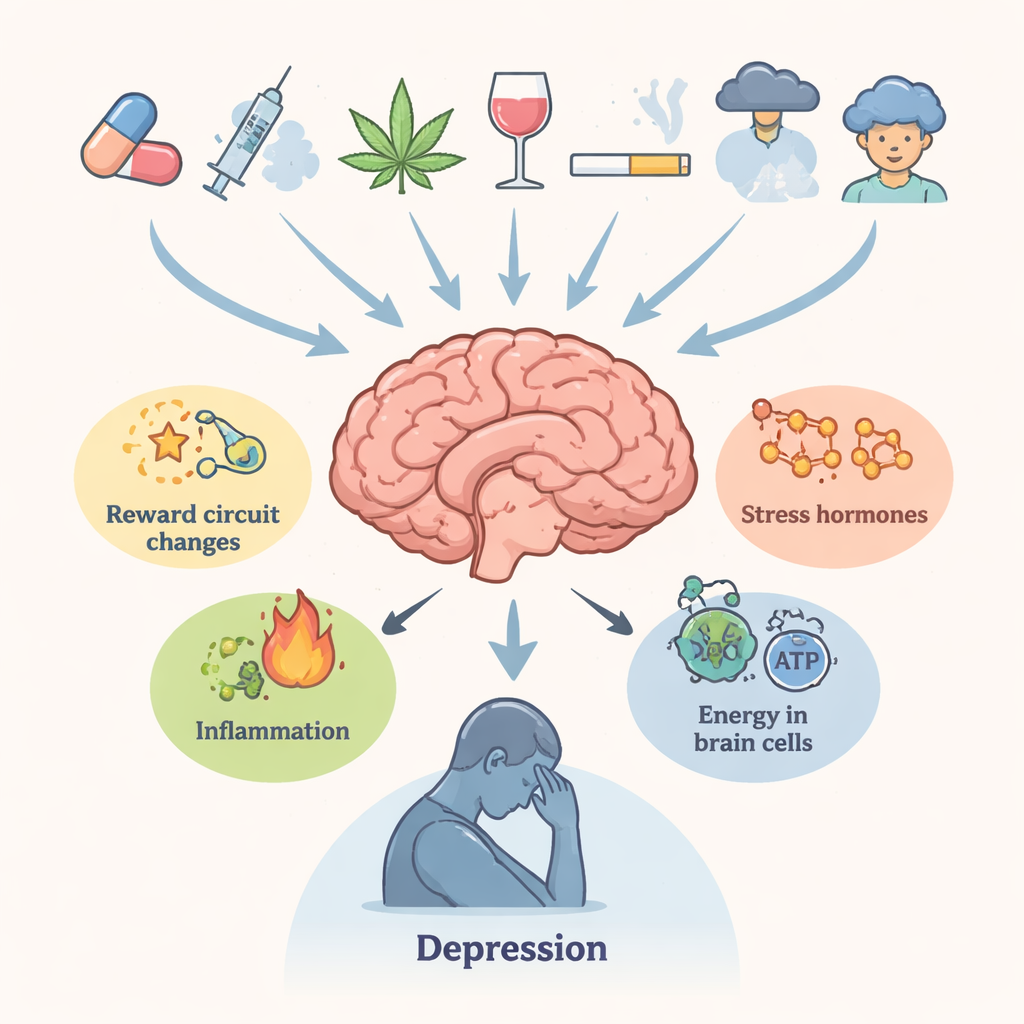
Drogen, die die Chemie des Gehirns umgestalten
Die Übersicht behandelt mehrere wichtige Wirkstoffklassen. Amphetaminartige Stimulanzien und verwandte Substanzen, einschließlich synthetischer „Bath Salts“, verursachen starke Dopamin- und andere Neurotransmitter-Spitzen, die langfristig Nervenendigungen schädigen, das Glutamatgleichgewicht stören, das endoplasmatische Retikulum belasten und Zellen in schädliche Autophagie treiben können. Cannabiskonsum in der Adoleszenz steht in Verbindung mit späterer Depression und erhöhtem Suizidrisiko, vermutlich durch lang anhaltende Veränderungen an Cannabinoidrezeptoren, der weißen Substanzstruktur und der Empfindlichkeit dopaminerger Schaltkreise. Opioide lindern zwar Schmerzen, können jedoch Entzündungen, Mitochondrienversagen und eine Verringerung wachstumsfördernder Signale wie des brain-derived neurotrophic factor (BDNF) auslösen. Kokain aktiviert wiederholt das Stresssystem und verändert Schlüsselregulatoren wie FKBP5, was zu Angst und gedrückter Stimmung während des Entzugs beiträgt. In jedem Fall neigen die biologischen Störungen dazu, anzuhalten, was erklärt, warum emotionale Symptome die offensichtliche Intoxikation oft überdauern.
Epigenetik: das Gedächtnis der Exposition
Um zu verstehen, warum Drogeneffekte andauern, konzentrieren sich die Autor:innen auf die Epigenetik – chemische Markierungen und molekulare Schalter, die die Genaktivität anpassen, ohne die DNA-Buchstaben zu ändern. Suchtmittel verändern die DNA-Methylierung (eine Markierung an Cytosinbasen), verändern chemische Gruppen an Histonproteinen, die DNA verpacken, und beeinflussen nichtkodierende RNAs, die die Produktion bestimmter Proteine feinjustieren. Beispielsweise verschieben Methamphetamin und Kokain Methylierungsmuster in belohnungsrelevanten Hirnregionen und verändern die Konzentration von Enzymen, die diese Markierungen hinzufügen oder entfernen. Opioide und Stimulanzien remodeln Histon-Acetylierung und -Methylierung an Genen, die Glutamatrezeptoren, Stresssignale und synaptische Struktur steuern. Dutzende von microRNAs, langen nichtkodierenden RNAs und zirkulären RNAs steigen oder fallen unter Drogenexposition und beeinflussen gemeinsam Entzündung, Neuronenwachstum und die Stärke von Synapsen. Diese epigenetischen Veränderungen wirken wie ein molekulares „Gedächtnis" der Drogenvorgeschichte.
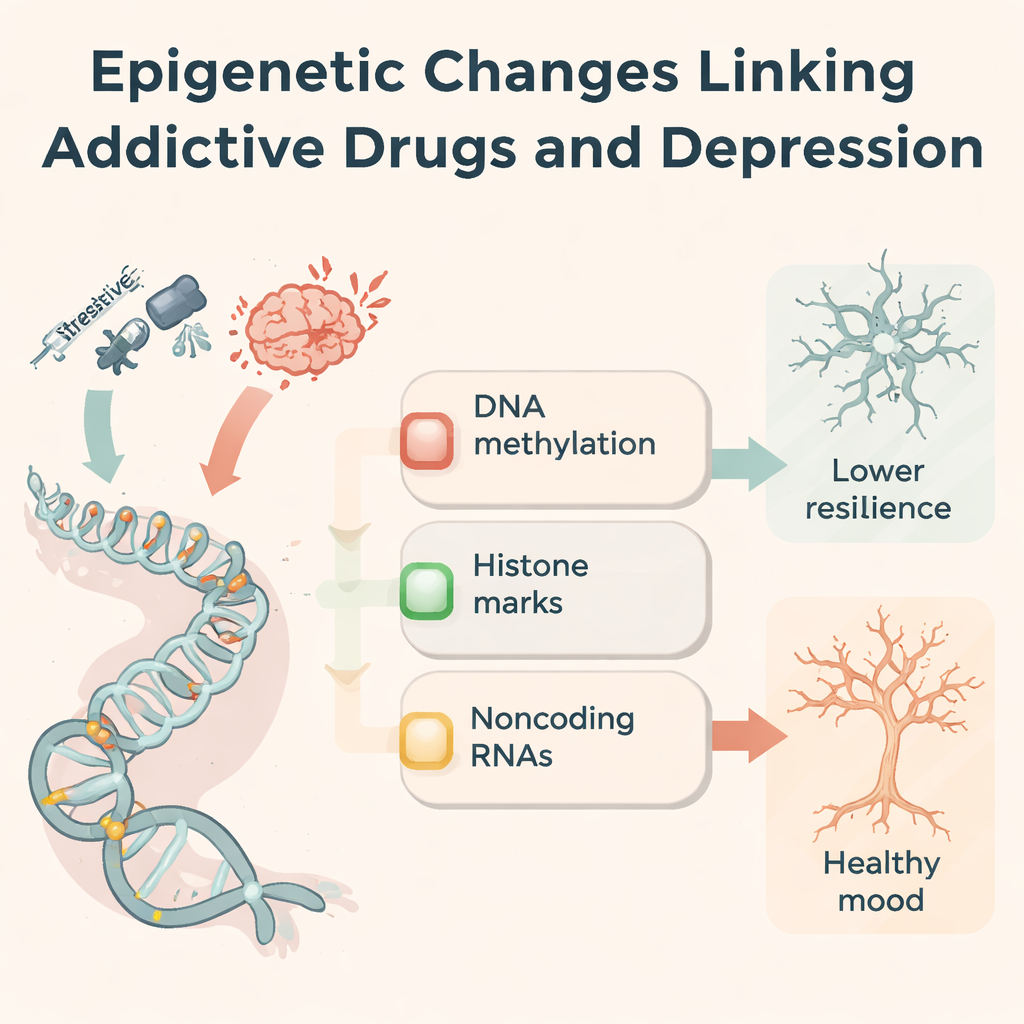
Geteilte molekulare Bahnen bei Depression und Sucht
Die gleiche epigenetische Maschinerie zeigt sich auch bei Menschen und Tieren mit Depression, die niemals Drogen genommen haben. Belastende Erfahrungen können die Methylierung von Stresshormonrezeptoren (wie NR3C1 und FKBP5) verändern, hilfreiche Wachstumsfaktoren wie BDNF reduzieren und Immun- sowie Glutamatwege umverdrahten. Viele derselben nichtkodierenden RNAs, die durch Drogen verändert werden, sind auch bei Depression fehlreguliert und beeinflussen, wie neue Neuronen entstehen, wie Mikroglia auf Entzündungen reagieren und wie stark Synapsen verbunden sind. Die Autor:innen schlagen einen Dreiteilerrahmen vor: Stressantwort-Regulation, Umgestaltung von Belohnungsschaltkreisen und synaptische Plastizität. Entlang dieser Achsen konvergieren Sucht und Depression wiederholt auf eine kleine Gruppe von Genen und Markierungen, was einen biologischen Grund dafür nahelegt, warum die beiden Störungen so häufig gemeinsam auftreten.
Was das für Prävention und Therapie der Zukunft bedeutet
Abschließend argumentiert die Übersicht, dass epigenetische Veränderungen zu Frühwarn-Biomarkern und Zielen für die nächste Generation von Therapien werden könnten. Breit wirkende Wirkstoffe, die epigenetische Markierungen löschen, haben bei Tieren bereits einige antidepressiv-ähnliche Effekte gezeigt, sind aber für den routinemäßigen Einsatz beim Menschen zu grob. Neue Werkzeuge – wie CRISPR-basierte Epigenom-Editoren und Therapien, die spezifische microRNAs oder lange RNAs modulieren – könnten eines Tages problematische Gene in bestimmten Gehirnzellen gezielt anpassen und andere verschonen. Die Autor:innen mahnen, dass die meisten aktuellen Daten von Nagetieren und aus Gesamtgewebe des Gehirns stammen und die menschliche Biologie komplexer ist. Dennoch bietet diese Arbeit, indem sie zeigt, wie Suchtmittel und Depression im selben molekularen „Notizbuch" niedergeschrieben werden, einen hoffnungsvollen Weg zu persönlicheren und nachhaltigen Therapien.
Zitation: Zhang, W., Xu, M., Wang, C. et al. Addictive drug abuse and depression-a focus on epigenetics. Commun Biol 9, 297 (2026). https://doi.org/10.1038/s42003-026-09705-9
Schlüsselwörter: Sucht und Depression, Epigenetik, Drogenmissbrauch, DNA-Methylierung, nichtkodierende RNA