Clear Sky Science · de
Med13 ist an der radialen Migration und der kontralateralen Projektion kortikaler Neuronen über PlxnA4 beteiligt
Wie ein einzelnes Gen beim Bau des denkenden Gehirns hilft
Gehirne wachsen nicht einfach nur; sie werden gebaut, Zelle für Zelle, in präzise organisierten Schichten und Verdrahtungsmustern. Diese Studie untersucht, wie ein Gen namens Med13 jungen Gehirnzellen in der Großhirnrinde hilft, an den richtigen Ort zu gelangen und Verbindungen zwischen den Hemisphären herzustellen. Da subtile Fehler in diesem Aufbauprozess zunehmend mit Erkrankungen wie Autismus und geistiger Behinderung in Verbindung gebracht werden, liefert das Verständnis von Med13 Einblicke, wie frühe Gehirnentwicklung schiefgehen kann.
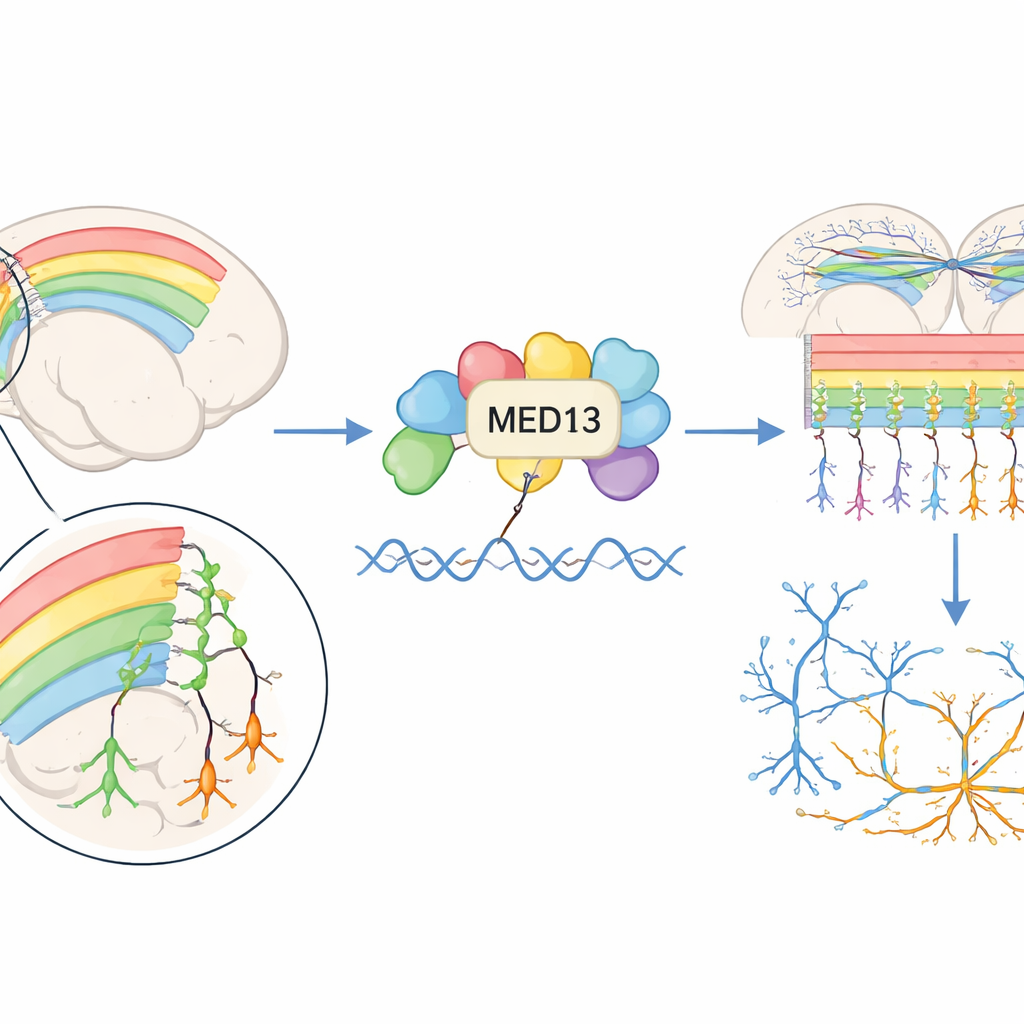
Die sechs Schichten der Großhirnrinde aufbauen
Die Großhirnrinde, die gefurchte äußere Schicht des Gehirns, ist in sechs Schichten von Nervenzellen organisiert, die während der Embryonalentwicklung entstehen. Neugeborene Neuronen entstehen tief im Gehirn und wandern dann in einer „innen-nach-außen“-Reihenfolge nach außen, um diese Schichten zu bilden. Die Autorinnen und Autoren fragten zuerst, wo und wann Med13 während dieses Prozesses aktiv ist. In Maus-Embryonen wurde Med13 in hoher Konzentration in Regionen nachgewiesen, in denen sich neuronale Stammzellen teilen und wo junge Neuronen unterwegs sind, besonders zu einem wichtigen Zeitpunkt in der mittleren Schwangerschaftsphase, in der viele kortikale Neuronen gebildet werden. Med13 war sowohl in teilenden Vorläuferzellen als auch in reifenden Neuronen vorhanden, was darauf hindeutet, dass es allgemein an der Gestaltbildung der Rinde beteiligt ist.
Wenn Neuronen vom Weg abkommen
Um zu prüfen, was Med13 tatsächlich bewirkt, reduzierten die Forschenden selektiv dessen Menge in sich entwickelnden kortikalen Neuronen von Mäusen mithilfe einer Technik, die gezielte DNA in das fetale Gehirn einführt. Markierte Neuronen ohne Med13 wurden über die Zeit verfolgt. Im Vergleich zu Kontrollneuronen blieben viele Med13-defiziente Zellen auf halbem Weg ihrer Wanderung stehen, anstatt die oberen Kortikalschichten zu erreichen, in denen sie hingehören. Selbst Tage nach der Geburt blieb ein großer Teil verstreut im tieferen Gewebe oder in der darunterliegenden weißen Substanz. Diese fehlplatzierten Zellen zeigten außerdem Anzeichen unvollständiger Reifung: Einige exprimierten keine Marker, die typisch für vollständig entwickelte obere Schicht-Neuronen sind, verwandelten sich jedoch nicht in andere Zelltypen wie untere Schicht-Neuronen oder Gliazellen. Das deutet darauf hin, dass Med13 nicht nur dafür nötig ist, dass Neuronen ihr Ziel erreichen, sondern auch, dass sie vollständig ihre korrekte Identität annehmen.
Gebrochene Brücken zwischen den Gehirnhemisphären
Eine ordnungsgemäße Gehirnfunktion hängt von Fernverbindungen zwischen Neuronen ab, einschließlich Fasern, die über das Corpus callosum die Mittellinie queren, um die linke und rechte Hemisphäre zu verbinden. Die Forschenden fanden heraus, dass Neuronen ohne Med13 viel schlechtere Projektionen zur gegenüberliegenden Gehirnseite aufwiesen. Weniger Axone drangen in die entsprechende Region der kontralateralen Rinde ein, und dieses Defizit wurde im Verlauf der Entwicklung ausgeprägter. Gleichzeitig waren die dendritischen „Bäume“, die eingehende Signale empfangen, deutlich einfacher: Med13-defiziente Neuronen hatten weniger Verzweigungen und eine kürzere gesamte dendritische Länge. Zusammengenommen deuten diese Veränderungen darauf hin, dass Med13 ein zentraler Organisator sowohl dafür ist, wo Neuronen landen, als auch dafür, wie reichhaltig sie Verbindungen zu ihren Partnern ausbilden.
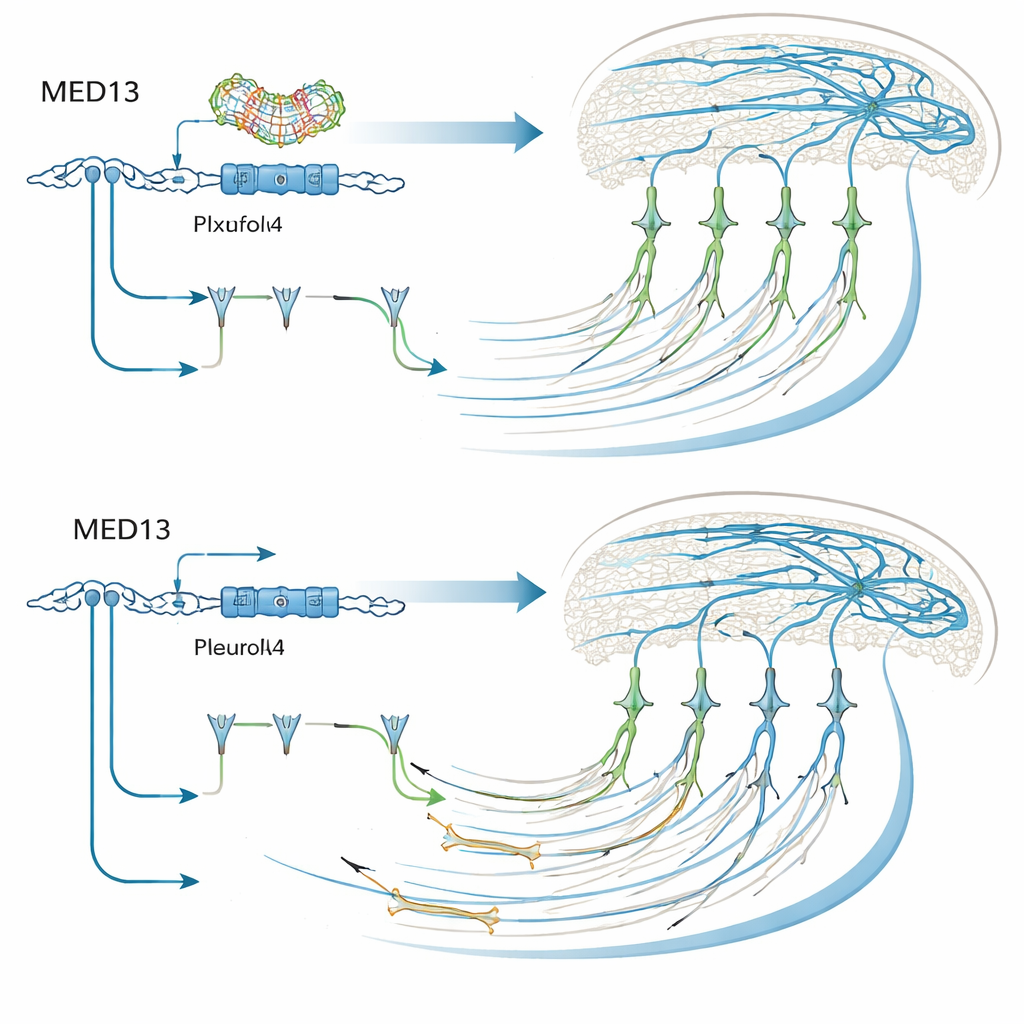
Von Genkontrolle zu Orientierungssignalen
Med13 ist Teil eines großen Proteinverbunds, der steuert, welche anderen Gene ein- oder ausgeschaltet werden. Daher suchten die Autorinnen und Autoren als Nächstes nach downstream-Effektoren, die seine Wirkungen erklären könnten. Mithilfe menschlicher, nervenähnlicher Zellen, in denen MED13 fehlte, katalogisierten sie Tausende von Proteinen und fanden über hundert, deren Mengen sich veränderten. Viele waren an Form, Bewegung und Entwicklung der Rinde beteiligt, und mehrere überschneiden sich mit bekannten Risiko-Genen für neuroentwicklungsbedingte Störungen. Ein Kandidat stach heraus: PlxnA4, ein Rezeptor, der Neuronen hilft, auf Orientierungssignale zu reagieren, während sie migrieren und Axone ausstrecken. Die PlxnA4-Spiegel sanken, wenn MED13 fehlte, sowohl in kultivierten menschlichen Zellen als auch in Mausneuronen mit reduziertem Med13. Bemerkenswerterweise konnte die erzwungene Überexpression von PlxnA4 in Neuronen deren Migrationsprobleme weitgehend beheben und einen Großteil ihrer callosalen Projektionen wiederherstellen, selbst wenn Med13 ausgeschaltet war. Dies behob jedoch nicht die vereinfachte dendritische Architektur, was darauf hindeutet, dass Med13 auch über andere Ziele wirkt, um neuronale Verzweigungen zu formen.
Was das für Gehirnerkrankungen bedeutet
Diese Befunde zeigen zusammen, dass Med13 jungen kortikalen Neuronen hilft, in die richtigen Schichten zu wandern und Langstreckenverbindungen auszubilden, zum Teil indem es das Orientierungsmolekül PlxnA4 aufrechterhält. Wenn Med13 gestört ist, fehlplatzieren sich Neuronen, entwickeln ihre Verzweigungen unzureichend und schicken weniger Fasern über das Corpus callosum — alles Veränderungen, die Gehirnveränderungen ähneln, die bei einigen neuroentwicklungsbedingten Störungen beobachtet werden. Obwohl viele weitere Gene und Signale beteiligt sind, positioniert die Einordnung von Med13 als zentralen Regulator ein klareres Bild davon, wie frühe genetische Veränderungen die Verschaltung des Gehirns und letztlich das Verhalten beeinflussen können.
Zitation: Li, ZX., Tu, SX., Li, YW. et al. Med13 is involved in the radial migration and contralateral projection of cortical neurons via PlxnA4. Commun Biol 9, 394 (2026). https://doi.org/10.1038/s42003-026-09704-w
Schlüsselwörter: kortikale Entwicklung, neuronale Migration, Corpus callosum, neuroentwicklungsstörungen, Genregulation