Clear Sky Science · de
Heterogenität zwischen VIP- und GRP-Neuronen bildet die Grundlage für AVP-Rezeptorsignalgebung im suprachiasmatischen Nukleus der Maus
Warum unsere Körperuhr so schwer zu verstellen ist
Jeder, der nach einem langen Flug durcheinandergeraten ist oder mit Nachtschichten zu kämpfen hatte, weiß, dass unsere innere Uhr plötzliche Zeitplanänderungen nicht mag. Dieses Paper stellt eine sehr konkrete Frage, die dem Kern dieses Problems gilt: Warum reagieren in der Hauptuhr des Gehirns einige Nervenzellen stark auf ein Zeitsignal, während benachbarte Zellen es weitgehend ignorieren? Indem die Autoren ein einzelnes chemisches Signal durch diesen winzigen Uhrenkreis bei Mäusen nachverfolgen, enthüllen sie eine versteckte Untergruppe von Zellen, die mitbestimmt, wie hartnäckig unsere Körperuhr bei „Jetlag“ ist. 
Eine winzige Uhr mit vielen Akteuren
Die Hauptuhr bei Säugetieren sitzt in einer kleinen Region des Gehirns, dem suprachiasmatischen Nukleus, kurz SCN. Obwohl sie nur etwa 20.000 Nervenzellen enthält, setzt sie sich aus mehreren unterschiedlichen Gruppen zusammen, die über verschiedene chemische Botenstoffe miteinander kommunizieren. Zellen in der oberen „Schale“ setzen überwiegend den Botenstoff Arginin-Vasopressin (AVP) frei, während Zellen in der unteren „Kern“-Region häufig andere Botenstoffe freisetzen, darunter vasoaktives intestinales Peptid (VIP) und gastrin-freisetzendes Peptid (GRP). Zusammen müssen diese Gruppen synchron bleiben, um die 24-Stunden-Rhythmen zu erzeugen, die Schlaf, Hormonfreisetzung und viele andere Körperfunktionen steuern. Welche genauen Zellen im Kern jedoch auf Signale von AVP-Zellen in der Schale hören, war bislang unklar.
Die Verkabelung von Sender- zu Empfängerzellen verfolgen
Die Forscher kartierten zunächst, wie sich AVP-Zellen in der Schale physisch mit VIP- und GRP-Zellen im Kern verbinden. Sie nutzten ein Virus, um die ausgehenden Fasern und mögliche Kontaktstellen der AVP-Neurone in Mäusen zu markieren, und färbten dann Hirnschnitte, um zu sehen, wo diese Fasern endeten. Sie fanden, dass AVP-Fasern offenbar Kontaktstellen sowohl an VIP- als auch an GRP-Zellen ausbildeten, jedoch in unterschiedlichen Anteilen: etwa ein Viertel der VIP-Zellen und mehr als die Hälfte der GRP-Zellen zeigten diese Appositionen. Das zeigte, dass AVP-Neurone beide Zelltypen im Kern erreichen, aber nicht, welche davon tatsächlich auf das Signal reagieren. Um das zu testen, verwendete das Team Optogenetik — sie aktivierten AVP-Neurone mit blauem Licht — und suchten dann nach c-Fos, einem Marker für zelluläre Aktivierung, in VIP- und GRP-Neuronen.
Eine kleine VIP-Untergruppe, die AVP wirklich „hört”
Als AVP-Neurone durch Licht stimuliert wurden, schalteten viele AVP-Zellen selbst c-Fos ein, wie zu erwarten war. Wichtig war, dass eine kleine Untergruppe von VIP-Zellen im Kern ebenfalls c-Fos-Aktivierung zeigte, obwohl sie das lichtempfindliche Protein nicht direkt exprimierten. Das deutet darauf hin, dass sie indirekt durch AVP-Eingang angetrieben wurden. Im Gegensatz dazu zeigten GRP-Zellen selten c-Fos, obwohl sie AVP-Kontakte erhielten. Die Autoren suchten dann mit empfindlichen RNA-Bildgebungsmethoden nach der Boten-RNA des AVP-Rezeptors V1a in diesen Populationen. Sie entdeckten, dass V1a nur in einer Minderheit der VIP-Zellen vorhanden war und in GRP-Zellen kaum nachweisbar war. Somit scheint unter den vielen VIP-Neuronen eine kleine V1a-positive Untergruppe speziell darauf abgestimmt zu sein, AVP-Signale zu empfangen und darauf zu reagieren, während die meisten GRP-Neuronen dies nicht tun. 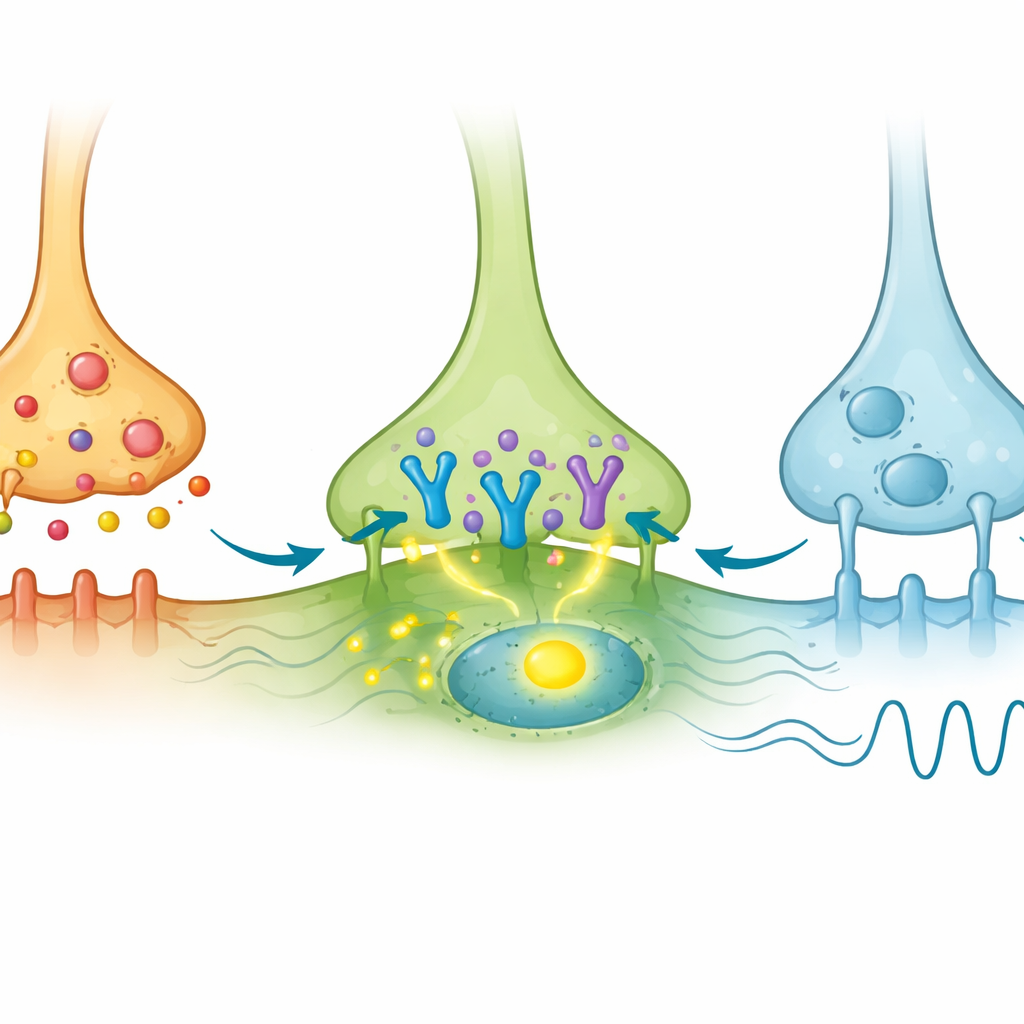
Wie eine winzige Zellgruppe die Erholung von Jetlag prägt
Um die Funktion dieser V1a-tragenden VIP-Neuronen zu untersuchen, erzeugten die Forscher Mäuse, bei denen der V1a-Rezeptor nur in VIP-Zellen entfernt wurde. Diese Tiere zeigten bei konstanter Dunkelheit eine normale Periodenlänge des täglichen Rhythmus, was zeigt, dass dieser Rezeptor in VIP-Neuronen nicht nötig ist, um das grundlegende Taktmaß der Uhr festzulegen. Als jedoch der Licht–Dunkel-Zyklus plötzlich um acht Stunden vor- oder zurückgestellt wurde, um Jetlag zu simulieren, passten sich die modifizierten Mäuse schneller an als ihre normalen Wurfgeschwister, besonders nach Vorverlegungen und bei männlichen Tieren. In anderen Experimenten hatte das Entfernen von V1a im gesamten Gehirn oder spezifisch im SCN ein ähnliches, „jetlag-resistentes“ Verhalten gezeigt. Die neuen Ergebnisse legen daher nahe, dass eine überraschend kleine Gruppe von VIP-Neuronen mit V1a-Rezeptoren einen überproportionalen Einfluss darauf haben kann, wie starr oder flexibel die Gesamtuhr ist.
Was das für unser Zeitgefühl bedeutet
Alltäglich gesprochen zeigt diese Studie, dass AVP-produzierende Neurone innerhalb der zentralen Uhr des Gehirns wie Zeitgeber in einer oberen Ebene wirken und Signale über V1a-Rezeptoren an eine ausgewählte Gruppe von VIP-Neuronen in der unteren Ebene senden. Diese wenigen VIP-Zellen helfen dem gesamten Netzwerk, plötzliche Änderungen des Licht–Dunkel-Zyklus zu widerstehen, indem sie das Tempo verlangsamen, mit dem die Uhr nach einer Verschiebung zurückgesetzt wird. Das Entfernen ihres AVP-empfindlichen Rezeptors macht das System anpassungsbereiter und erleichtert jetlag-ähnliche Anpassungen bei Mäusen. Indem die Arbeit diese verborgene Vielfalt unter Uhrenneuronen aufzeigt, liefert sie ein detaillierteres Verkabelungsdiagramm dafür, wie unser inneres Zeitgefühl stabilisiert wird — und deutet an, dass das gezielte Manipulieren ähnlicher Wege beim Menschen eines Tages helfen könnte, Jetlag oder andere Rhythmusstörungen zu behandeln.
Zitation: Zhou, H., Moriyasu, D., Hsiao, SW. et al. Heterogeneity between VIP and GRP neurons underlies AVP receptor signaling in the mouse suprachiasmatic nucleus. Commun Biol 9, 414 (2026). https://doi.org/10.1038/s42003-026-09694-9
Schlüsselwörter: zirkadiane Uhr, suprachiasmatischer Nukleus, Vasopressin-Signalgebung, VIP-Neuronen, Jetlag