Clear Sky Science · de
Strukturelle Grundlage der Erkennung von Fledermausrezeptoren durch SARS-CoV-2 und SARS2-ähnliche Fledermaus-Coronaviren
Warum diese Fledermaus–Virus-Geschichte immer noch wichtig ist
Die COVID-19-Pandemie begann vor mehr als sechs Jahren, doch Wissenschaftlerinnen und Wissenschaftler setzen weiterhin zusammen, wie das Virus, das sie verursacht — SARS-CoV-2 — so erfolgreich Menschen infizieren konnte. Ein zentrales Rätsel ist, wie dieses Virus und seine nahen Verwandten in Fledermäusen an ein Protein namens ACE2 auf der Zelloberfläche andocken – ein erster und entscheidender Schritt für die Infektion. Das Verständnis dieser mikroskopischen Schloss-und-Schlüssel-Interaktionen kann klären, woher das Virus stammt, wie es sich angepasst hat und was passieren könnte, wenn verwandte Viren künftig auf den Menschen überspringen.
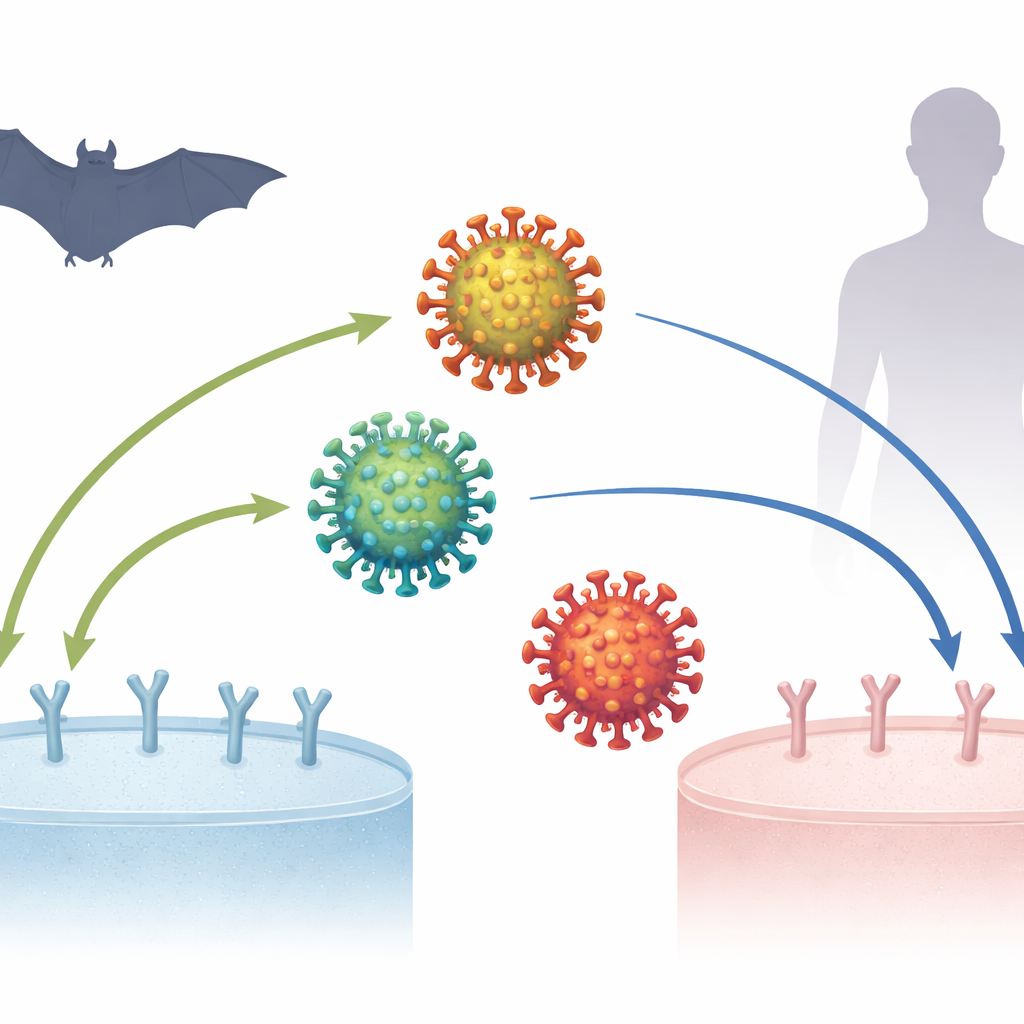
Der virale Händedruck unter der Lupe
Die Studie konzentriert sich auf das Spike-Protein, die kronenartige Struktur auf der Virusoberfläche, die ACE2 greift. Eine kleine Region des Spikes, die Rezeptorbindungsdomäne (RBD), wirkt wie eine Fingerspitze, die den ACE2-„Türknauf“ umklammert. Frühere Arbeiten zeigten, dass die RBD bei Wirtswechseln – etwa von Fledermäusen über Zibetkatzen zu Menschen – häufig Mutationen akkumuliert, die den Griff am neuen Wirts-ACE2 verbessern. SARS-CoV-2 stellte jedoch ein Rätsel dar: Seine ursprüngliche Form band menschliches ACE2 bereits sehr gut, noch bevor viel Zeit für Anpassung vergangen war, und einige in Fledermäusen gefundene, mit SARS-CoV-2 verwandte Viren schienen menschliches ACE2 sogar besser zu binden als fledermausliches ACE2. Das ließ einige vermuten, SARS-CoV-2 könnte eine Ausnahme von den üblichen evolutionären Regeln sein.
Fledermaus- und menschliche Rezeptoren im Vergleich
Um dieses Rätsel zu untersuchen, analysierten die Forschenden zwei Fledermaus-Coronaviren, die eng mit SARS-CoV-2 verwandt sind: BANAL-52 und BANAL-236. Sie verglichen, wie stark die RBDs dieser Viren und die von SARS-CoV-2 an ACE2 aus Menschen und verschiedenen Fledermausarten binden. Mit zellbasierten Bindungsassays, hochpräzisen Biosensor-Messungen und Infektionstests mit harmlosen „Pseudoviren“ fanden sie ein klares Muster. Die RBD von BANAL-52 band am stärksten an das ACE2 einer Fledermausart, Rhinolophus sinicus, und etwas weniger stark an menschliches ACE2. Die RBD von SARS-CoV-2 zeigte dagegen eine leichte Präferenz für menschliches ACE2 gegenüber fledermauslichem ACE2. Insgesamt hielt die RBD von BANAL-52 sowohl an Fledermaus- als auch an menschlichen Rezeptoren fester als die von SARS-CoV-2, war aber am feinsten auf jenes bestimmte fledermausliche ACE2 abgestimmt.
Wie eine atomare Feinabstimmung das Gleichgewicht kippt
Das Team wandte sich dann der Röntgenkristallographie zu, die Strukturen auf atomarer Ebene zeigt, um genau zu sehen, wie der virale „Finger“ und der ACE2-„Türknauf“ in Kontakt treten. Sie fokussierten zwei Schlüsselpositionen: eine auf der viralen RBD (Residue 498 genannt) und eine auf ACE2 (Residue 41). Bei BANAL-52 verwenden sowohl die virale Stelle als auch die fledermausliche ACE2-Stelle dasselbe Baustein-Aminosäure, Histidin, was eine sehr enge, geschichtete Interaktion ermöglicht – ein Stapeln wie zwei Münzen und zusätzlich eine Wasserstoffbrückenbindung. Im menschlichen ACE2 befindet sich an derselben Position eine verwandte, aber leicht unterschiedliche Aminosäure, Tyrosin, die weiterhin gut mit BANAL-52s Histidin stapelt, jedoch die zusätzliche Wasserstoffbrücke nicht bietet. SARS-CoV-2 dagegen nutzt an dieser viralen Position Glutamin, das nicht auf die gleiche Weise stapeln kann und daher zu schwächerer Bindung an sowohl fledermausliches als auch menschliches ACE2 führt. Durch gezielten Austausch dieser Aminosäuren in fledermauslichem ACE2 bestätigten die Forschenden, dass das Stärken oder Abschwächen dieses einen Kontaktpunkts umschlagen kann, welche Virus- oder Wirtstypen bevorzugt werden.
Warum menschliches ACE2 so einladend ist
Über diesen einen Kontakt hinaus fragten die Autorinnen und Autoren, weshalb menschliches ACE2 generell ein so effizienter Zugangspunkt für Coronaviren ist. Beim direkten Vergleich von Fledermaus- und menschlichem ACE2 identifizierten sie mehrere menschspezifische Merkmale, die den viralen Händedruck verbessern. Zwei Positionen im menschlichen ACE2, besetzt mit den Aminosäuren Histidin (an Stelle 34) und Methionin (an Stelle 82), erzeugen stärkere Wasserstoffbrücken und hydrophobe „Flecken“, die der viralen RBD ein stabileres Einrasten ermöglichen. Eine weitere menschliche Restgruppe, Threonin an Position 27, schwächt die Bindung etwas gegenüber der Fledermausversion, aber insgesamt überwiegen die zusätzlichen günstigen Kontakte. Diese Details passen zu früheren Arbeiten, die zeigten, dass menschliches ACE2 mehrere „Hotspots“ besitzt, die es zu einem attraktiven Rezeptor für eine breite Palette von Coronaviren machen.
Die Ursprungsfrage neu einordnen
Setzt man alle Daten zusammen, argumentiert die Studie, dass SARS-CoV-2 und seine fledermauslichen Verwandten weiterhin dem üblichen evolutionären Muster folgen. Der Spike von BANAL-52 scheint am besten an ACE2 bestimmter Fledermäuse angepasst zu sein, ist aber zugleich mit menschlichem ACE2 kompatibel. Der Spike von SARS-CoV-2 wiederum ist besser auf menschliches ACE2 abgestimmt als auf fledermausliches ACE2, unterstützt durch spezielle Kontaktpunkte am menschlichen Rezeptor. Kleine Änderungen an nur wenigen Positionen – insbesondere am viralen Residue 498 und benachbarten Stellen – können das Gleichgewicht verschieben, welche Wirte bevorzugt werden. Für Nicht-Fachleute lautet die Schlussfolgerung: Es ist nicht nötig, exotische Erklärungen heranzuziehen; gut verstandene, standardmäßige strukturelle Prinzipien der Protein–Protein-Interaktion reichen aus, um zu erklären, wie diese Viren Fledermaus- und menschliche Zellen erkennen, und sie stützen eine enge evolutionäre Verbindung zwischen SARS-CoV-2 und verwandten Fledermaus-Coronaviren.
Zitation: Hsueh, FC., Shi, K., Aihara, H. et al. Structural basis for bat receptor recognition by SARS-CoV-2 and bat SARS2-like coronaviruses. Commun Biol 9, 398 (2026). https://doi.org/10.1038/s42003-026-09682-z
Schlüsselwörter: SARS-CoV-2 Evolution, Fledermaus-Coronaviren, ACE2-Rezeptor, Wirtsspektrum von Viren, Bindung des Spike-Proteins