Clear Sky Science · de
Von Afrikanischer Schweinepest codiertes Protein MGF 505–3R beeinträchtigt die angeborene Immunität durch ubiquitinvermittelte Degradation von MyD88
Warum das für Tiergesundheit und darüber hinaus wichtig ist
Die Afrikanische Schweinepest hat Schweinebestände weltweit verwüstet, bedroht die Nahrungsmittelversorgung und verursacht enorme wirtschaftliche Schäden. Das für die Krankheit verantwortliche Virus ist tödlich, unter anderem weil es die frühen Warnsysteme des Körpers umgeht. Diese Studie zeigt, wie ein virales Protein namens MGF 505–3R gezielt einen wichtigen Alarmschalter in Zellen sabotiert, und demonstriert, dass ein winziger Abschnitt dieses Proteins in Mäusen auch als wirksames antientzündliches Mittel genutzt werden kann.
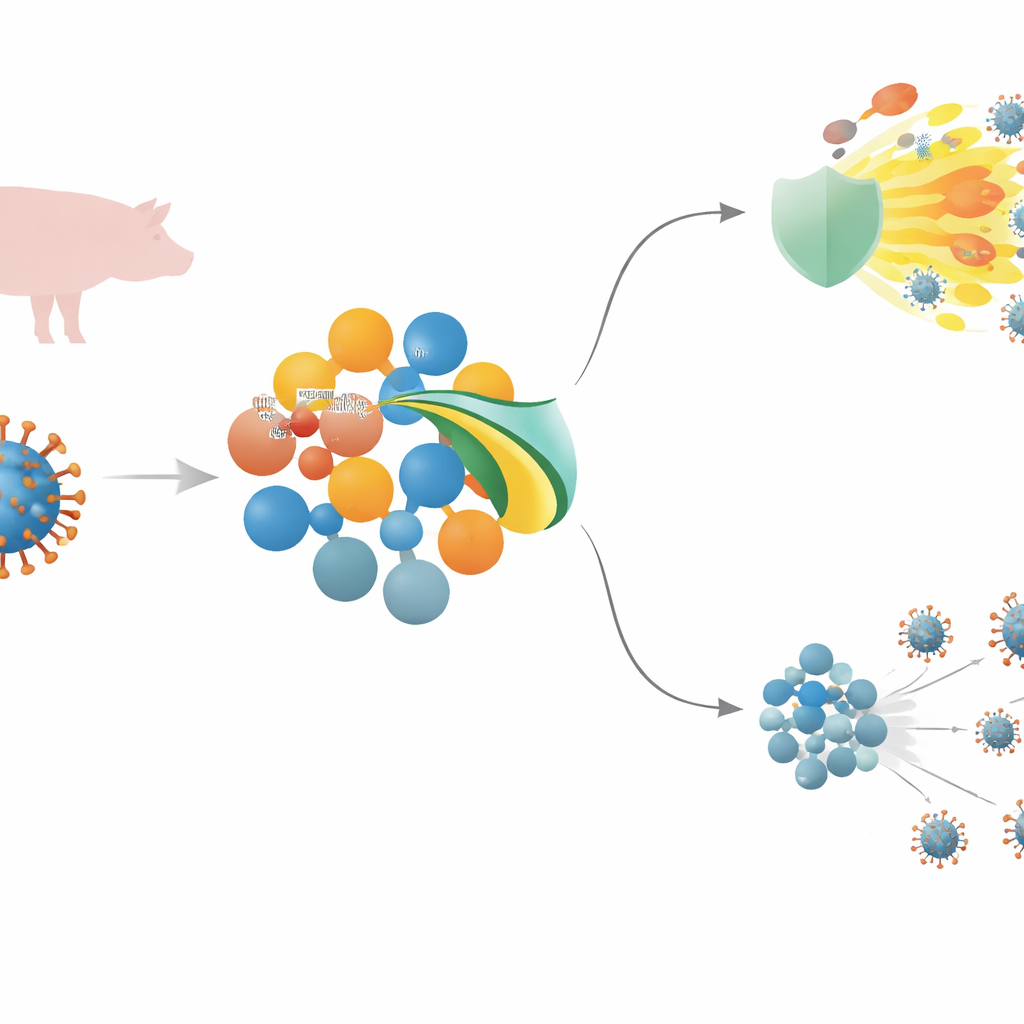
Ein tödliches Schweinevirus und die erste Verteidigungslinie des Körpers
Das Afrikanische Schweinepestvirus (ASFV) ist ein großes DNA‑Virus, das nahezu jedes infizierte Schwein töten kann. Um Fuß zu fassen, muss es die angeborene Immunität überlisten — die rasche, vorderste Verteidigung, die Eindringlinge erkennt und Entzündungen sowie antivirale Moleküle auslöst. Zentral für diese Reaktion ist eine Signalkette, zu der Sensoren auf der Zelloberfläche, das Relay‑Protein MyD88 und ein Hauptschalter namens NF–κB gehören, die gemeinsam die Produktion entzündlicher Botenstoffe und antiviraler Interferone antreiben. ASFV trägt viele Gene, denen man eine Störung dieser Signale zuschreibt, doch bei mehreren davon, einschließlich MGF 505–3R, waren die genauen Mechanismen bislang unklar.
Wie das Virus die Drähte des Immunalarms durchtrennt
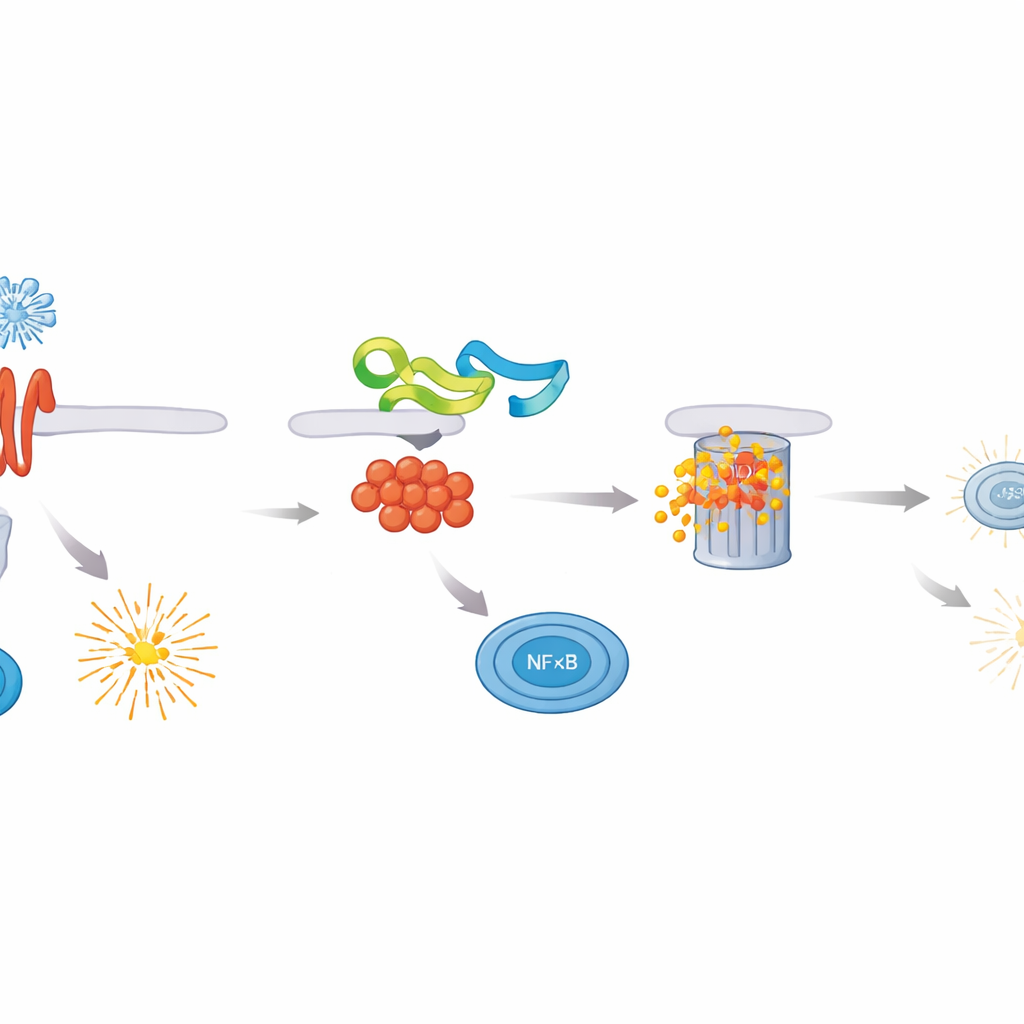
Die Forscher durchsuchten ASFV‑Proteine auf ihre Fähigkeit, die NF–κB‑Aktivität zu dämpfen, und fanden, dass MGF 505–3R ein besonders starker Inhibitor ist. In Anwesenheit dieses viralen Proteins produzierten Zellen, die unterschiedlichen Immunreizen ausgesetzt waren, deutlich weniger entzündliche Zytokine und wesentlich geringere Mengen an Typ‑I‑ und Typ‑III‑Interferonen. Genauere Untersuchungen zeigten, dass MGF 505–3R direkt auf MyD88 wirkt, den zentralen Adapter, der viele Immunsensoren mit NF–κB verbindet. MGF 505–3R bindet MyD88 und markiert es für den Abbau durch die zellulären Protein‑Vernichtungsmechanismen mittels einer Form der Kennzeichnung, der K48‑verknüpften Ubiquitinierung. Wenn MyD88 abgebaut wird, gelingt NF–κB nicht der Transport in den Zellkern und das Einschalten schützender Gene, wodurch Zellen für Virusvermehrung empfänglicher werden.
Fokussiert auf ein winziges, aber kraftvolles Proteinfragment
Um den entscheidenden Teil von MGF 505–3R zu identifizieren, erzeugte das Team verkürzte Versionen des Proteins und prüfte deren Wirkung. Sie fanden heraus, dass die Aminosäuren 89–277 sowohl notwendig als auch ausreichend sind, um MyD88 zu binden, dessen Ubiquitinierung zu fördern und die NF–κB‑Aktivierung zu blockieren. Mit Hilfe von Computervorhersagen zur Proteinfaltung schnitten sie aus diesem Bereich zwei kurze Peptide heraus. Eines davon, pep3R–1, hob sich deutlich ab: Es verringerte scharf die NF–κB‑Aktivität, blockierte die Phosphorylierung und den Kerntransport der NF–κB‑Untereinheit p65 und senkte die Expression entzündlicher Zytokine und Interferone in Immunzellen, die mit verschiedenen Gefahrensignalen stimuliert wurden. In Zellkulturen dämpften sowohl das vollständige MGF 505–3R als auch pep3R–1 nicht nur antivirale Signalwege, sondern ermöglichten auch einer Test‑Viruslinie eine effizientere Replikation, was die Kraft dieses Mechanismus zur Kontrolle von Infektionen unterstreicht.
Ein viraler Trick als mögliche Therapie
Die Forscher fragten dann, ob das Peptid nicht genutzt werden könnte, um schädliche Entzündungen zu beruhigen, statt Viren zu unterstützen. In einem Mausmodell für durch das Chemikalium DSS ausgelöste Colitis verlieren die Tiere normalerweise Gewicht, entwickeln blutigen Durchfall und zeigen schwere Schäden sowie Infiltration von Immunzellen im Darm. Mit pep3R–1 behandelte Mäuse kamen deutlich besser davon: Die Krankheitswerte waren niedriger, die Därme länger und gesünder, und die mikroskopische Untersuchung zeigte erhaltene Gewebestrukturen mit deutlich weniger entzündlichen Zellen. Die Spiegel wichtiger Entzündungsmoleküle wie TNF‑α, IL‑1β, IL‑6 sowie eines Enzyms, das mit dem Einstrom weißer Blutkörperchen assoziiert ist, waren im Darmgewebe und Blut reduziert. In einem weiteren Experiment verringerte pep3R–1 auch die entzündliche Reaktion auf ein systemisches bakterielles Toxin, was darauf hinweist, dass es sowohl lokale als auch den gesamten Organismus betreffende Entzündungsstürme abschwächen kann.
Was das für Schweine, Menschen und zukünftige Behandlungen bedeutet
Diese Arbeit zeigt, dass das ASFV‑Protein MGF 505–3R dem Virus hilft, indem es das zentrale Immunrelay MyD88 demontiert und damit sowohl entzündliche als auch Interferon‑Verteidigungen ausschaltet. Gleichzeitig lässt sich ein kleines Fragment dieses viralen Proteins, pep3R–1, umwidmen, um in Mäusen übermäßige Entzündungen sicher zu dämpfen, etwa in einem Darmkrankheitsmodell. Zwar ist noch viel zu tun — etwa Stabilität und Verabreichung zu verbessern und Tests in weiteren Krankheitskontexten durchzuführen — doch die Studie legt sowohl eine kritische Schwachstelle offen, die antivirale Strategien anvisieren könnten, als auch einen vielversprechenden Entwurf für die Entwicklung neuer peptidbasierter antientzündlicher Wirkstoffe, inspiriert von viraler Immunumgehung.
Zitation: Liu, H., Sun, L., Wang, F. et al. African swine fever virus–encoded protein MGF 505–3R impairs innate immunity via ubiquitin–mediated degradation of MyD88. Commun Biol 9, 407 (2026). https://doi.org/10.1038/s42003-026-09681-0
Schlüsselwörter: Afrikanische Schweinepest, angeborene Immunität, NF-kappaB, MyD88, antientzündliches Peptid