Clear Sky Science · de
Das ZIKV-Hüllenprotein blockiert stark die frühe gerichtete Differenzierung in der neuronalen Linie
Warum das für wachsende Gehirne wichtig ist
Das Zika-Virus sorgte zunächst dafür, dass Babys mit ungewöhnlich kleinen Köpfen und schweren Hirnschäden geboren wurden. Aber wie kann eine Infektion im Mutterleib so wirkungsvoll die frühesten Schritte des Gehirnbaus beim Embryo entgleisen lassen? Diese Studie konzentriert sich auf eine einzelne virale Komponente – das Hüllenprotein, das Zika-Partikel umgibt – und fragt, ob dieses Protein allein die Bildung von Nervenzellen fehlleiten kann. Indem die Forschenden die frühe Gehirnentwicklung im Labor mit Stammzellen von Mäusen nachbilden, decken sie auf, wie dieses virale Protein leise, aber kräftig die normale Entstehung neuronaler Schaltkreise blockiert.
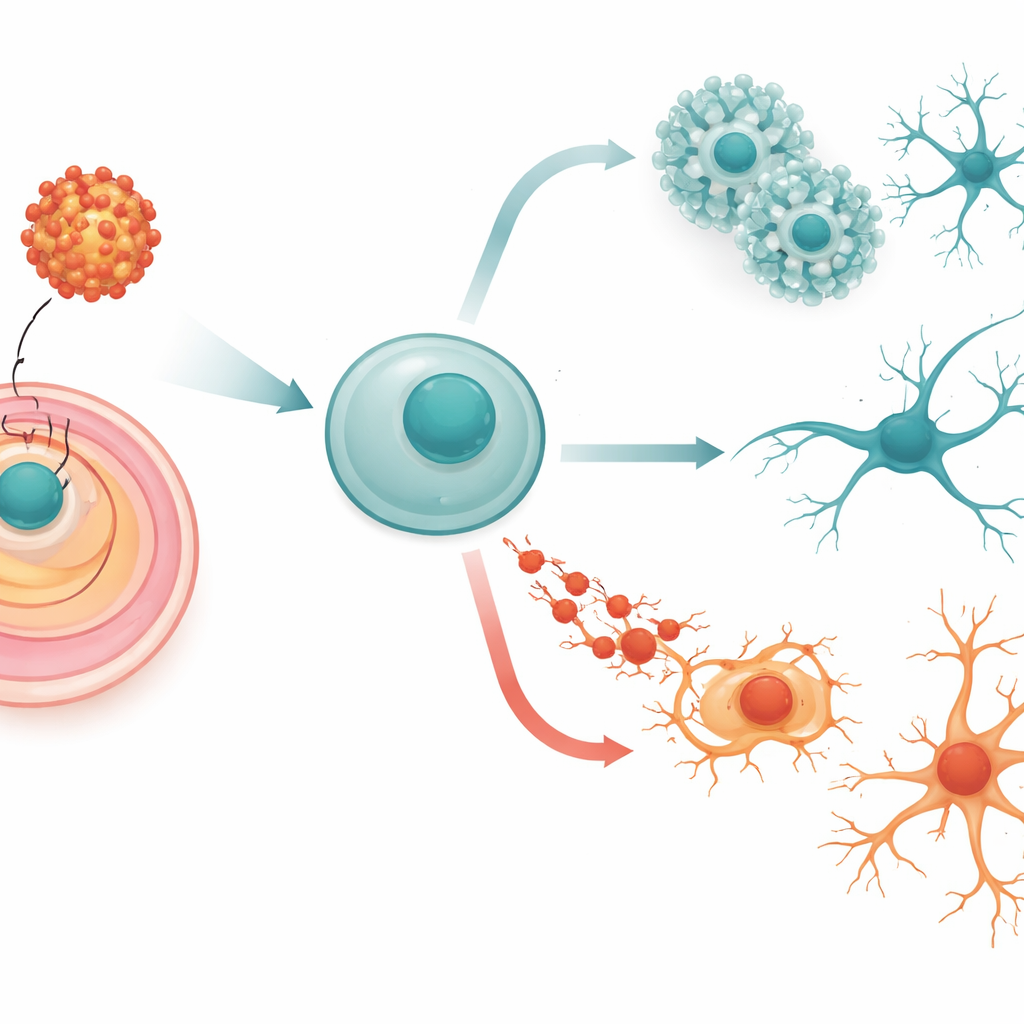
Von flexiblen Starterzellen zu zukünftigen Nervenzellen
Unser Gehirn beginnt als ein Gefüge einfacher, hochflexibler Zellen, so genannter embryonaler Stammzellen. Diese Zellen können sich in jedes Gewebe des Körpers verwandeln, folgen unter geeigneten Bedingungen jedoch einem genau choreografierten Pfad zur Nervenzellenbildung. Zuerst verpflichten sie sich zur „neuralen“ Richtung, dann bilden sie rosettenähnliche Strukturen, die dem frühen Nervensystem ähneln, und schließlich reifen sie zu Neuronen heran, die sich über lange, verzweigende Fortsätze verbinden. Das Team verwendete murine embryonale Stammzellen als Modell für diese frühen Stadien und brachte sie so zum Ausdruck, dass sie das Zika-Hüllenprotein produzierten, entweder mit oder ohne eine kleine Veränderung an einer Schlüsselstelle für Glykosylierung, von der bekannt ist, dass sie die Virusstärke beeinflusst.
Virale Hülle friert die ersten Schritte des Gehirnbaus ein
Wenn die Stammzellen das Zika-Hüllenprotein produzierten, wirkten sie weiterhin gesund und behielten ihre breite Potenz, sich in verschiedene Gewebe zu entwickeln. Erlaubte man ihnen jedoch, sich frei zu differenzieren, war ihre Fähigkeit, komplexe 3D-Aggregate zu bilden, die die drei grundlegenden Keimblätter des Embryos repräsentieren, stark reduziert, und Marker aller drei Schichten gingen zurück. Das deutet darauf hin, dass das virale Protein die Stammzellen nicht direkt abtötet, sondern subtil ihre Fähigkeit beeinträchtigt, normale Entwicklungswege einzuschlagen. Eine mutierte Version des Proteins, der eine spezifische Zuckerbindung fehlt, veränderte dieses Muster auf eine ungleichmäßigere Weise, was darauf hindeutet, dass die feine chemische Modifikation des Proteins bestimmt, wie es die Entwicklung stört.
Blockade des Wegs von der Stammzelle zum Neuron
Die Forschenden richteten den Fokus dann gezielt auf den Übergang von der Stammzelle zum frühen Neuron und nutzten dafür zwei etablierte Labor‑Modelle: eine flache „Monolayer“-Kultur und eine 3D‑„Neurosphären“-Kultur, die frühes Hirngewebe nachahmt. In beiden Systemen zeigten Kontrollzellen über Tage hinweg einen gleichmäßigen Anstieg der Expression von Markern für neurale Stammzellen und Neuronen, bildeten organisierte Rosetten und zahlreiche junge Neuronen. Zellen, die das Hüllenprotein produzierten, hingegen erzeugten deutlich weniger neurale Stammzellen, weniger Rosetten und wesentlich weniger frühe Neuronen, was sich in reduzierten Levels wichtiger Gene und Proteine mit Nervenzellidentität niederschlug. Die glycosylierungsfreie Mutante verursachte auf Geneebene allgemein eine noch stärkere Blockade und aktivierte zusätzlich entzündliche Wege des programmierten Zelltods, was auf einen Mechanismus für schwerwiegendere Schäden hinweist.
Stummschaltung der Kommunikation in jungen neuronalen Netzwerken
Um zu verstehen, was in den Zellen schieflief, verglich das Team die globale Genaktivität in normalen und Hüllen-produzierenden Zellen in kritischen Differenzierungsstadien. Sie stellten fest, dass viele Gene, die mit Nervenwachstum, Synapsenbildung und den feinen Dornfortsätzen an Dendriten zusammenhängen, die Erinnerungen speichern, herunterreguliert waren. Signalwege, die am Beladen und Freisetzen von Neurotransmittern, am Verknüpfen von Axonen mit ihren Zielen und am Zusammenbau von Synapsen beteiligt sind, waren durchweg unterdrückt. Gleichzeitig waren Signalrouten im Zusammenhang mit Calcium und bestimmten Zelloberflächenrezeptoren aktiviert, was die Zellen potenziell übererregbar oder fehlgesteuert machen könnte. Diese weitreichenden Veränderungen zeigten sich sowohl in flachen als auch in 3D‑Kulturen und machen deutlich, dass das Hüllenprotein wiederholt sich entwickelnde neuronale Zellen davon abhält, robuste, gut vernetzte Netzwerke aufzubauen.
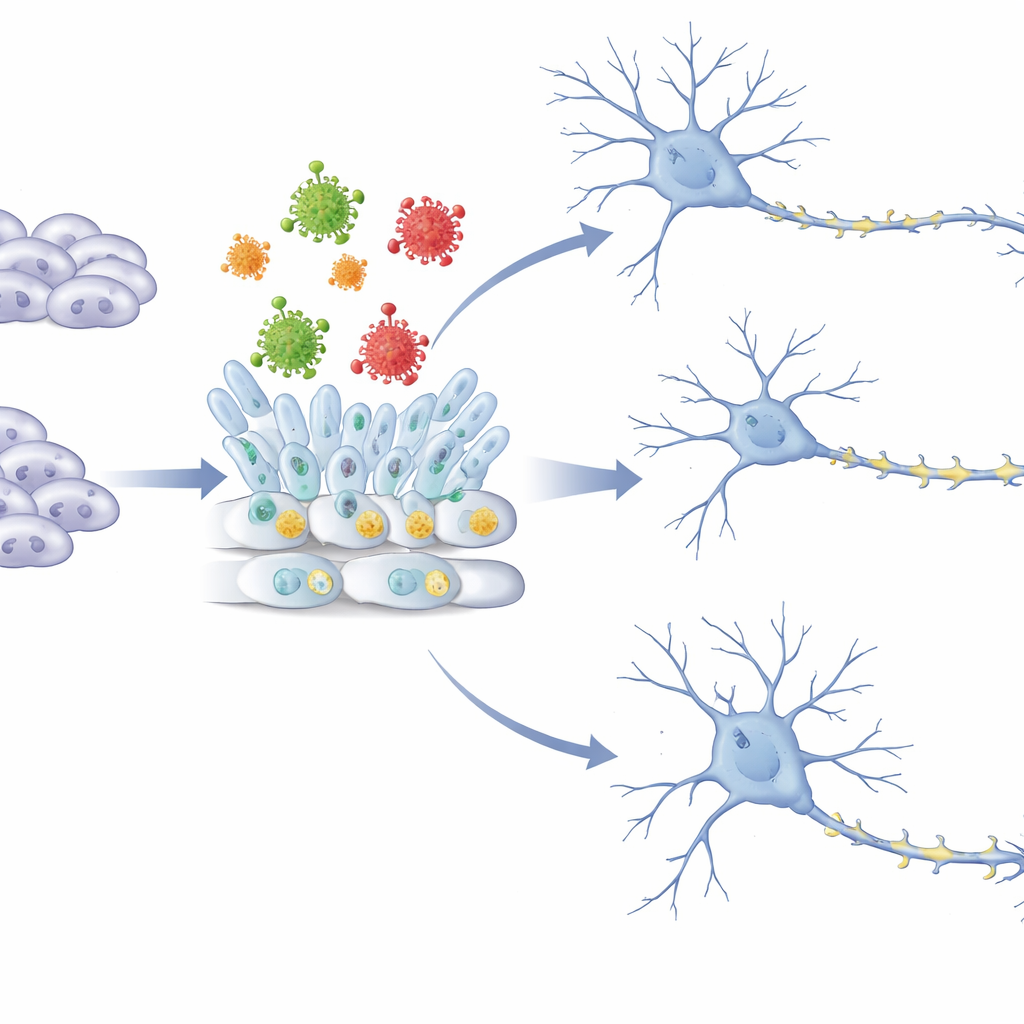
Was das für Zika‑assoziierte Geburtsfehler bedeutet
Für Nicht‑Spezialisten lautet die Kernbotschaft: Das Zika‑Virus muss nicht aktiv replizieren und Zellen abtöten, um das sich entwickelnde Gehirn zu schädigen. Diese Arbeit zeigt, dass sein äußeres Hüllenprotein allein frühe Stammzellen von dem normalen Weg zum Neuron abdrängen kann und die genetischen Programme schwächt, die für die Bildung gesunder Synapsen und dendritischer Dornfortsätze nötig sind. Solch frühe, stille Störungen tragen dazu bei zu erklären, wie eine Exposition während der Schwangerschaft zu Zuständen wie Mikrozephalie und langfristigen kognitiven Problemen führen kann. Die Ergebnisse mahnen zudem, dass Impfstoffe oder Therapien, die Hüllenproteine verwenden, sorgfältig auf mögliche Auswirkungen auf die Gehirnentwicklung geprüft werden müssen, selbst wenn kein lebender Erreger vorhanden ist.
Zitation: Ma, ZH., Wang, Y., Hassaan, N.A. et al. ZIKV envelope protein is a strong blocker of early directional differentiation in the neural lineage. Commun Biol 9, 395 (2026). https://doi.org/10.1038/s42003-026-09672-1
Schlüsselwörter: Zika-Virus, Gehirnentwicklung, neurale Stammzellen, virales Hüllenprotein, Mikrozephalie