Clear Sky Science · de
Der Kern-Zellzyklus-Transkriptionsfaktor TOC1 bindet direkt an Promotoren von Abwehrgenen und reguliert die Immunität in Arabidopsis
Pflanzen im täglichen Verteidigungsrhythmus
Pflanzen können nicht vor Krankheitserregern fliehen und sind daher auf fein abgestimmte Abwehrsysteme angewiesen. Diese Studie zeigt, dass ein Teil der inneren Tagesuhr der Pflanze, ein Protein namens TOC1, mehr tut als nur die Zeit zu messen. Es bestimmt auch, wann Pflanzen besonders verwundbar oder besonders resistent gegenüber einem verbreiteten Grauschimmelpilz sind, und hilft so zu erklären, warum die Tageszeit den Verlauf einer Infektion beeinflussen kann.
Warum die Tageszeit das Infektionsrisiko ändert
Die Forschenden arbeiteten mit Arabidopsis, einer kleinen Senfpflanze, die als Modellorganismus weit verbreitet ist, und dem Pilz Botrytis cinerea, der viele Kulturen befällt. Frühere Arbeiten zeigten, dass Pflanzen rund um die Morgendämmerung generell widerstandsfähiger gegen diesen Pilz sind und nachts anfälliger. Hier konzentrierte sich das Team auf TOC1, ein zentrales Uhrprotein, das normalerweise am Abend seinen Höhepunkt erreicht, um zu prüfen, ob es diesen Tag–Nacht-Wechsel der Krankheitsresistenz direkt steuert.
Uhrprotein, das pflanzliche Abwehrkräfte abschwächt
Mithilfe von Pflanzen, die zu viel TOC1 produzierten, und von Mutanten ohne TOC1 infizierten die Autorinnen und Autoren Blätter entweder zur subjektiven Morgendämmerung oder zur Nacht unter konstantem Licht sowie unter normalen Licht–Dunkel-Zyklen. Bei normalen Pflanzen hing die Größe der Läsionen — das durch den Pilz verursachte abgestorbene Gewebe — stark vom Infektionszeitpunkt ab. Im Gegensatz dazu verloren sowohl TOC1-überexprimierende als auch TOC1-lackierende Pflanzen diese tägliche Schwankung. Pflanzen mit überschüssigem TOC1 verharrten in einem sehr anfälligen Zustand, während Pflanzen ohne TOC1 so reagierten, als wären sie in ihrem widerstandsfähigsten Zustand gefangen. Dieses Muster zeigt, dass TOC1 als Bremse der Immunität wirkt: mehr TOC1 bedeutet schwächere Abwehr, besonders wenn das Protein am Abend normalerweise hoch ist.
Abwehrgene bereits vor dem Angriff bereit
Um zu verstehen, was TOC1 innerhalb der Zelle bewirkte, verglich das Team die Aktivität von Tausenden Genen in normalen und TOC1-losen Pflanzen, jeweils mit und ohne Infektion. Schon bevor ein Pilz eintraf, zeigten die Mutanten ohne TOC1 eine fehlerhafte Expression von Hunderten Genen, die mit Stress und Abwehr verbunden sind. Viele dieser Gene trugen kurze DNA-Motive, die TOC1 zu erkennen bekannt ist, was nahelegt, dass es normalerweise an deren Kontrollregionen sitzt und sie herunterreguliert. Wichtige Regulatoren von Hormonwegen, die an der Abwehr beteiligt sind — insbesondere solche, die durch Jasmon- und Ethylen-Signale gesteuert werden — waren in Abwesenheit von TOC1 aktiver, was eine molekulare Erklärung für die erhöhte Resistenz der Mutanten liefert.
Wie TOC1 und MYC2 dieselben Schalter teilen
Die Geschichte wird auf der Ebene einzelner Abwehrschalter im Genom komplexer. Die Autorinnen und Autoren betrachteten mehrere verteidigungsbezogene Transkriptionsfaktoren — ERF4, ORA47, ORA59 und WRKY33 — deren Promotoren ein gemeinsames DNA-Motiv namens G-Box enthalten. Dieses Motiv wird auch von einem anderen Protein, MYC2, erkannt, einem zentralen Akteur in der Jasmonat-Signalgebung. Mit chromatinimmunpräzipitierenden Experimenten zeigten sie, dass TOC1 in gesunden Pflanzen physisch diese G-Box-Regionen besetzt, was zu seiner Rolle passt, Abwehrgene zu dämpfen. Nach einer Pilzinfektion verschwand TOC1s Bindung an diese Promotoren größtenteils, während MYC2 gebunden blieb. Wenn MYC2 genetisch entfernt wurde, nahm die TOC1-Bindung in gesunden Pflanzen ab und, entscheidend, TOC1 wurde nach einer Infektion nicht mehr freigesetzt. Gleichzeitig fiel die Expression der nachgeschalteten Abwehrregulatoren. Zusammen deuten diese Ergebnisse darauf hin, dass MYC2 hilft, TOC1 an Abwehrgene zu rekrutieren und es infektionsabhängig wieder zu verdrängen.
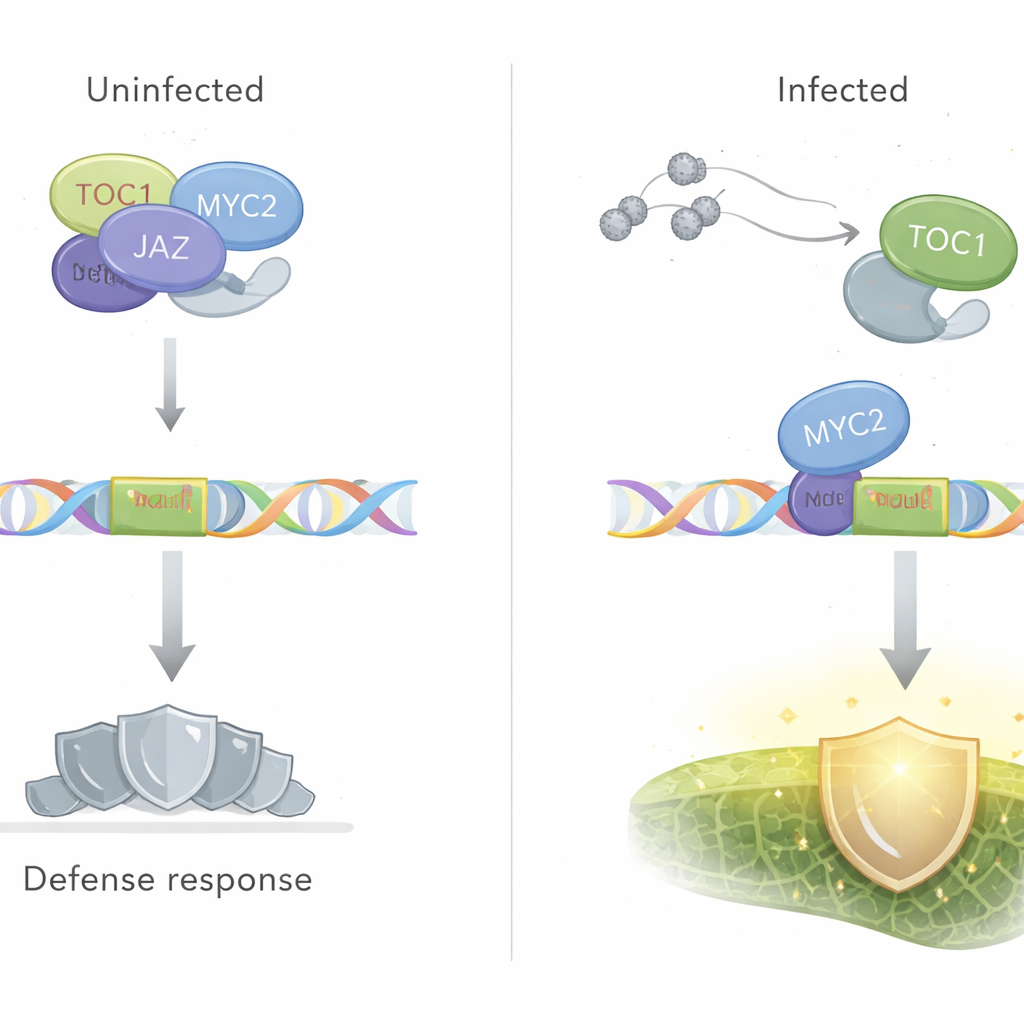
Uhrgesteuerte Immunität im Alltag
Setzt man diese Teile zusammen, schlagen die Autorinnen und Autoren vor, dass die Pflanzenuhr und die Hormon-Signalweiterleitung ein gemeinsames Bedienfeld für die Immunität bilden. Über einen 24-Stunden-Zyklus steigen die TOC1-Spiegel am Abend an, und mit Unterstützung von MYC2 sitzt TOC1 auf G-Box-Motiven in Abwehrgenen und dämpft deren Aktivität, wodurch ein tägliches "Tor" entsteht, das das Zeitfenster starker Abwehr verengt. Wenn ein Pathogen erkannt wird und die Jasmonatspiegel ansteigen, ändert MYC2 sein Verhalten, TOC1 wird von diesen DNA-Stellen freigesetzt und die Bremse der Abwehr wird aufgehoben, sodass die Pflanzen eine akute Reaktion starten können, unabhängig von der Tageszeit. Für eine allgemeine Leserschaft ist die Kernaussage, dass die Stärke der pflanzlichen Immunität nicht konstant ist: Sie wird von der inneren Uhr geplant, und TOC1 ist eine zentrale Zeitkomponente, die direkt die Schalter wichtiger Abwehrgene umlegt.
Zitation: Sparks, SL., Roden, L.C. & Ingle, R.A. The core clock transcription factor TOC1 binds directly to defence gene promoters regulating immunity in Arabidopsis. Commun Biol 9, 402 (2026). https://doi.org/10.1038/s42003-026-09667-y
Schlüsselwörter: pflanzliche circadiane Uhr, Arabidopsis-Immunität, Botrytis cinerea, Jasmonat-Signalübertragung, Transkriptionsfaktoren