Clear Sky Science · de
Aktivierung des von Cytomegalovirus kodierten G‑Protein‑gekoppelten Rezeptors UL33 durch ein angeborenes N‑terminales Peptid
Wie ein verbreitetes Virus unsere Zellen umprogrammiert
Das humane Cytomegalovirus (HCMV) infiziert stillschweigend den Großteil der Menschen und bleibt meist unbemerkt. Bei Neugeborenen, Transplantatempfängern und anderen mit geschwächtem Immunsystem kann es jedoch schwere Erkrankungen verursachen. Diese Studie zeigt im molekularen Detail, wie ein virales Protein namens UL33 wie ein eingebauter Schalter wirkt, der infizierte Zellen dauerhaft zugunsten des Virus verstellt. Das Verständnis dieses verborgenen Schalters hilft zu erklären, wie HCMV lebenslang persistiert, und weist auf neue Wege hin, es zu deaktivieren, ohne die normale Zell‑Signalübertragung zu stören.
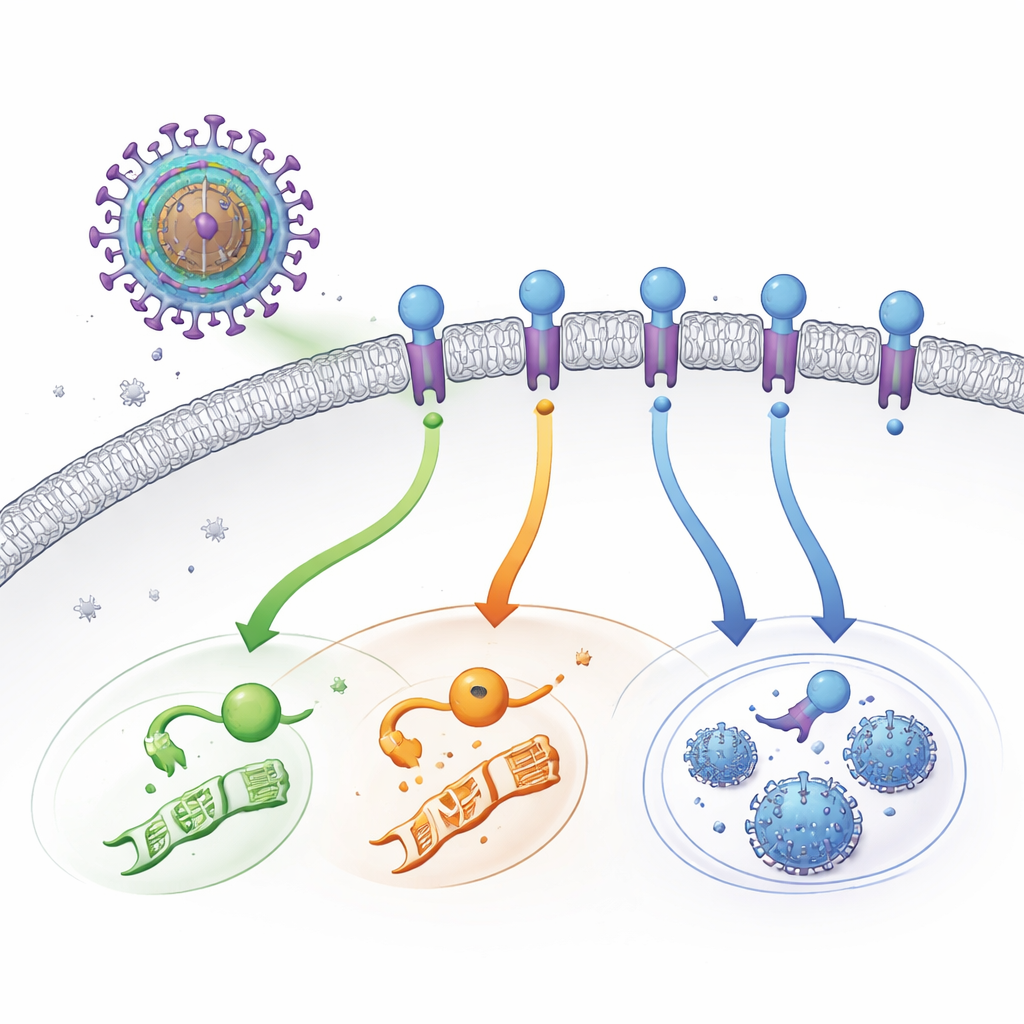
Ein heimlicher viraler Schalter an der Zelloberfläche
HCMV trägt eigene Versionen von Zelloberflächenrezeptoren — Proteine, die normalerweise Hormone oder Immun‑Signale wahrnehmen. UL33 ist einer dieser viralen Rezeptoren. Anders als typische Rezeptoren, die auf ein äußeres Signal warten, ist UL33 „ständig an“. Sobald es in die äußere Membran einer infizierten Zelle eingebaut ist, kann es gleichzeitig mehrere der wichtigsten Kommunikationswege der Zelle anzapfen. Diese Wege steuern Prozesse wie Genaktivität, Stoffwechsel und die Entscheidung, ob die Zelle in einen Ruhezustand geht oder neue Viren produziert. Jahrelang war bekannt, dass UL33 aktiv ist, doch unklar blieb, was es einschaltet, zumal nie ein externes aktivierendes Molekül (Ligand) gefunden worden war.
Ein Selbststarter: Der Rezeptor, der seinen eigenen Schlüssel mitbringt
Mithilfe hochauflösender Kryo‑Elektronenmikroskopie hielten die Autoren dreidimensionale Momentaufnahmen von UL33 in Komplex mit einem der zellulären Signalisierungspartner, einem G‑Protein namens Gs, fest. Die Bilder zeigen, dass der allererste Abschnitt des UL33‑Proteins — sein kurzer N‑terminaler Schwanz — zurückgefaltet in eine Tasche des Rezeptors selbst hineinragt, ähnlich einem dauerhaft im Schloss steckenden Schlüssel. Dieser "verankerte" Schwanz liegt in einer kleinen Seitenkammer, die bei verwandten menschlichen Rezeptoren normalerweise einen Teil eines Immun‑Signalmoleküls, einer Chemokin‑Domäne, aufnehmen würde. Indem er diese Tasche von vornherein belegt, verhindert UL33, dass äußere Chemokine überhaupt binden, was erklärt, warum es als „Waisenrezeptor“ gilt, der nicht auf die normalen Botenstoffe des Wirts reagiert.
Entscheidende Atome im viralen Einschaltmechanismus
Um zu bestätigen, dass dieser eingebaute Schwanz tatsächlich der Auslöser ist, veränderte das Team systematisch einzelne Bausteine von UL33 in menschlichen Zellen. Sie konzentrierten sich auf die ersten Aminosäuren des Schwanzes und auf passende Stellen in der Tasche, die ihn fassen. Wenn sie diese Schlüsselreste gegen neutralere Aminosäuren austauschten oder einen davon ganz entfernten, sank die Signalfähigkeit von UL33 nahezu auf null — obwohl die veränderten Rezeptoren weiterhin in normaler Menge an der Zelloberfläche erschienen. Mit anderen Worten: Das Protein war vorhanden, aber stumm. Das zeigt, dass der Schwanz nicht nur eine strukturelle Zier ist, sondern das essentielle selbstaktivierende Element, das UL33 eingeschaltet hält.
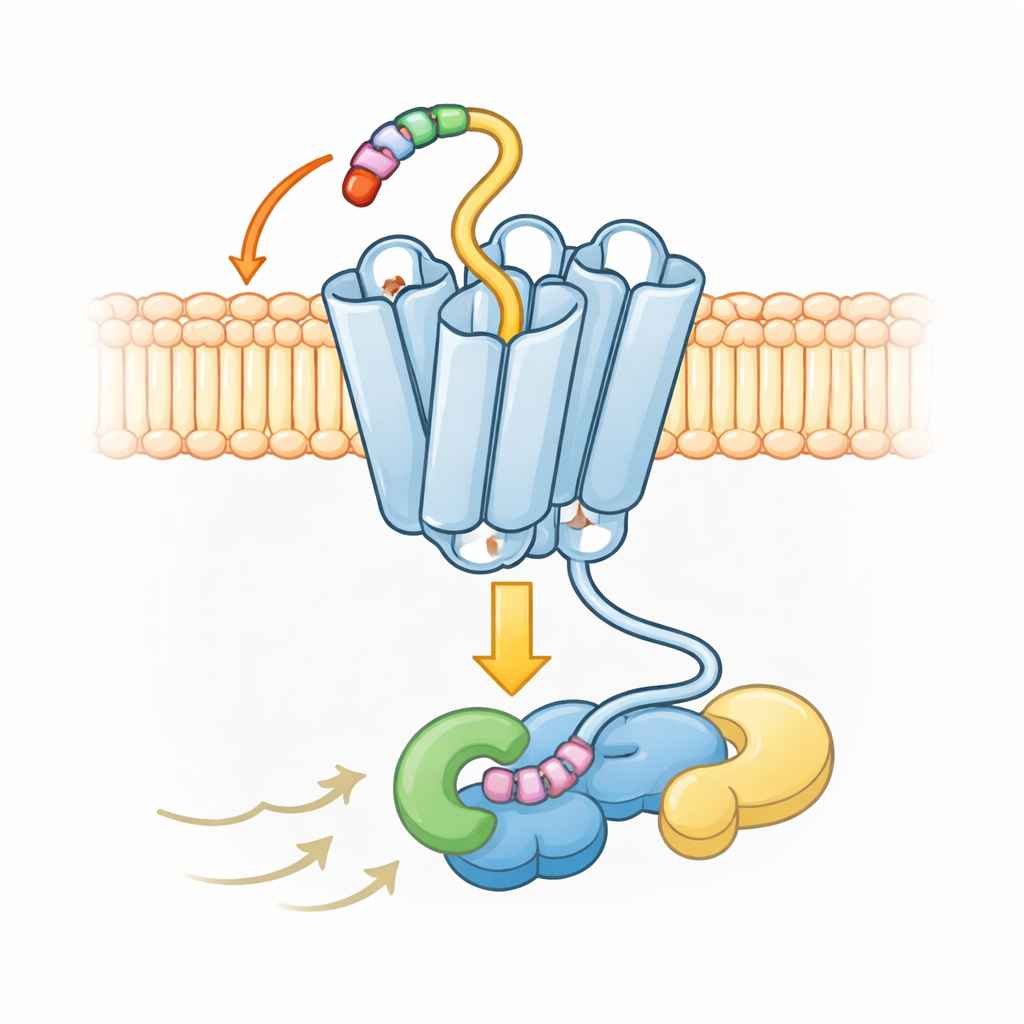
Eine ungewöhnliche Form für breite, aber kontrollierte Signalübertragung
Die Strukturkarten zeigen außerdem, dass UL33 eine etwas andere aktive Form annimmt als typische menschliche Rezeptoren. Bei den meisten Rezeptoren dieser Familie schwingt eine der sieben Helices nahe der Zellinnenseite bei Aktivierung deutlich nach außen und öffnet eine große Höhlung, in der G‑Proteine andocken. Bei UL33 bleibt diese Helix viel näher zur Mitte und schafft so eine engere Passform. Trotzdem kann UL33 mehrere Arten von G‑Proteinen — Gs, Gq und Gi — binden, indem es präzise Kontakte mit der Spitze des G‑Proteins herstellt, die in den Rezeptor einschiebt. Diese Kontakte begünstigen bestimmte G‑Proteine und schließen andere, wie die Gruppe G12/13, aus, sodass das Virus die Reaktionen der Zelle gezielt verzerren kann, ohne unkontrollierte Signale auszulösen.
Neue Verwundbarkeiten für ein altes Virus
Durch die Kombination von Strukturaufnahmen mit funktionellen Tests zeichnet die Studie ein klares Bild: UL33 ist ein selbststartender viraler Rezeptor, dessen eigener Schwanz als dauerhaft angehefteter Aktivator fungiert. Dieses Prinzip erlaubt es HCMV, die Signalkaskaden der Wirtszelle sanft, aber dauerhaft zu justieren, um die Virusreplikation und Reaktivierung zu fördern, insbesondere durch die Aktivierung von Signalwegen, die virale Gene einschalten. Gleichzeitig macht die Arbeit Schwachstellen sichtbar, die von Medikamenten ausgenutzt werden könnten, etwa ein enger Tunnel, der zur Tasche führt, in der der Schwanz sitzt. Moleküle, die sich in diesem Bereich verkeilen oder den Schwanz verdrängen, könnten UL33 beruhigen und den viralen Schaden verringern, während die normalen Rezeptoren des Körpers verschont blieben. Für Patienten mit HCMV‑Risiko könnte das gezielte Ansteuern dieses viralen „Hauptschalters“ eines Tages eine präzisere Möglichkeit bieten, das Virus in Schach zu halten.
Zitation: Drzazga, A.K., Suzuki, S., Wouters, C. et al. Activation of cytomegalovirus-encoded G protein-coupled receptor UL33 by an innate N-terminal peptide. Commun Biol 9, 415 (2026). https://doi.org/10.1038/s42003-026-09660-5
Schlüsselwörter: Cytomegalovirus, viraler GPCR, Zell‑Signalübertragung, Cryo‑EM‑Struktur, Wirkstoff‑Ziel