Clear Sky Science · de
Untersuchung der Reaktionen von Salmonella-Biofilmen auf Antibiotikabehandlung mittels optischer photothermischer Infrarotspektroskopie
Warum klebrige Keimstädte wichtig sind
Viele krankheitserregende Bakterien leben bevorzugt in dicht gepackten Gemeinschaften, sogenannten Biofilmen, in denen Zellen aneinander und an Oberflächen im Körper oder an medizinischen Geräten haften. Innerhalb dieser schleimigen „Städte“ können Mikroben Antibiotika widerstehen, die sie sonst abtöten würden. Diese Studie stellt eine neue Methode vor, um Biofilme detailliert zu untersuchen und zu zeigen, welche Zellen aktiv wachsen und wie sie reagieren, wenn potente Wirkstoffe zugegeben werden. Das Verständnis dieser unsichtbaren Aktivitätsmuster könnte Ärzten helfen, Behandlungen zu entwickeln, die die hartnäckigen Abwehrmechanismen von Biofilmen durchbrechen.
Verborgenes Leben in bakteriellen Städten
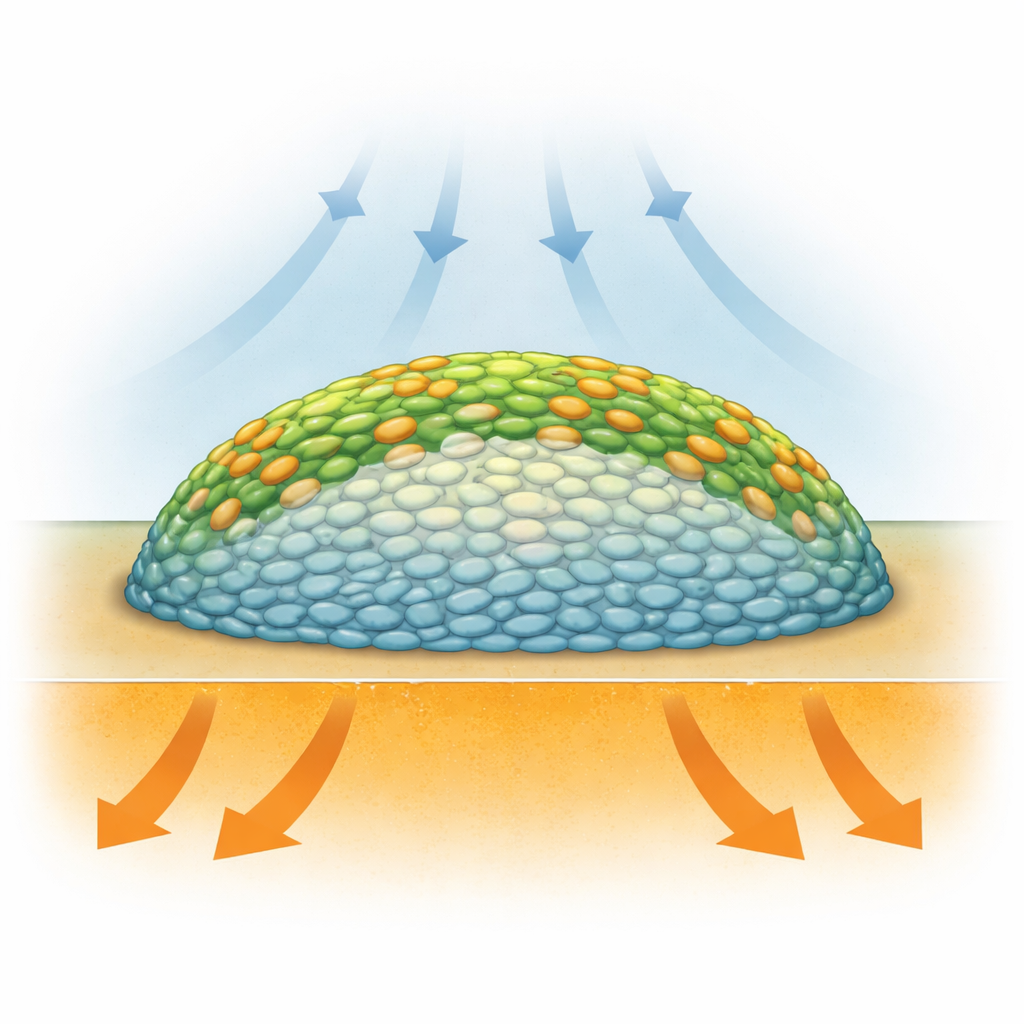
Biofilme sind keine zufälligen Keimansammlungen: Sie sind geschichtete Strukturen, in denen Bakterien je nach Lage sehr unterschiedliche Bedingungen vorfinden. Zellen an der Außenseite haben mehr Zugang zu Sauerstoff aus der Luft, während jene im Inneren sauerstoffarm sind und ihr Wachstum verlangsamen oder in eine Ruhestellung gehen können. Frühere Methoden wie die Fluoreszenzmikroskopie konnten die Struktur zeigen, erforderten aber oft zugesetzte Farbstoffe oder genetische Marker, die die Biologie stören könnten, und sie maßen nicht direkt die chemische Aktivität der Zellen. Die Forschenden benötigten eine Möglichkeit, die Chemie lebender Biofilme schichtweise zu „sehen“, ohne sie auseinanderzureißen oder stark zu verändern.
Chemie sehen mit unsichtbarem Licht
Das Team wandte eine Technik namens optische photothermische Infrarotspektroskopie (O-PTIR) an, die gepulstes unsichtbares Infrarotlicht und einen sichtbaren Laser nutzt, um winzige Molekülschwingungen zu detektieren. Diese Schwingungen wirken wie Fingerabdrücke wichtiger Zellbestandteile, etwa Proteinen, Lipiden und DNA. Um den Stoffwechsel — die aktive Nutzung von Nährstoffen — nachzuverfolgen, fütterten sie Salmonella Typhimurium-Biofilme mit einer speziellen Zuckerform, deren Kohlenstoffatome etwas schwerer sind als üblich (ein stabiles Isotop, bekannt als Kohlenstoff-13). Wenn Zellen aktiv wachsen und neue Proteine bilden, bauen sie diese schwereren Atome in ihre Strukturen ein, was zu subtilen, aber nachweisbaren Verschiebungen im Infrarotsignal führt. Durch Kryoschnitt des Biofilms und das Scannen dünner Querschnitte erzeugten die Forschenden chemische Karten, die zeigen, wo im Biofilm dieses schwere Kohlenstoffisotop eingebaut worden war.
Aktivitätsringe und ruhige Kerne
Die Infrarotbildgebung unbehandelter Salmonella-Biofilme zeigte ein auffälliges Muster: Die äußeren Bereiche und Oberflächenschichten wiesen starke Einlagerung des schweren Kohlenstoffs auf, während ein großer zentraler Kern sehr wenig zeigte. Anders gesagt verhielt sich der Biofilm wie ein Ring aktiver Zellen, der ein ruhiges Inneres umgibt. Statistische Analysen der Infrarotspektren bestätigten, dass Signale von proteinbezogenen Schwingungen in den äußeren Schichten stärker verschoben waren als im Zentrum, was auf eine höhere Proteinsynthese an den Rändern hinweist. Diese Ergebnisse stützen die Idee, dass die Verfügbarkeit von Sauerstoff — die an der Oberfläche am größten ist — der Haupttreiber für metabolische „Hotspots“ in diesem Koloniemodell ist, obwohl Nährstoffe von unten hineinströmen. Die Studie lieferte eine der klarsten und hochauflösendsten Ansichten davon, wie der Stoffwechsel innerhalb eines Biofilms geschichtet ist.
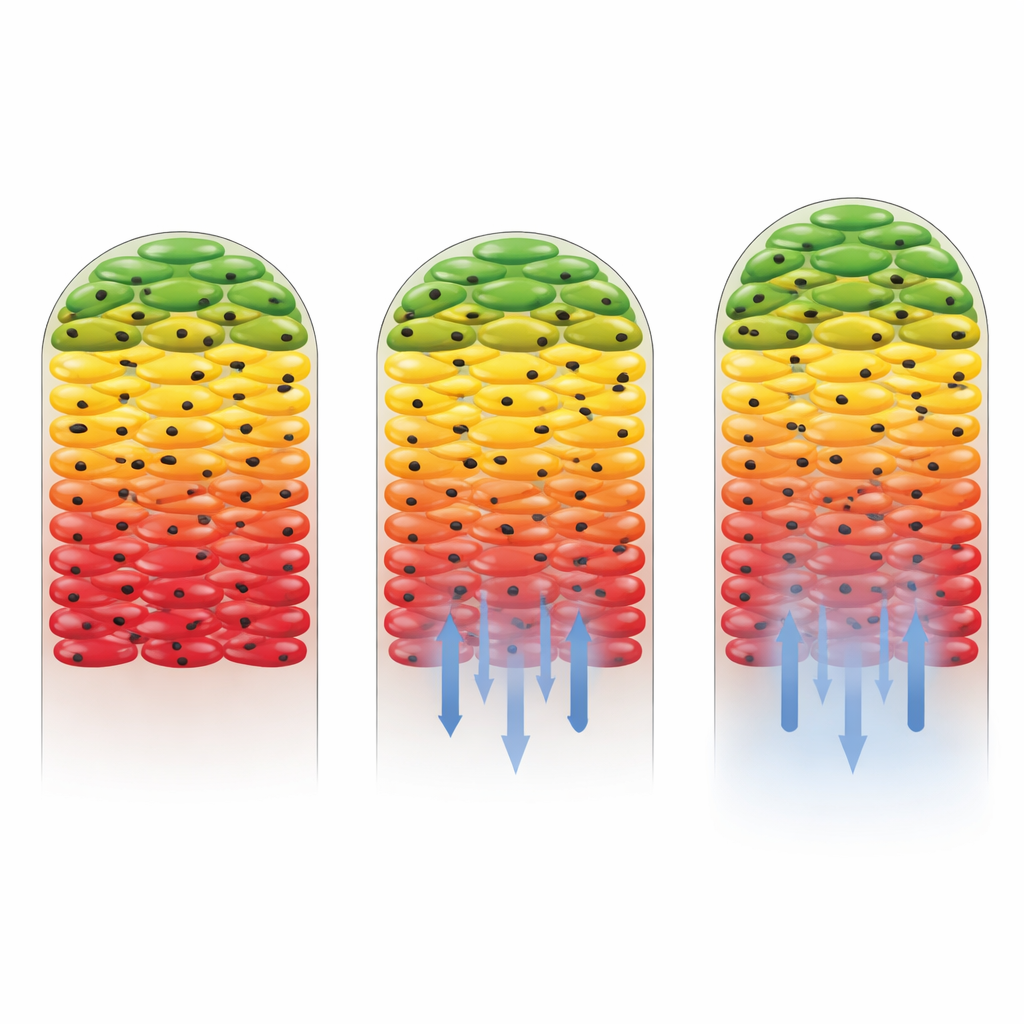
Wie verschiedene Antibiotika die Biofilmaktivität umgestalten
Die Forschenden untersuchten anschließend, was passiert, wenn Antibiotika zugegeben werden. Sie verwendeten zwei Wirkstoffe: Kanamycin, gegen das der Salmonella-Stamm empfindlich ist, und Gentamicin, gegen das der Stamm weitgehend unempfindlich gemacht worden war. In Gegenwart von Gentamicin änderte sich das generelle Muster aus aktiven Außenschichten und ruhigem Kern kaum, was zeigte, dass resistente Zellen weiter wuchsen und schweren Kohlenstoff in großen Teilen des Biofilms einbauten. Im Gegensatz dazu reduzierte Kanamycin die metabolische Aktivität drastisch, vor allem in der Nähe des Biofilmgrundes, wo die Wirkstoffkonzentration am höchsten war. Nur ein dünner Streifen von Zellen, am weitesten vom Antibiotikum entfernt, zeigte noch Zeichen des Kohlenstoffaufbaus. Dies zeigte nicht nur, dass das Medikament wirksam war, sondern auch, dass die Biofilmstruktur selbst einige Zellen schützte, indem sie das Antibiotikum beim Eindringen abschwächte.
Neue Einblicke in die Behandlung hartnäckiger Infektionen
Für Laien ist die Kernbotschaft, dass diese Arbeit ein leistungsfähiges „chemisches Mikroskop“ bietet, um zu beobachten, wie bakterielle Gemeinschaften in drei Dimensionen leben und auf Behandlungen reagieren. Durch die Kombination einer nicht-destruktiven Infrarot-Bildgebung mit einer sicheren schweren Kohlenstoffform konnten die Forschenden genau feststellen, wo Bakterien aktiv wuchsen und wie sich diese Aktivität unter verschiedenen Antibiotika veränderte. Ihre Ergebnisse bestätigen, dass Biofilme eine Mischung aus aktiven und nahezu ruhenden Zellen beherbergen und dass wirksame Wirkstoffe dennoch durch die physische Barriere des Biofilms abgeschwächt werden können. Zukünftig könnte dieser Ansatz genutzt werden, um neue Therapien zu testen, zu erforschen, wie verschiedene Arten in gemischten Biofilmen zusammenarbeiten oder Resistenz teilen, und letztlich dabei helfen, klügere Strategien zur Beseitigung persistenter Infektionen zu entwerfen.
Zitation: Smaje, D., Zhu, X., Hinton, J.C.D. et al. Investigating Salmonella biofilm responses to antibiotic treatment using optical photothermal infrared spectroscopy. Commun Biol 9, 405 (2026). https://doi.org/10.1038/s42003-026-09655-2
Schlüsselwörter: Biofilme, Salmonella, Antibiotikaresistenz, Infrarotbildgebung, stabile Isotopenmarkierung