Clear Sky Science · de
Natürlich vorkommendes Dinactin zielt auf das cpsA‑Protein und tötet Mycobacterium tuberculosis durch Störung der Protonenmotorischen Kraft
Neue Hoffnung gegen einen hartnäckigen Lungenkiller
Tuberkulose gehört weiterhin zu den tödlichsten Infektionskrankheiten weltweit, und multiresistente Stämme breiten sich aus. Diese Studie stellt eine natürlich vorkommende Verbindung namens Dinactin vor, die von Bodenbakterien produziert wird und Mycobacterium tuberculosis abtöten kann, einschließlich medikamentenresistenter und ruhender Formen, die besonders schwer zu eliminieren sind. Indem die Forschenden untersuchten, wie Dinactin wirkt und wie es mit bestehenden Medikamenten zusammenwirkt, skizzieren sie eine vielversprechende neue Strategie, um die TB‑Behandlung zu verkürzen und zu verbessern.
Eine versteckte Waffe in der Natur entdecken
Um nach neuen TB‑Medikamenten zu suchen, screente das Team mehr als 6.000 natürliche Extrakte aus Pflanzen und Mikroorganismen und testete deren Fähigkeit, das Wachstum von TB‑Bakterien in ganzen Zellen statt in isolierten Enzymen zu stoppen. Unter den vielen Kandidaten stach Dinactin hervor. Es gehört zu einer Familie ringförmiger Moleküle, den Makrotetroliden, und zeigte starke Aktivität gegen Standardlaborstämme von TB in sehr niedrigen Dosen, ohne rote Blutkörperchen zu schädigen. Beim Vergleich von Dinactin mit eng verwandten Molekülen erwies sich Dinactin als sowohl wirksamer als auch selektiver, weshalb es der beste Kandidat für eine vertiefte Untersuchung war. 
Kraftvolle Wirkung in schwer erreichbaren Bakterien
TB‑Bakterien können sich in mehreren schwer zu behandelnden Zuständen verbergen: aktiv teilend in der Lunge, in Ruhe mit verlangsamtem Stoffwechsel oder geschützt in Immunzellen. Dinactin griff sie in allen drei Zuständen an. Es tötete aktiv wachsende TB‑Zellen mit einem steilen Abfall lebensfähiger Bakterien und war auch gegen nährstoff‑verarmte, nicht replizierende Zellen wirksam, die Standardtherapien oft überleben. In einem Modell mit menschlichen Makrophagen drang Dinactin in die Wirtszellen ein und reduzierte die Zahl der internalisierten TB‑Bakterien um etwa das Hundertfache. In infizierten Wachsmottenlarven, einem in vivo‑Modell, verbesserte Dinactin allein das Überleben und verringerte die bakterielle Last; die Vorteile waren noch größer, wenn es mit bestehenden TB‑Medikamenten kombiniert wurde.
Zusammenarbeit mit bestehenden Arzneimitteln
Weil die TB‑Behandlung auf Medikamentenkombinationen beruht, prüften die Forschenden, wie Dinactin mit aktuellen Antibiotika wie Rifampicin, Isoniazid, Bedaquilin und anderen interagiert. Mithilfe von Checkerboard‑Assays fanden sie heraus, dass Dinactin die Wirkung der meisten dieser Mittel deutlich verstärkte, insbesondere von Rifampicin und Isoniazid: Durch Zugabe von Dinactin funktionierten deutlich niedrigere Dosen dieser Standardwirkstoffe effektiv. Bemerkenswert ist, dass Dinactin bei klinischen multiresistenten TB‑Isolaten einen Großteil ihrer Sensibilität gegenüber Rifampicin und Isoniazid wiederherstellte. In stationären Kulturen, die eine persistente Infektion nachahmen, töteten Kombinationen aus Dinactin und Rifampicin bzw. Isoniazid deutlich mehr Bakterien als ein einzelnes Mittel, was darauf hindeutet, dass auf Dinactin basierende Kombinationen hartnäckige Infektionen schneller klären könnten.
Wie Dinactin die bakterielle Energie untergräbt
Um zu verstehen, wie Dinactin TB‑Bakterien tötet, untersuchte das Team dessen Auswirkungen auf die Zellhülle und Energiesysteme. Dinactin wirkt als Ionenträger und shuttlelt Kalium und Natrium durch die bakterielle Membran. Dieser zusätzliche Ionentransport macht die Membran durchlässiger und flüssiger, faltet die bakterielle Oberfläche sichtbar ein und lässt Farbstoffe leichter eindringen. Durch den Ionentransport kollabiert die protonenmotorische Kraft — das elektrische und chemische Gefälle, das Bakterien wie eine kleine Batterie zur ATP‑Produktion nutzen. Messungen zeigten, dass beide Komponenten dieses Gradienten, die Membranspannung und der Protonenunterschied, nach Dinactin‑Behandlung verloren gingen. Infolgedessen sanken die ATP‑Spiegel innerhalb der Zellen stark, obwohl ihre Sauerstoffverbrauchsmachinerie weiterlief, was darauf hinweist, dass die Energieproduktion von der Atmung entkoppelt wurde. Dinactin störte außerdem das Gleichgewicht zwischen den reduzierten und oxidierten Formen eines wichtigen Stoffwechselkofaktors (NADH/NAD+) und löste eine Freisetzung reaktiver Sauerstoffspezies innerhalb der Bakterien aus, die weitere zelluläre Komponenten schädigten. 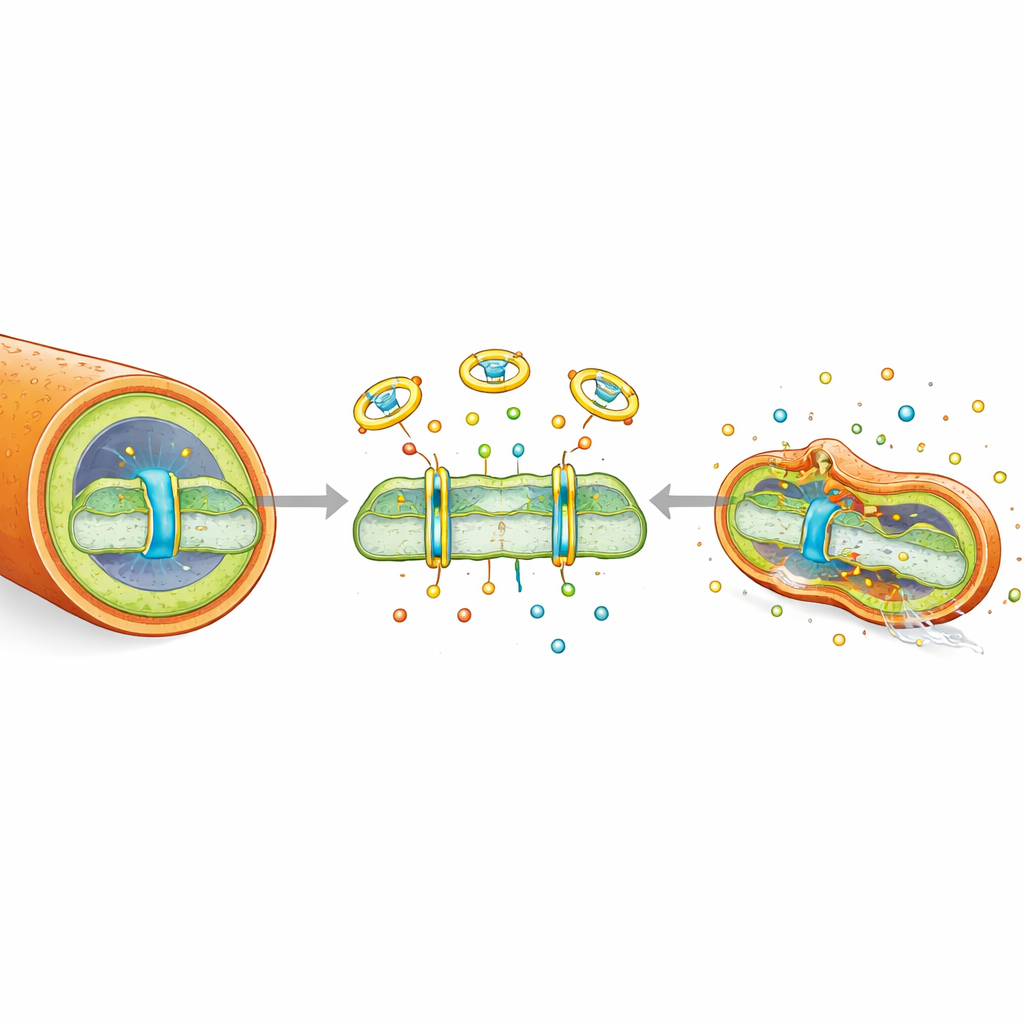
Angriff auf einen wichtigen Zellwandbauer
Um ein spezifisches molekulares Ziel zu identifizieren, isolierten die Forschenden seltene TB‑Verwandte, die spontan weniger empfindlich gegenüber Dinactin geworden waren, und sequenzierten deren Genome. Die meisten dieser Mutanten trugen die gleiche Veränderung in einem Gen namens cpsA, das ein Mitglied der LytR‑Cps2A‑Psr (LCP)‑Proteinfamilie kodiert, die an der Verknüpfung wichtiger Zellwandbestandteile beteiligt ist. Wenn cpsA oder das zugehörige Partnerprotein überproduziert wurde, wurden die Bakterien toleranter gegenüber Dinactin; das Löschen von cpsA machte Zellen auf Platten resistenter, zeigte aber auch, dass Dinactin wahrscheinlich zusätzliche Ziele hat. Mithilfe von Strukturmodellierung und Bindungsexperimenten zeigte das Team, dass Dinactin fest an das cpsA‑Protein an einer spezifischen Stelle bindet und dass die mit Resistenz assoziierte Mutation diese Wechselwirkung deutlich schwächt. Da LCP‑Proteine in Gram‑positiven Bakterien weit verbreitet und in den meisten Gram‑negativen Arten nicht vorhanden sind, hilft diese Zielrichtung zu erklären, warum Dinactin bevorzugt TB und verwandte Organismen angreift.
Welche Bedeutung das für die zukünftige TB‑Behandlung haben könnte
Für Nicht‑Spezialisten ist die zentrale Botschaft, dass Dinactin eine natürliche Verbindung ist, die TB‑Bakterien an ihrer verwundbarsten Stelle trifft: ihrer Energieversorgung und dem Aufbau der Zellwand. Es verhält sich wie ein winziger Ionentransporter, der die bakterielle „Batterie“ entlädt, die Zellen an ATP verarmt, ihre interne Chemie durcheinanderbringt und ein essentielles Zellwand‑Aufbauprotein stört. Gleichzeitig arbeitet es Hand in Hand mit den wichtigsten TB‑Medikamenten und macht diese gegen resistente und ruhende Bakterien wirksamer. Zwar bleibt noch viel Arbeit — insbesondere Sicherheitstests und Studien in Säugetiermodellen — doch positioniert diese Studie Dinactin und verwandte Moleküle als vielversprechende Bausteine für die nächste Generation von TB‑Therapien.
Zitation: Wang, G., Dong, W., Bai, Y. et al. Naturally occurring dinactin targets cpsA protein and kills Mycobacterium tuberculosis by disrupting the proton motive force. Commun Biol 9, 417 (2026). https://doi.org/10.1038/s42003-026-09654-3
Schlüsselwörter: Tuberkulose, Dinactin, Antibiotikaresistenz, Bakterieller Energiestoffwechsel, Wandproteine