Clear Sky Science · de
Agentenbasierte Modellierung zellulärer Dynamik in der adoptiven Zelltherapie
Warum computererzeugte Zellen für die Krebsversorgung wichtig sind
Krebstherapien, die lebende Immunzellen einsetzen, verändern die Medizin. Neue Ansätze jedoch allein in Tieren und Menschen zu testen, ist langsam, teuer und mitunter riskant. Diese Studie stellt ABMACT vor, ein virtuelles Labor, das „digitale“ Krebs‑ und Immunzellen erzeugt und sie auf dem Bildschirm interagieren lässt. Indem es reale Experimente nachspielt und erweitert, zeigt ABMACT Forschern, welche Eigenschaften von NK‑Zell‑Therapien am wichtigsten sind und wie Behandlungspläne bereits weit vor klinischen Studien feinabgestimmt werden können. 
Zellen als digitale Akteure
ABMACT beruht auf agentenbasierter Modellierung, einer Methode, bei der jede Zelle zu einem eigenen kleinen Software‑Agenten wird, der sich bewegen, teilen, sterben oder Nachbarn angreifen kann – jeweils nach einfachen Regeln. Die Autoren definierten vier Hauptakteure: Tumorzellen, aggressive NK‑Zellen, die Tumore töten können, ausgebrannte NK‑Zellen, die ihre Schlagkraft verloren haben, und „wachsame“ NK‑Zellen, die zunächst inaktiv sind, aber wieder aktiv werden können. Regeln dafür, wie diese Zellen wachsen, ermüden, wandern und ihren Zustand wechseln, stammen aus vorhandenen Labor‑ und Tierstudien und wurden in die Simulation kodiert, sodass Tausende virtueller Zellen einen Miniaturbehandlungsverlauf durchspielen können.
Die innere Verdrahtung der Zelle hinzufügen
Moderne Einzelzellsequenzierung zeigt, welche Gene in jeder NK‑Zelle aktiv sind, doch diese molekularen Details lassen sich nur schwer in Ganzorganismus‑Verhalten übersetzen. ABMACT begegnet dem, indem es Genaktivitätsmuster mit praktischen Eigenschaften verknüpft, etwa mit der Wahrscheinlichkeit, dass eine NK‑Zelle eine Tumorzelle tötet, oder mit der Anzahl an Zielen, die sie vor Erschöpfung eliminieren kann. Das Team nutzte Gen‑ und Signalwegdaten aus Mausmodellen für Lymphome und Hirntumoren, um abzuschätzen, wie bestimmte Gene NK‑Zellen zu stärkerer oder schwächerer Tumorkontrolle treiben. Diese gen‑basierten Effekte werden einzelnen virtuellen NK‑Zellen zufällig zugewiesen, wodurch eine digitale Population entsteht, die die natürliche Mischung aus starken und schwachen Killern realer Experimente widerspiegelt.
Tierexperimente nachspielen und erweitern
Die Forschenden überprüften ABMACT anhand mehrerer Experimente, in denen gentechnisch veränderte NK‑Zellen zur Behandlung von Blutkrebserkrankungen und Glioblastomen bei Mäusen eingesetzt wurden. In Lymphom‑Modellen reproduzierte der Simulator korrekt die überlegene Tumorkontrolle von NK‑Zellen, die sowohl einen tumorerkennenden Rezeptor als auch das Wachstumssignal IL‑15 exprimieren, im Vergleich zu einfacheren Produkten oder unveränderten Zellen. Er entsprach nicht nur den gemessenen Tumorgrößen zu einzelnen Zeitpunkten, sondern füllte auch den tagesgenauen Anstieg und Abfall der Tumorlast, der NK‑Zell‑Expansion, der Erschöpfung und dem Auftreten wachsamer Zellen aus. In Glioblastom‑Modellen verfolgte ABMACT erneut die beobachtete Tumorkontrolle und sagte sogar Ergebnisse in einer separaten Ko‑Kultur‑Studie voraus, ohne neu justiert werden zu müssen, was darauf hindeutet, dass seine Regeln allgemeine Merkmale der NK‑Tumor‑Interaktion erfassen.
„Was‑wäre‑wenn“‑Behandlungsentscheidungen im Silizium testen
Da ABMACT am Computer läuft, kann es Fragen untersuchen, die in Tieren schwer oder teuer zu testen wären. Die Autoren variierten systematisch Zell‑Eigenschaften und Dosen, um zu ermitteln, welche Stellschrauben die Tumorkontrolle am stärksten beeinflussen. Sie fanden, dass das Verhältnis von NK‑Zellen zu Tumorzellen, die Fähigkeit jeder NK‑Zelle, wiederholt viele Ziele zu töten, und ihre grundlegende Killing‑Stärke wichtiger sind, als die bloße Verlängerung der Lebensdauer der Zellen. Simulierte Auffrischungsbehandlungen zeigten, dass frühere zusätzliche Dosen und Produkte mit höherer Tötungskraft ein Tumorrebond wirksamer verhindern können als späte, moderate Auffrischungen. Das Modell untersuchte auch, wie schlechte NK‑Zell‑Homing, überfülltes Gewebe oder sauerstoffarme Nischen Begegnungen mit Tumoren verzögern und zum Therapieversagen beitragen können. 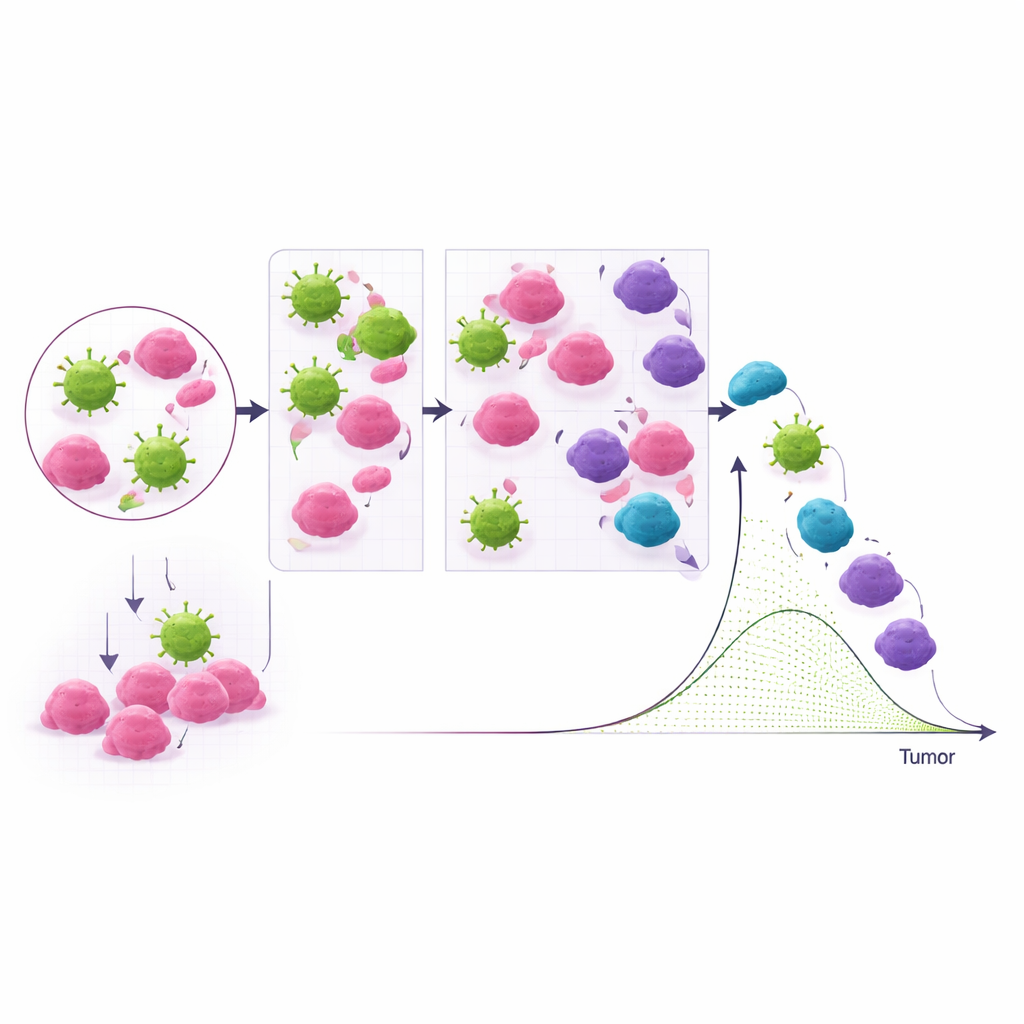
Was das für künftige Zelltherapien bedeutet
Für Nicht‑Fachleute lässt sich ABMACT als hochauflösender Flugsimulator für NK‑Zell‑Krebsbehandlungen betrachten. Indem es seine digitalen Zellen in echte genetische und experimentelle Daten einbettet, erklärt das Framework, warum einige gentechnisch veränderte NK‑Produkte andere übertreffen und warum höhere Dosen nicht immer bessere Ergebnisse liefern. Es weist auf praktische Gestaltungsprinzipien hin: Schicke genügend NK‑Zellen zum Tumor, mache sie zu effizienten Serienkillern und plane Behandlungen früh und durchdacht statt bloß die Dosis zu erhöhen. Solche Modelle können Labor‑ und klinische Tests nicht ersetzen, aber sie können die Auswahl an Optionen einschränken, die Abhängigkeit von Tierstudien verringern und im Lauf der Zeit helfen, Zelltherapien an die Biologie einzelner Patientinnen und Patienten zu personalisieren.
Zitation: Wang, Y., Casarin, S., Daher, M. et al. Agent-based modeling of cellular dynamics in adoptive cell therapy. Commun Biol 9, 409 (2026). https://doi.org/10.1038/s42003-026-09653-4
Schlüsselwörter: adoptive Zelltherapie, natürliche Killerzellen, agentenbasierte Modellierung, Krebsimmuntherapie, CAR‑NK