Clear Sky Science · de
Modellauswahl in der präklinischen Forschung zu Nukleinsäuretherapeutika
Gene in Medikamente verwandeln
Nukleinsäuretherapien sind eine neue Arzneimittelklasse, die nicht primär über die Blockade von Proteinen wirkt, wie die meisten Medikamente, sondern eine Ebene früher ansetzt – bei unseren genetischen Botschaften. Dieser Übersichtsartikel erklärt, wie Wissenschaftler die geeigneten Labor‑ und Tiermodelle auswählen, um diese RNA‑zielgerichteten Wirkstoffe zu testen, bevor sie an Patientinnen und Patienten gelangen. Für Laien ist das relevant, weil kluge Modellentscheidungen zu schnelleren, sichereren und wirksameren Behandlungen genetischer Erkrankungen führen können, einschließlich seltener Kindheitskrankheiten und häufigerer Leiden wie Herzkrankheiten.
Wodurch unterscheiden sich diese genetischen Medikamente?
Nukleinsäuretherapeutika (NATs) umfassen kurze Stränge wie Antisense‑Oligonukleotide (ASOs) und kleine interferierende RNAs (siRNAs). Statt auf Form und Chemie von Proteinzielen zu vertrauen, erkennen diese Wirkstoffe ihre Ziele nach Basenpaarungsregeln – dieselbe A‑T‑ und G‑C‑Übereinstimmung, die der DNA zugrunde liegt. Das macht sie programmierbar: Kennt man die zu verändernde RNA‑Sequenz, kann man oft viele Kandidaten schnell entwerfen, ohne jahrelange klassische Chemie. Die Schwierigkeit liegt dann nicht mehr in der Frage »Können wir eine aktive Verbindung herstellen?«, sondern »Wie messen wir, ob sie in einem realistischen biologischen Umfeld wirklich wirkt?« Da schon ein einzelner Basenunterschied die Aktivität entscheidend beeinflussen kann, ist die Wahl geeigneter Testsysteme kritisch.
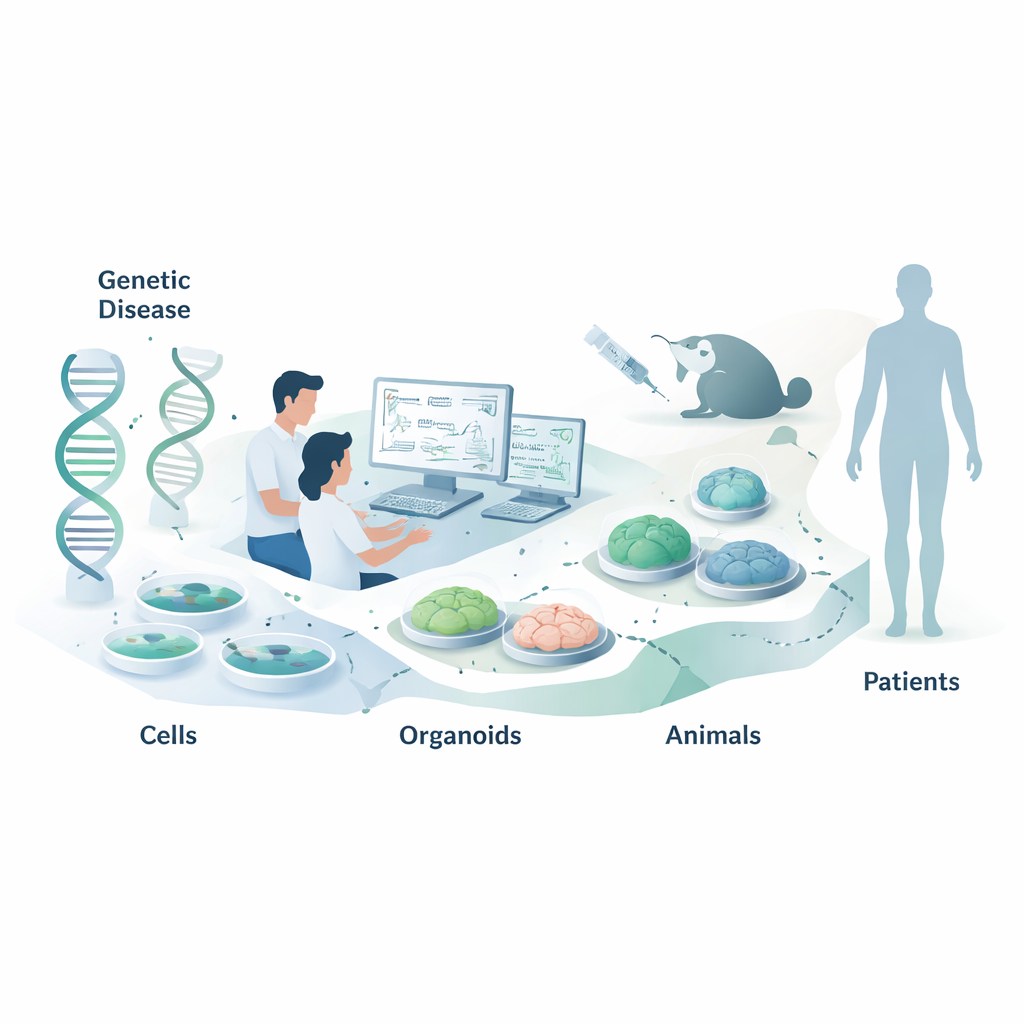
Einfache Zelltests: schnell, aber nicht die ganze Geschichte
Die erste Station für die meisten NATs ist ein Panel relativ leicht zu kultivierender Zelllinien wie HeLa oder HEK293, die das Ziel‑RNA bereits exprimieren. Forschende geben große Bibliotheken von Kandidaten‑ASOs oder siRNAs zu und messen dann, wie stark Ziel‑RNA und das dazugehörige Protein abnehmen, mit Techniken wie PCR und Western‑Blot. Sie arbeiten auch mit patienteneigenen Zellen, die den genetischen Hintergrund einer Person besser erfassen und Tests von »allelselektiven« Wirkstoffen erlauben, die nur die fehlerhafte Genkopie stilllegen. Wenn das natürliche Gen nicht bequem exprimiert wird, führen Wissenschaftler manchmal künstliche Minigene oder Reporterplasmide ein, die aufleuchten, wenn die RNA geschnitten oder korrekt gespleißt wird. Solche Systeme sind leistungsfähig, um viele Designs schnell zu vergleichen, können aber wichtige Details übersehen, etwa natürliche RNA‑Struktur oder zelltyp‑spezifische Verarbeitung, weshalb Ergebnisse in realistischeren Kontexten bestätigt werden müssen.
Von molekularen Korrekturen zum realen Zellverhalten
Viele NATs zielen nicht nur darauf ab, fehlerhafte RNA zu zerstören, sondern sie durch Modifikation des Spleißens zu reparieren – des Prozesses, der die Stücke der Genbotschaft zusammenfügt. Sorgfältig gestaltete ASOs können bewirken, dass Zellen ein schädliches Exon überspringen, ein fehlendes Stück wiederherstellen oder das Einfügen eines »Pseudo‑Exons« verhindern, das den Code zerstört. Um zu prüfen, ob solche Änderungen die Zellfunktion tatsächlich verbessern, gehen Forschende über einfache Messungen von RNA‑ und Proteinmengen hinaus. In patientenabgeleiteten Zellen testen sie, ob Enzymaktivität zurückkehrt, ob Ionentransport in Lungenzellen normalisiert wird oder ob Signalwege in Immunzellen korrekt reagieren. Zunehmend nutzen sie dreidimensionale Organoide – Mini‑Gewebe, die aus Stammzellen von Patientinnen und Patienten gezüchtet werden und Herzschläge, Gehirnnetzwerkaktivität oder anderes komplexes Verhalten nachahmen können. Diese 3‑D‑Modelle sind organnäher, aber aufwändiger, langsamer und teurer, sodass Teams Realismus und Durchsatz abwägen müssen.
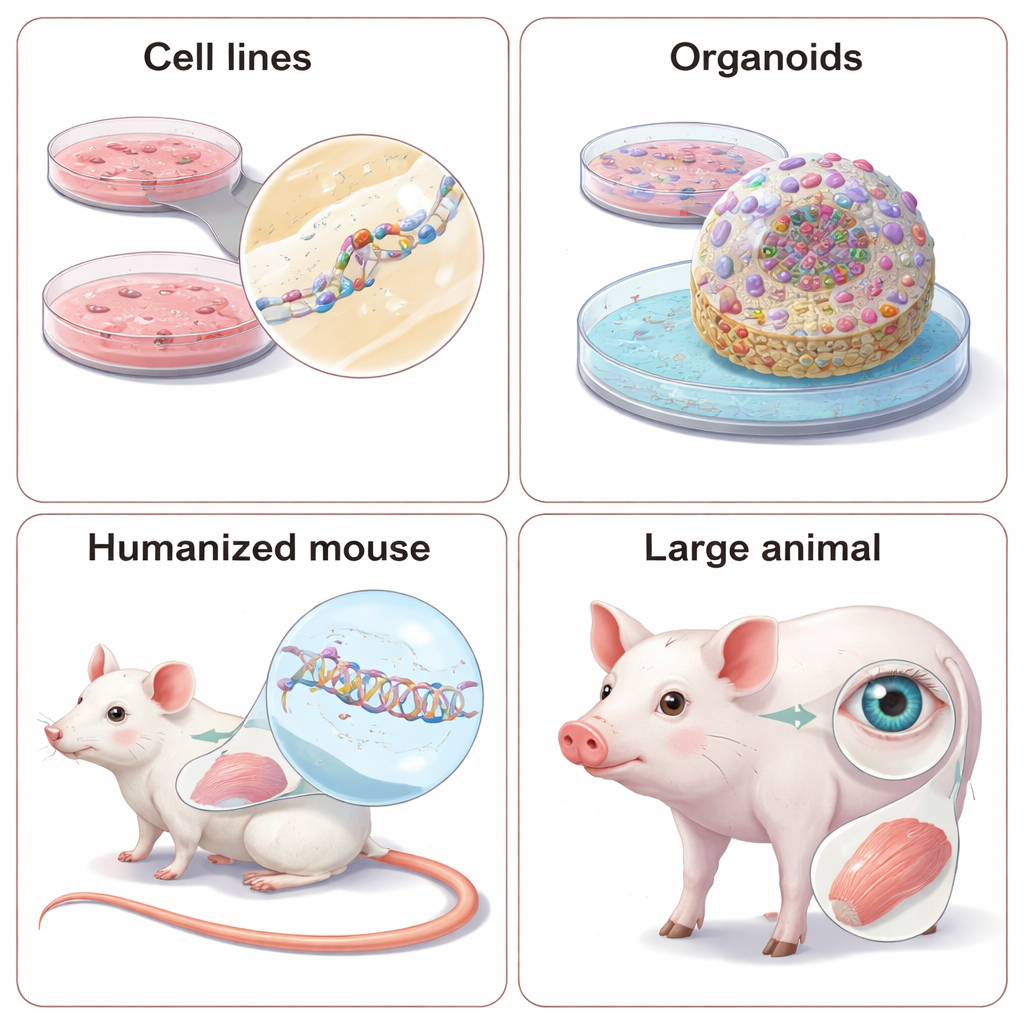
Warum Tiere weiterhin wichtig sind – und wie man sie humanisiert
Einige Krankheitsmerkmale, wie der Gesamtstoffwechsel, Organ‑zu‑Organ‑Interaktionen oder Verhalten, lassen sich in Schalen nicht abbilden. Dafür werden NATs in lebenden Tieren getestet. Da diese Wirkstoffe auf exakte RNA‑Sequenzen achten, stehen Forschende vor einer Wahl: »Surrogat«‑Wirkstoffe zu entwerfen, die zur tierischen Version des Gens passen, oder das Tier so umzubauen, dass es menschliche genetische Sequenzen trägt. Surrogat‑ASOs und siRNAs können zeigen, ob die Senkung eines Gens Symptome in etablierten Mausmodellen verbessert, spiegeln aber nicht perfekt das human‑zielende Medikament wider. Humanisierte Modelle – Mäuse oder sogar Mini‑Schweine mit Abschnitten oder vollständigen Kopien menschlicher Gene – erlauben das Testen des tatsächlichen klinischen Kandidaten, benötigen jedoch erhebliche Zeit und Kosten, und subtile Unterschiede in der Genregulation zwischen Arten können weiterhin zu Überraschungen führen. Der Überblick hebt auch die zunehmende Nutzung großer Tiere hervor, insbesondere bei Erkrankungen von Auge und Muskulatur, wo die Anatomie der des Menschen näher kommt.
Blick nach vorn: intelligentere Modelle und weniger Raten
Die Autoren kommen zu dem Schluss, dass es kein einzelnes »bestes« Modell für Nukleinsäurewirkstoffe gibt; stattdessen braucht jedes Projekt einen maßgeschneiderten Fahrplan, der mit schnellen, einfachen Assays beginnt und zu komplexeren, humanrelevanten Systemen fortschreitet. Da Regulatoren und Geldgeber den Tiergebrauch reduzieren wollen, werden anspruchsvolle Organoide, Organ‑on‑a‑Chip‑Systeme und Computermodelle voraussichtlich mehr der Arbeit übernehmen, besonders in Kombination mit maschinellen Lernwerkzeugen, die vorhersagen, welche Sequenzen und Chemien am besten funktionieren. Letztlich können Forschende durch das Verständnis der Stärken und blinden Flecken jedes Modells – und durch das Teilen von Best Practices und Daten in der gesamten Fachwelt – programmierbare genetische Ideen verlässlicher in sichere, wirkungsvolle Medikamente für Patientinnen und Patienten verwandeln.
Zitation: Oliver, P.L., Hill, A.C. Model selection in preclinical nucleic acid therapeutics research. Commun Biol 9, 200 (2026). https://doi.org/10.1038/s42003-026-09650-7
Schlüsselwörter: Nukleinsäuretherapeutika, Antisense-Oligonukleotide, siRNA, präklinische Modelle, Gentherapie