Clear Sky Science · de
Selektive Bindung zweiwertiger Kationen verändert die Mechanik von Nukleosomen und befreit die Dynamik der Histonschwänze
Wie winzige Ionen unsere DNA steuern helfen
In jeder Zelle müssen Meter an DNA gefaltet, verdichtet und doch bei Bedarf zugänglich gehalten werden. Dieser Artikel untersucht, wie zwei häufige Mineralionen in unseren Zellen, Magnesium und Calcium, subtil beeinflussen, wie DNA um Proteine gewickelt ist, und damit beeinflussen, wie dicht unser genetisches Material verpackt ist und wie leicht es gelesen werden kann. Durch Simulationen dieser Wechselwirkungen auf atomarer Ebene zeigen die Autoren, dass Veränderungen der Ionenkonzentrationen lokale DNA-Strukturen versteifen oder entspannen und das Verhalten flexibler Proteinschwänze verändern können, die bei der Organisation von Chromosomen helfen.
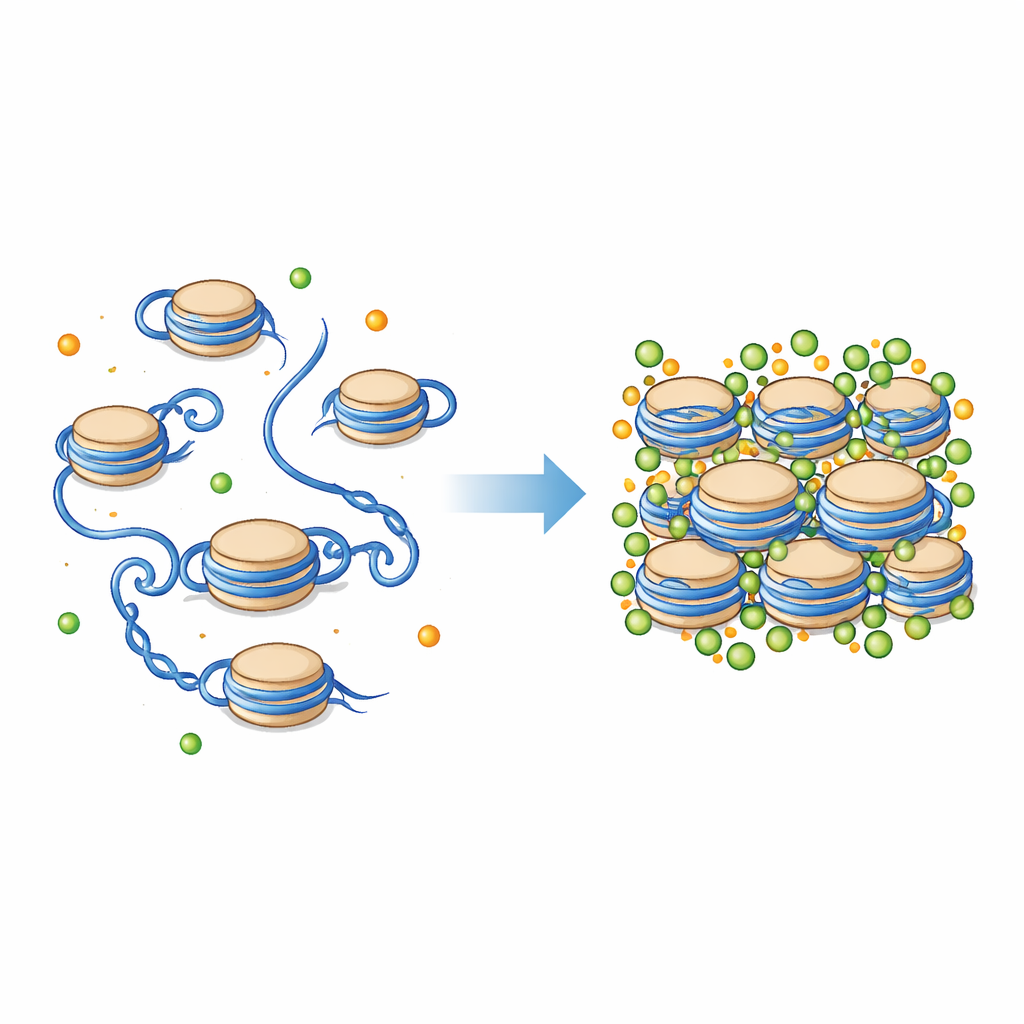
Die Perle im Zentrum der Chromosomenpackung
DNA in unseren Zellen liegt nicht lose herum; sie ist um Proteinscheiben gewickelt, die Nukleosomen genannt werden. Jedes Nukleosom ist ein kurzer Abschnitt DNA, der um einen Komplex aus Histonproteinen gewunden ist, mit flexiblen Schwänzen, die nach außen reichen. Zusammen bilden diese Einheiten die grundlegende "Perlen-auf-einer-Schnur"-Struktur des Chromatins, die sich dann zu kompakteren Fasern falten kann. Die Umgebung der Nukleosomen ist voll mit geladenen Teilchen, darunter Magnesium (Mg²⁺) und Calcium (Ca²⁺). Diese Ionen sind dafür bekannt, die Kondensation von Chromosomen zu fördern, doch genau wie sie die feinen mechanischen Details der Nukleosomen und ihrer Histonschwänze beeinflussen, war schwer direkt zu beobachten.
Simulation einer dicht bevölkerten atomaren Welt
Um diese Details zu entschlüsseln, führten die Autoren 81 Mikrosekunden groß angelegte Computersimulationen durch, in denen jedes Atom von DNA, Protein, Wasser und Ionen explizit modelliert wurde. Sie variierten systematisch Magnesium- und Calciumspiegel, testeten unterschiedliche Beschreibungen des Ionverhaltens in den Simulationen und untersuchten Nukleosomen mit und ohne ihre Histonschwänze. Durch den Vergleich der simulierten Ionbindungsprofile mit experimentellen Messungen identifizierten sie ein verfeinertes Modell, das am besten widerspiegelt, wie reale Nukleosomen diese Ionen anziehen: Magnesium bevorzugt DNA-Rillen, während Calcium häufiger am DNA-Rückgrat und an bestimmten sauren Proteinstellen anliegt.
Wie Ionen die DNA zusammendrücken und den Kern versteifen
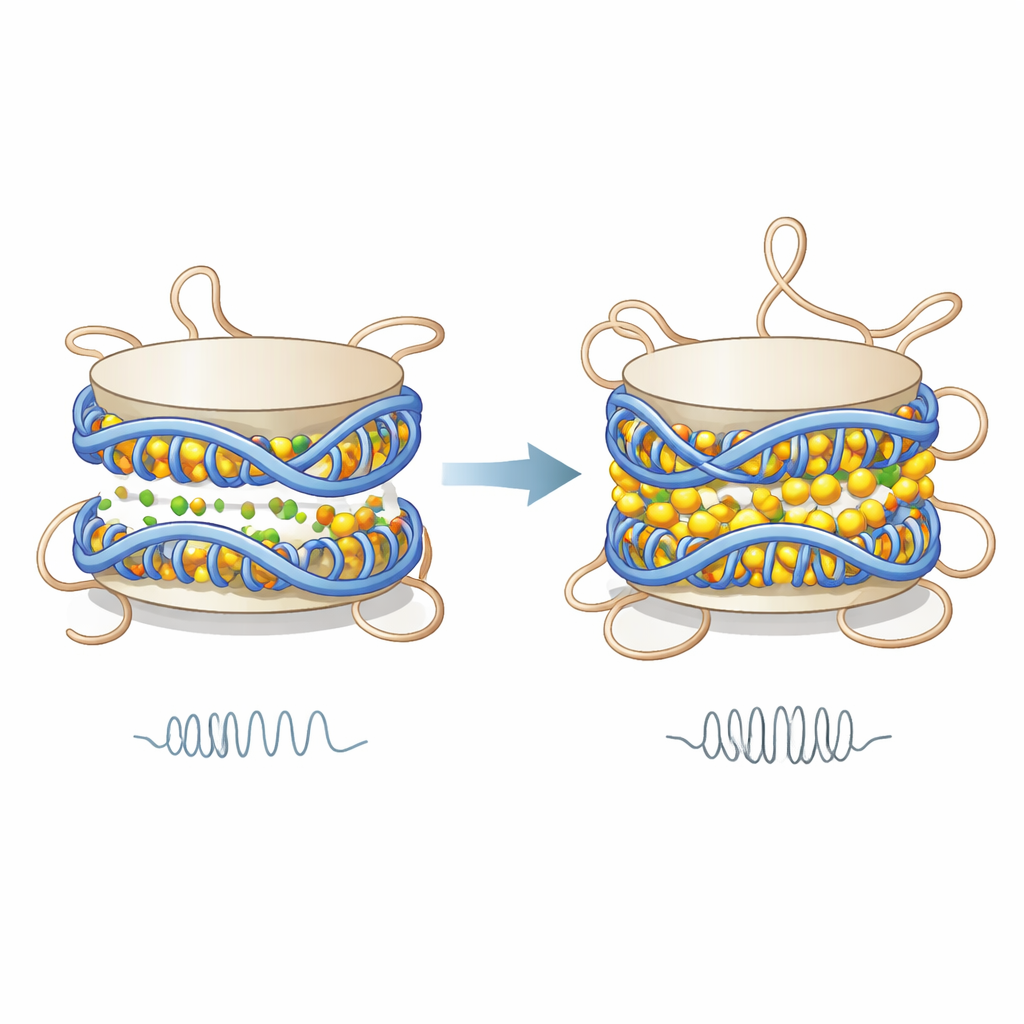
Die Simulationen zeigen, dass zweiwertige Ionen entlang der DNA-Oberfläche und in dem engen Raum zwischen den beiden Windungen der DNA, die jedes Nukleosom umwickeln, konzentriert sind. Durch die teilweise Neutralisierung der starken negativen DNA-Ladung reduzieren diese Ionen die elektrische Abstoßung zwischen benachbarten DNA-Windungen. Das Ergebnis ist, dass die beiden DNA-Spiralen näher zueinander gezogen werden, das Nukleosom leicht kürzer wird und seine mechanische Steifigkeit zunimmt, gemessen mit einem Modell, das das Nukleosom als winzigen elastischen Zylinder behandelt. Diese zusätzliche Steifigkeit entsteht nicht durch Abfallen der DNA oder großes Abwickeln; vielmehr resultiert sie aus subtilen Abstandsänderungen und koordinierteren Bewegungen bestimmter DNA-Regionen, die zusammen wie eine steifere Einheit agieren.
Die Befreiung der flexiblen Proteinschwänze
Während der DNA-Kern kompakter und starrer wird, reagieren die flexiblen Histonschwänze entgegengesetzt. Unter niedrigen Ionenkonzentrationen haften positiv geladene Aminosäuren in diesen Schwänzen an der negativ geladenen DNA und bilden zahlreiche stabile Kontakte. Wenn Magnesium oder Calcium entlang der DNA binden, schirmen sie diese Ladungen ab und schwächen die Anziehung zwischen Schwänzen und DNA. Die Autoren finden, dass Kontakte zwischen Schwänzen – besonders jene des H3-Histons – seltener werden, die Verweilzeiten auf der DNA kürzer sind und die Schwänze ein breiteres Positionsspektrum durchmustern. Das bedeutet, die Schwänze interagieren mit der DNA in häufigeren, aber kürzeren Begegnungen, werden dynamischer und können möglicherweise leichter benachbarte Nukleosomen erreichen.
Folgen für Genkontrolle und Chromatinstatus
Zusammen zeichnen diese Befunde eine doppelte Rolle für Magnesium und Calcium im Chromatin. Indem sie die DNA-Wicklung straffen und die Nukleosomensteifigkeit erhöhen, fördern sie kompakteres, weniger flexibles Chromatin. Gleichzeitig lockern sie Histonschwanz–DNA-Kontakte und erhöhen die Schwanzbeweglichkeit, wodurch Schlüsselseiten freigelegt werden, die chemisch modifiziert oder von regulatorischen Proteinen erkannt werden können. Da die Ionenkonzentrationen im Zellkern mit Signalen und Energieverbrauch schwanken, legt diese Arbeit nahe, dass kleine chemische Änderungen in der zellulären Umgebung sowohl das mechanische Verhalten von Nukleosomen als auch die Zugänglichkeit ihrer regulatorischen Schwänze feinjustieren können und so Fenster für Genaktivität öffnen oder schließen helfen.
Zitation: Hu, G., Zhang, H., Xu, W. et al. Selective binding of divalent cations reshapes nucleosome mechanics and unlocks histone tail dynamics. Commun Biol 9, 365 (2026). https://doi.org/10.1038/s42003-026-09648-1
Schlüsselwörter: Chromatin, Nukleosomenmechanik, Magnesium- und Calciumionen, Histonschwänze, Genregulation