Clear Sky Science · de
Wnt11 vermittelt die Interaktion zwischen Fibroblasten und glatten Muskelzellen und fördert neurogene Blasenfibrose bei Ratten
Wenn Nerven versagen, vernarbt die Blase
Viele Menschen mit Rückenmarksverletzungen, Multipler Sklerose oder Parkinson entwickeln eine „neurogene Blase“, bei der geschädigte Nerven die Speicherung und Ausscheidung von Urin nicht mehr richtig steuern können. Im Laufe der Zeit kann die Blasenwand durch narbenähnliches Gewebe dick und steif werden, was die Nierenfunktion und die Lebensqualität bedroht. Diese Studie an Ratten deckt einen wichtigen molekularen Verursacher dieser Vernarbung auf und deutet auf neue Ansätze hin, das Fortschreiten zu verlangsamen oder möglicherweise zu verhindern.
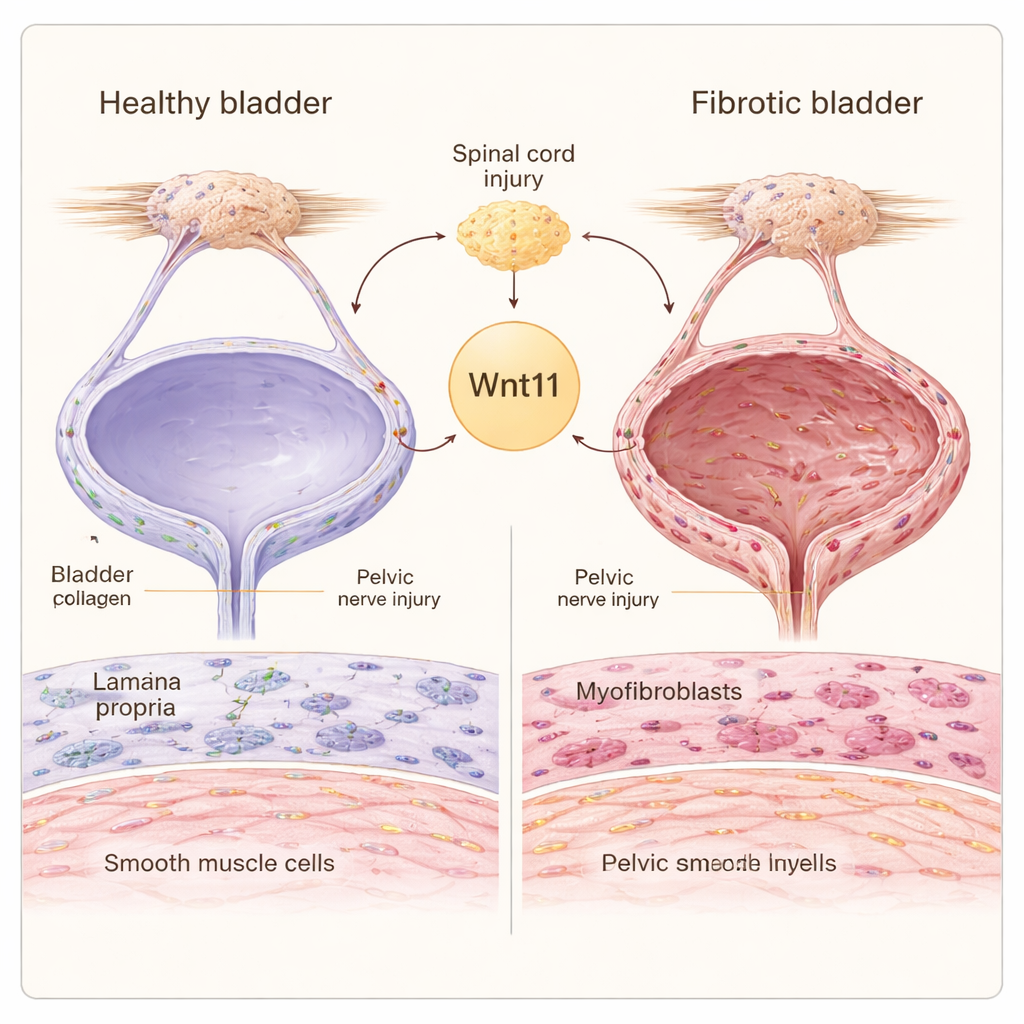
Ein versteckter Preis der Nervenschädigung
Wenn die Nerven, die die Blase versorgen, verletzt werden – sei es im Rückenmark oder in der Beckenregion – muss das Organ härter arbeiten, um den Urin zu bewältigen. Die Blasenwand enthält zwei wichtige Stütz-Zelltypen: Fibroblasten, die das Bindegewebe um die Zellen herum bilden, und glatte Muskelzellen, die sich zusammenziehen, um den Urin auszutreiben. Bei der neurogenen Blase können Fibroblasten in hochaktive „Myofibroblasten“ umschalten, die überschüssiges Kollagen produzieren, während glatte Muskelzellen von einem schlanken, kontraktilen Zustand in einen voluminöseren, stärker synthetischen Zustand übergehen. Zusammen führen diese Veränderungen zur Ablagerung starrer Narben, die die Dehnbarkeit und Entleerung der Blase verringern.
Ein Signalmolekül rückt ins Rampenlicht
Die Forschenden konzentrierten sich auf eine Familie von Zell‑zu‑Zell‑Kommunikationsproteinen, die als Wnt‑Liganden bekannt sind und in anderen Organen Gewebewachstum und Vernarbung regulieren. Beim Screening von Blasen aus rückenmarksverletzten Ratten fanden sie, dass ein Mitglied, Wnt11, in den fibrotischen Blasen, die entweder durch Rückenmarksverletzung oder durch Zerquetschung des Becken-Nervs verursacht wurden, konstant und stark erhöht war. Die Wnt11‑Spiegel stiegen sowohl in Fibroblasten als auch in glatten Muskelzellen an, und die Menge an Wnt11 korrelierte mit dem Schweregrad der Blasenfunktionsstörung. Wenn normale Blasenzellen im Reagenzglas einem anderen pro‑fibrotischen Faktor, TGF‑β1, ausgesetzt wurden, erhöhten sie ebenfalls die Wnt11‑Produktion, was auf eine sich gegenseitig verstärkende Schleife zwischen diesen beiden Signalen hindeutet.
Vom chemischen Signal zur dauerhaften Narbe
Um zu prüfen, ob Wnt11 nur Beiwerk oder ein aktiver Treiber ist, ergänzte das Team Ratten mit Nervenverletzung um zusätzliches Wnt11‑Protein und blockierte außerdem die Wnt‑Sekretion mit einem Wirkstoff namens LGK974. Zusätzliches Wnt11 vergrößerte die Blasen, verschlechterte die Druckmuster während Füllung und Entleerung, verdickte die Muskelschicht und erhöhte die Kollagenablagerung. Die Blockade der Wnt‑Sekretion hatte den gegenteiligen Effekt: sie verbesserte die Harnprobleme und reduzierte das Narbengewebe. In isolierten Zellen trieb Wnt11 Fibroblasten in Richtung Myofibroblasten und veranlasste glatte Muskelzellen in den synthetischen, fibrosefördernden Phänotyp. Das Abschalten des Wnt11‑Gens selbst bremste diese Veränderungen ab, was deutlich machte, dass Wnt11 ein zentraler Beschleuniger der Blasenumbildung ist.
Wie Zellen das Fibrose‑Signal entschlüsseln
Bei genauerer Untersuchung kartierte die Studie den Weg von Wnt11 an der Zelloberfläche bis zu Genveränderungen im Zellkern. Wnt11 bindet an einen Rezeptor namens Vangl2 auf Blasenfibroblasten und glatten Muskelzellen. Diese Partnerschaft nutzt nicht den klassischen Wnt‑Weg mit dem Protein β‑Catenin; stattdessen aktiviert sie eine andere Kette, den sogenannten planar cell polarity (PCP)‑Signalweg. Hier rekrutieren Wnt11 und Vangl2 ein Adapterprotein namens DVL2, das dann die Kinase JNK einschaltet. JNK aktiviert seinerseits die Transkriptionsfaktoren c‑JUN und NFAT5, die in den Zellkern wandern und helfen, pro‑fibrotische Gene einzuschalten. Der TGF‑β1‑Signalweg, ein bekannter Treiber der Vernarbung, konvergiert physisch und funktionell mit dieser Wnt11–Vangl2–JNK‑Achse, sodass sich die beiden Signale sowohl an der Zellmembran als auch im Kern gegenseitig verstärken.
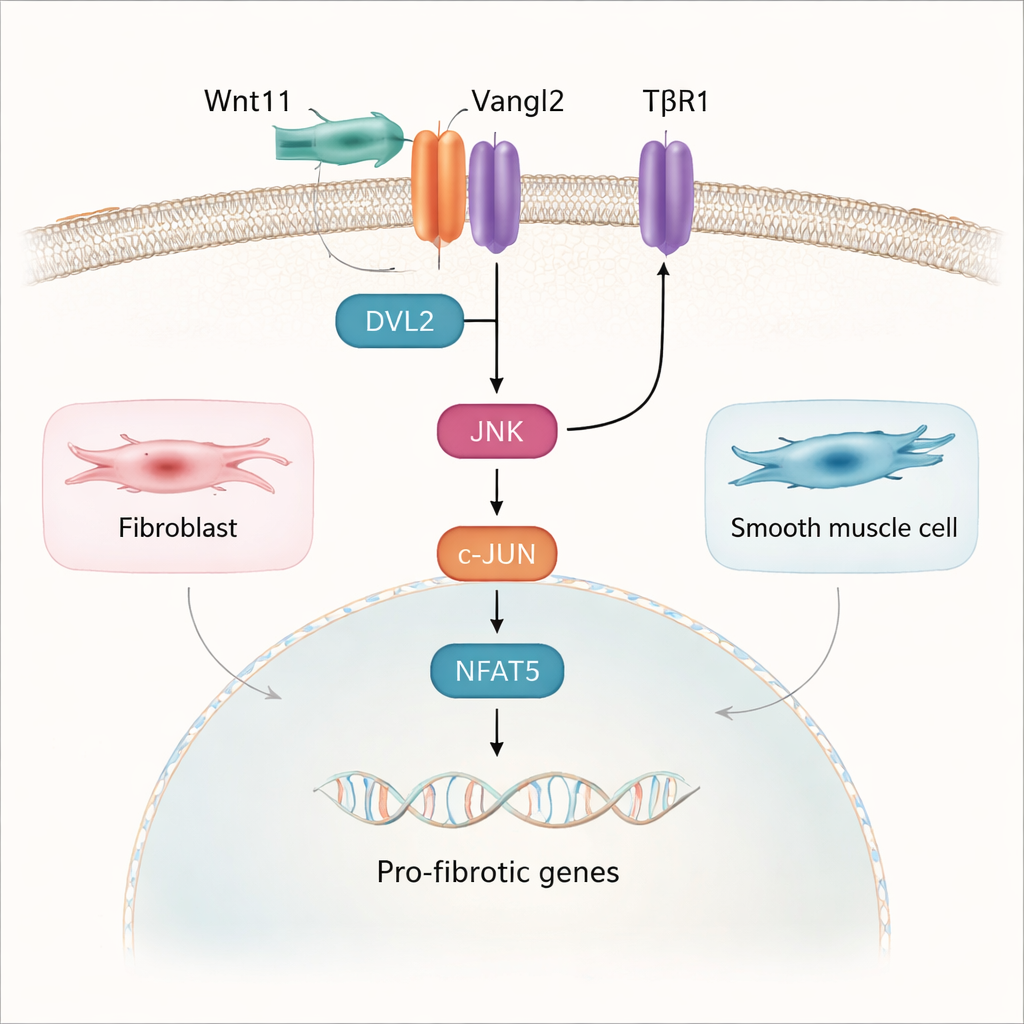
Auf dem Weg zu weicheren, gesünderen Blasen
Da Wnt11 und TGF‑β1 zusammenwirken, um die Blase zu verhärten, testete das Team Wirkstoffe, die Schlüsselschritte beider Wege blockieren. Bei Ratten mit neurogener Blase ergab die kombinierte Hemmung des TGF‑β‑Rezeptors TβR1 und der JNK‑Kinase die besten Ergebnisse: kleinere Blasen, dünnere Muskelwände, weniger Kollagen und verbesserte Urinspeicherung und ‑entleerung im Vergleich zur Einzeldosisbehandlung. Für Laien lautet die Kernbotschaft: Ein spezifisches, durch Nervenverletzung ausgelöstes Signal, Wnt11, hilft dabei, normale Stütz‑ und Muskelzellen in narbenbildende Zellen umzuwandeln. Die Unterbrechung dieses Signals, insbesondere in Kombination mit klassischen TGF‑β‑Blockern, könnte die Grundlage künftiger Therapien bilden, die nicht nur Symptome behandeln, sondern die Struktur und Funktion der Blase bei Menschen mit neurogener Blase erhalten.
Zitation: Ge, Q., Zhang, J., Fan, Z. et al. Wnt11 mediates fibroblast–smooth muscle cell interaction to promote neurogenic bladder fibrosis in rats. Commun Biol 9, 194 (2026). https://doi.org/10.1038/s42003-026-09647-2
Schlüsselwörter: neurogene Blase, Fibrose, Wnt11, glatte Muskelzellen, TGF-β-Signalweg