Clear Sky Science · de
Tbr2-abhängige parallele Wege regulieren die Entwicklung unterschiedlicher ipRGC-Subtypen
Wie unsere Augen Zeit und Form mitteilen
Über das Bildsehen hinaus halten unsere Augen auch still und leise die innere Uhr in Takt, steuern die Pupillenweite und helfen uns, die allgemeine Helligkeit wahrzunehmen. Eine kleine Gruppe besonderer Netzhautnervenzellen, die intrinsisch photosensitiven retinalen Ganglienzellen (ipRGCs), übernimmt einen Großteil dieser Aufgaben. Sie reagieren auf Licht mithilfe eines Pigments namens Melanopsin und senden Signale tief ins Gehirn. Diese Studie stellt eine grundlegende Frage mit weitreichenden Folgen: Wie teilt sich eine frühe Population sich entwickelnder Nervenzellen in mehrere verschiedene ipRGC-Typen auf, von denen jeder für eine andere Funktion verdrahtet ist?
Ein Hauptschalter, viele lichtempfindliche Zelltypen
In der Mausnetzhaut gehen alle sechs bekannten ipRGC-Subtypen aus einer frühen Population von Ganglienzellen hervor, die ein Gen namens Tbr2 aktivieren. Dieses Gen wirkt wie ein Hauptschalter und schaltet Programme ein, die für die Bildung von ipRGCs und für die Aufrechterhaltung der Aktivität des Melanopsin-Gens Opn4 erforderlich sind. Allein ein einzelner Hauptschalter kann jedoch nicht erklären, wie sechs verschiedene ipRGC-Varianten entstehen, jede mit eigener Form, Lichtantworten und Zielregionen im Gehirn. Die Autoren führten RNA-Sequenzierungen entwickelnder Mäusenetzhäute durch, um nach Genen zu suchen, deren Aktivität von Tbr2 abhängt. Unter einer kleinen Zahl von Kandidaten stachen zwei hervor: Irx1 und Tbx20, beide bereits als Regulatoren zellulärer Identität in anderen Körperregionen bekannt. 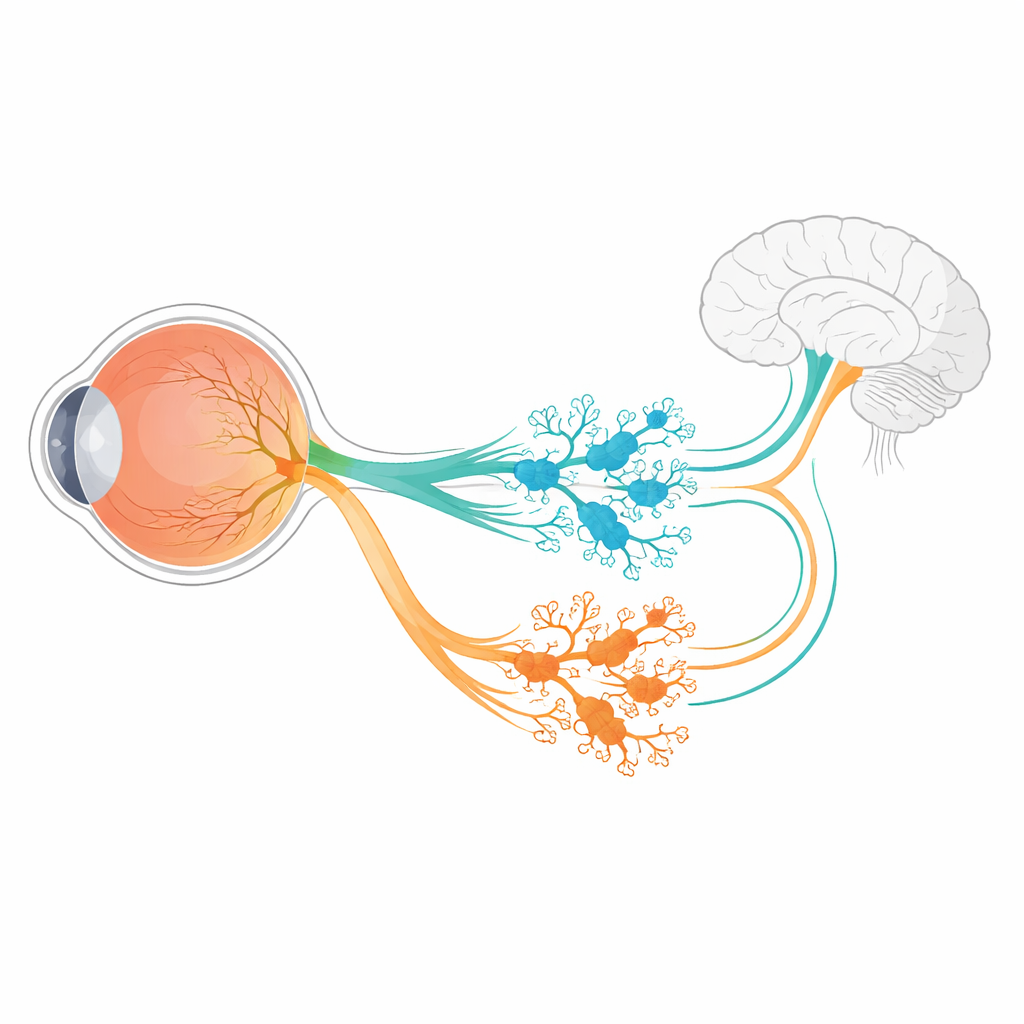
Zwei verzweigende Wege in der Netzhaut
Mithilfe neu konstruierter Mausstämme, die Irx1- bzw. Tbx20-produzierende Zellen mit fluoreszenten oder enzymatischen Markern kennzeichnen, verfolgten die Forschenden, wo und wann diese Faktoren eingeschaltet werden. Sie fanden heraus, dass Irx1 und Tbx20 in überlappenden Gruppen junger retinaler Ganglienzellen um die Mitte der Gestationszeit erscheinen, sich aber bis zum Erwachsenenalter schnell zu nahezu vollständig getrennten Sätzen aufteilen. Irx1 kommt vorwiegend in drei ipRGC-Typen vor, die als M3, M4 und M5 bezeichnet werden, während Tbx20 in M1-, M2- und M6-Zellen konzentriert ist, mit nur geringen Überlappungen in einigen M3- und M5-Zellen. Detaillierte Bildgebung, elektrische Messungen und Bahnnachverfolgungen zeigten, dass jeder Faktor eine eigene Sammlung von ipRGCs kennzeichnet, die charakteristische dendritische Anordnungen, Lichtantworten und Projektionmuster zu spezifischen Hirnregionen für die Uhreinstellung, Reflexe und visuelle Verarbeitung aufweisen.
Schalter, die Lichtempfindlichkeit und Überleben der Zellen einstellen
Als Nächstes fragten die Forschenden, was passiert, wenn jeder Faktor entfernt wird. Wurde Irx1 in der sich entwickelnden Netzhaut ausgeschaltet, blieben Anzahl und Grundstruktur der Irx1-gekennzeichneten ipRGCs weitgehend erhalten, aber ihre Melanopsin-Level sanken deutlich. Mit anderen Worten: Irx1 erwies sich als essenziell, um das Opn4-Lichtwahrnehmungsprogramm in M3-, M4- und M5-Zellen vollständig zu aktivieren, nicht jedoch für die Bildung dieser Zellen an sich. Tbx20 verhielt sich anders. Das Entfernen von Tbx20 senkte nicht nur die Opn4-Expression, sondern halbierte außerdem ungefähr die Zahl der Tbx20-positiven ipRGCs und verringerte später das Überleben dieser Zellen. Das deutet darauf hin, dass Tbx20 sowohl beim Aufbau als auch bei der Erhaltung bestimmter ipRGC-Subtypen, insbesondere M1, M2 und M6, hilft und zugleich deren melanopsinbasierte Lichtempfindlichkeit unterstützt. 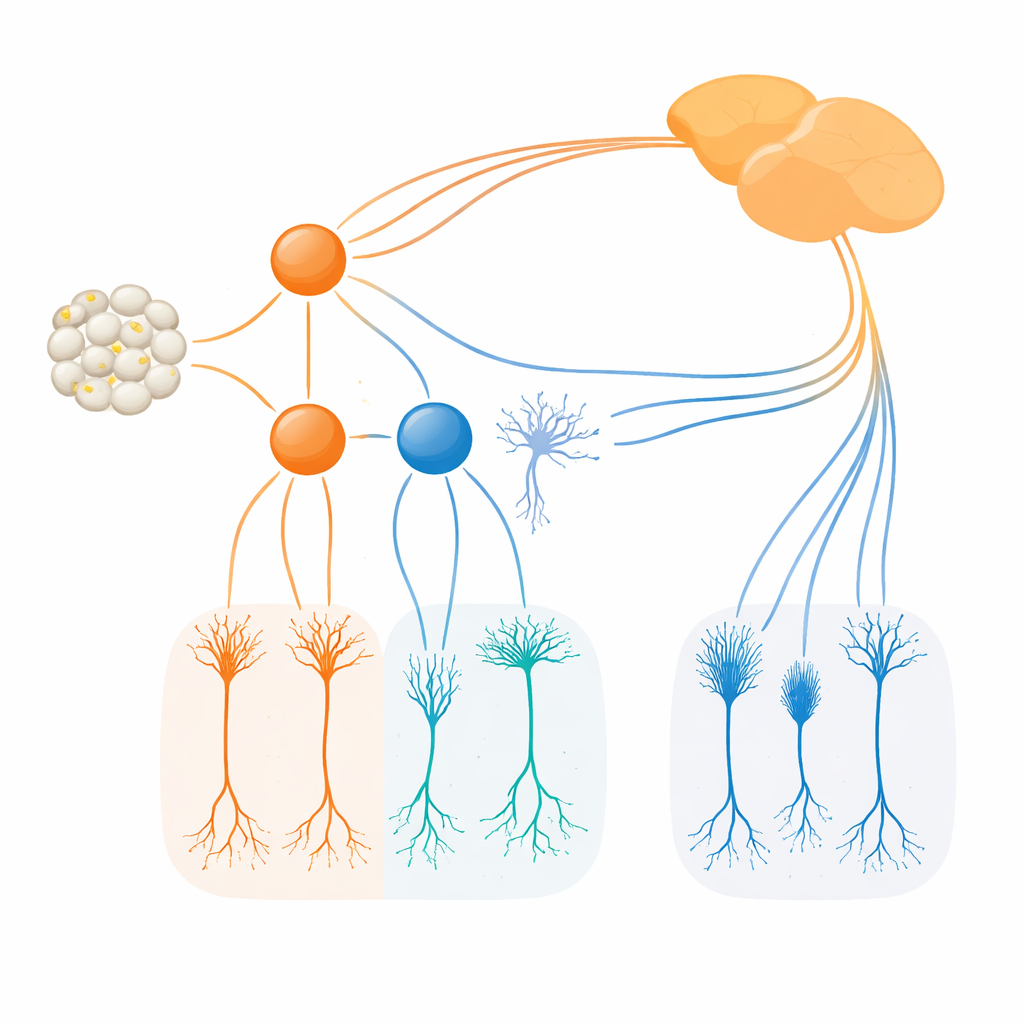
Den Zeitpunkt der Aufspaltung in unterschiedliche Zellfamilien festlegen
Indem sie genetische Reporter an präzisen Embryonaltagen kurzzeitig aktivierten, konnten die Autoren Zellen „zeitstempeln“, die Irx1 oder Tbx20 exprimierten, und ihre Schicksale bis ins Erwachsenenalter verfolgen. Diese Experimente zeigten, dass Tbx20-gekennzeichnete Zellen sich etwas früher als Irx1-gekennzeichnete Zellen für ihre endgültigen ipRGC-Identitäten festlegen, wobei die meisten Entscheidungen knapp vor der Geburt getroffen werden. In einem kurzen Zeitfenster können sowohl Irx1 als auch Tbx20 in einigen Zellen gemeinsam exprimiert werden, und doppelte Knockout-Mäuse, die beide Gene fehlten, zeigten einen deutlich stärkeren Verlust melanopsin-positiver ipRGCs als die einzelnen Mutanten. Das legt nahe, dass die beiden Wege vorübergehend zusammenarbeiten und sich dann trennen, um unterschiedliche Untergruppen von ipRGCs auf separaten Entwicklungsbahnen zu führen.
Was das für das Verständnis von Sehen und Gesundheit bedeutet
Für Nichtfachleute lautet die Kernbotschaft, dass ein frühes Gen, Tbr2, nicht allein wirkt. Stattdessen verzweigt es in zwei parallele Kontrollpfade, einen um Irx1 und einen um Tbx20. Diese Pfade bestimmen, welche Art von ipRGC eine junge Zelle wird, justieren, wie stark sie Licht wahrnimmt, und legen fest, ob sie sich mit Hirnregionen verbindet, die die innere Uhr regulieren, Pupillenreflexe steuern oder andere visuelle Funktionen übernehmen. Die Arbeit liefert ein klareres Schaltbild dafür, wie unsere internen „Lichtmesser“ aufgebaut werden, und hebt spezifische genetische Schritte hervor, die beteiligt sein könnten, wenn diese Zellen verloren gehen oder fehlfunktionieren — mit möglicher Relevanz für Schlafstörungen, saisonale Stimmungsschwankungen und Erkrankungen, die die Netzhaut schädigen.
Zitation: Kiyama, T., Chen, CK., Altay, H.Y. et al. Tbr2-dependent parallel pathways regulate the development of distinct ipRGC subtypes. Commun Biol 9, 347 (2026). https://doi.org/10.1038/s42003-026-09645-4
Schlüsselwörter: retinale Ganglienzellen, Melanopsin, neuronale Entwicklung, zirkadiane Rhythmen, Transkriptionsfaktoren