Clear Sky Science · de
Strukturanalyse zeigt, dass Wassermoleküle die Selbstaktivierung von GPR99 vermitteln
Warum dieser Rezeptor für Entzündungen wichtig ist
Unsere Atemwege und andere Gewebe nehmen ständig chemische Signale wahr, die auf Infektion oder Reizung hindeuten. Ein solcher Sensor ist das auf Zelloberflächen sitzende Protein GPR99, das sich als entscheidender Schalter bei entzündlichen Erkrankungen wie Asthma und Nasenpolypen herauskristallisiert. Diese Studie erklärt auf atomarer Ebene, wie sich GPR99 auch ohne externen chemischen Auslöser selbst einschalten kann — und wie winzige Wassercluster dabei helfen — und liefert Anhaltspunkte für die Entwicklung neuer entzündungshemmender Wirkstoffe.
Ein eingebauter Ein‑Schalter im Zell‑Sensor
GPR99 gehört zu einer großen Familie von Zelloberflächenproteinen, die Signale von außen nach innen weiterleiten, häufig indem sie ihre Form ändern und Partnerproteine namens G‑Proteine anheuern. Im Gegensatz zu den meisten dieser Rezeptoren ist GPR99 ungewöhnlich aktiv, selbst wenn kein Signalmolekül gebunden ist. Die Autoren zeigen, dass eine flexible Schleife auf der Außenseite von GPR99, bekannt als die zweite extrazelluläre Schleife, wie ein innerer Schlüssel wirkt: Sie faltet sich in die übliche Bindungstasche hinein, imitiert ein aktivierendes Signal und schaltet den Rezeptor so eigenständig ein.
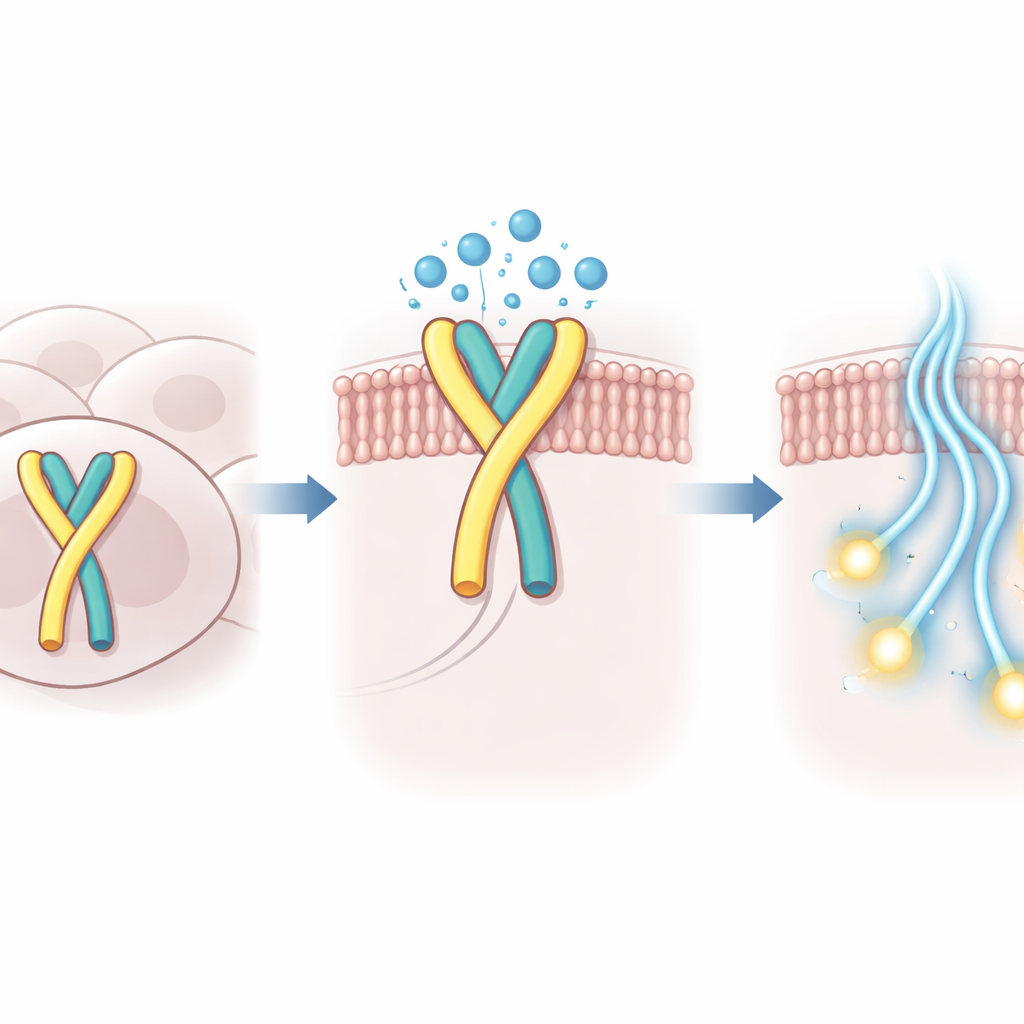
Wie Wasser hilft, den Schalter zu halten
Mithilfe hochauflösender Kryo‑Elektronenmikroskopie hielten die Forscher die dreidimensionale Struktur des menschlichen GPR99 in seinem selbstaktivierten Zustand fest, gebunden an sein G‑Protein‑Partner. In der Bindungstasche, in der sich normalerweise externe Moleküle befinden würden, beobachteten sie neben der eingeklappten Schleife auch einen kleinen Cluster geordneter Wassermoleküle. Diese Wassermoleküle bilden eine polare Brücke zwischen der Schleife und dem umgebenden Protein, kompensieren das flachere Eindringen der Schleife und stabilisieren die aktive Gestalt des Rezeptors. Wenn wichtige Aminosäuren in der Schleife oder in der benachbarten Tasche so verändert wurden, dass diese wassermittelte Kontakte geschwächt wurden, sank die eingebaute Aktivität von GPR99 in zellbasierten Tests deutlich.
Umordnung des inneren Mechanismus für konstantes Signalisieren
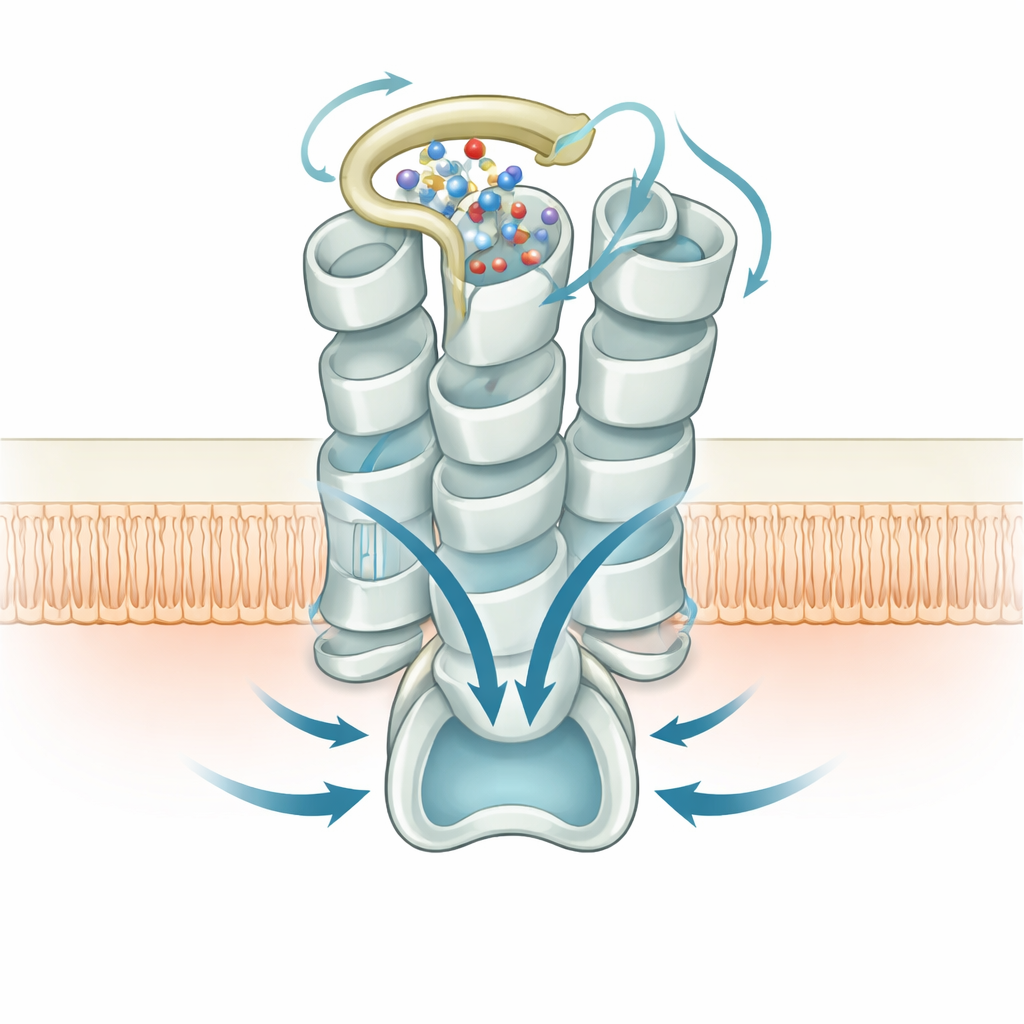
Das Team verglich die selbstaktivierte Struktur mit anderen Familienmitgliedern, darunter einem eng verwandten Rezeptor, der das Stoffwechselzwischenprodukt Succinat bindet, sowie einer aktiven Form von GPR99, die an das Metabolit 2‑Oxoglutarat gebunden ist. Sie fanden heraus, dass GPR99 in Abwesenheit jeglichen externen Liganden bereits vollständig in einer aktivierten Konformation bereitsteht: Mehrere konservierte „Mikroschalter“ in seinem helikalen Kern nehmen Formen an, die normalerweise nur bei Stimulation dieser Rezeptoren zu sehen sind. Kritische Positionen, die Rezeptoren üblicherweise im Aus‑Zustand halten, sind bei GPR99 ersetzt oder neu ausgerichtet, wodurch interne Zwänge gelockert und die offene Konfiguration begünstigt werden, die den G‑Protein‑Partner aufnimmt.
Die Nachricht ins Zellinnere weitergeben
Auf der inneren Seite der Membran zeigt die Struktur, wie GPR99 das Gq‑Typ‑G‑Protein greift, das sein Signal überträgt. Ein helikaler Schwanz des G‑Proteins schmiegt sich in eine durch das Auswärtsdrehen einer von GPR99s Helices geöffnete Kavität und bildet ein Netzwerk aus polaren und hydrophoben Kontakten mit den inneren Schleifen und dem Schwanz des Rezeptors. Mutationen, die diese Schnittstelle stören, reduzieren ebenfalls die Signalübertragung und bestätigen, dass die durch die äußere Schleife und den Wassercluster erzeugte Selbstaktivierung effizient an intrazelluläre Partner gekoppelt ist. Zusammen verknüpfen diese strukturellen Momentaufnahmen Änderungen an der Außenfläche des Rezeptors mit den Calcium‑Signalwellen, die er innerhalb der Zellen auslöst.
Auswirkungen für Atmung und darüber hinaus
Die Autoren schlagen vor, dass die eingebaute Aktivität von GPR99, verstärkt durch strukturelle Wassermoleküle, Gewebe der Atemwege in einen „Bereitschaftsmodus“ versetzen könnte — bereit, Schleim freizusetzen und eine Immunantwort auszulösen, wenn entzündliche Lipide oder metabolische Veränderungen auftreten. Da GPR99 auch ohne externe Signale hochaktiv ist und seine Aktivierung auf einer spezifischen Schleifen‑und‑Wasser‑Anordnung beruht, bieten diese strukturellen Erkenntnisse konkrete Ziele für Wirkstoffdesigner. Kleine Moleküle, die diesen internen Schalter oder sein Wassernetz stören, könnten übermäßige Entzündungen dämpfen, während Verbindungen, die die Wechselwirkung feinabstimmen, die Empfindlichkeit von GPR99 therapeutisch nutzbar machen könnten.
Zitation: Xiao, M., Bao, X., Guo, Y. et al. Structural analysis reveals that water molecules mediate self-activation of GPR99. Commun Biol 9, 342 (2026). https://doi.org/10.1038/s42003-026-09644-5
Schlüsselwörter: GPR99, GPCR‑Aktivierung, Strukturelle Biologie, Entzündung, wassermittelte Signalübertragung