Clear Sky Science · de
Struktureller Mechanismus, wie anti‑MHC‑I‑Antikörper inhibitorische NK‑Zell‑Rezeptoren in der Tumorimmunität blockieren
Die stillen Krebskiller des Körpers aktivieren
Unser Immunsystem verfügt über mächtige Wächter, die sogenannten natürlichen Killer (NK)-Zellen, die Krebszellen und virusinfizierte Zellen erkennen und zerstören können. Tumoren schaffen es jedoch oft, diese Wächter stummzuschalten. Diese Arbeit zeigt auf atomarer Ebene, wie ein speziell entwickelter Antikörper diese „Stummschaltung“ entfernen und NK‑Zellen wieder wecken kann, sodass sie Tumoren effektiver angreifen. Die Studie verbindet hochmoderne Strukturbiologie mit Experimenten an Mäusen und demonstriert, wie ein Antikörper bestehende Krebsimmuntherapien ergänzen könnte.
Die Immun‑ID‑Schilder auf unseren Zellen
Jede Zelle unseres Körpers trägt molekulare „ID‑Schilder“ auf ihrer Oberfläche, die MHC‑Klasse‑I‑Moleküle genannt werden. Diese Schilder helfen den Immunzellen, normales Gewebe von gefährlichen Zellen zu unterscheiden, die krebsartig geworden oder von Viren infiziert sind. NK‑Zellen scannen diese Schilder kontinuierlich. Wenn sie normale Muster wahrnehmen, senden inhibitorische Rezeptoren auf NK‑Zellen ein beruhigendes Signal, das einen Angriff verhindert. Tumoren halten diese Schilder häufig sichtbar und nutzen sie als Schutzschild: Solange das inhibitorische Signal fließt, halten NK‑Zellen inne und der Krebs kann wachsen.
Ein Antikörper, der das Schutzschild ergreift
Die Forscher untersuchten einen monoklonalen Antikörper namens B1.23.2, der stark an viele menschliche MHC‑Klasse‑I‑Varianten auf Tumorzellen bindet. Mithilfe von Kryo‑Elektronenmikroskopie und Röntgenkristallographie kartierten sie genau, wie dieser Antikörper auf der MHC‑Oberfläche sitzt. B1.23.2 heftet sich an eine konservierte Kante des MHC‑Moleküls—eine α2‑Helix—ohne das Leichtkettenpartner zu berühren und nur geringfügig das präsentierte Peptid zu erfassen. Das bedeutet, dass der Antikörper eine breite Palette menschlicher MHC‑A, ‑B und ‑C‑Moleküle mit sehr hoher Affinität erkennen kann, während er relativ unempfindlich gegenüber den spezifischen kurzen Proteinfragmenten ist, die das MHC präsentiert.
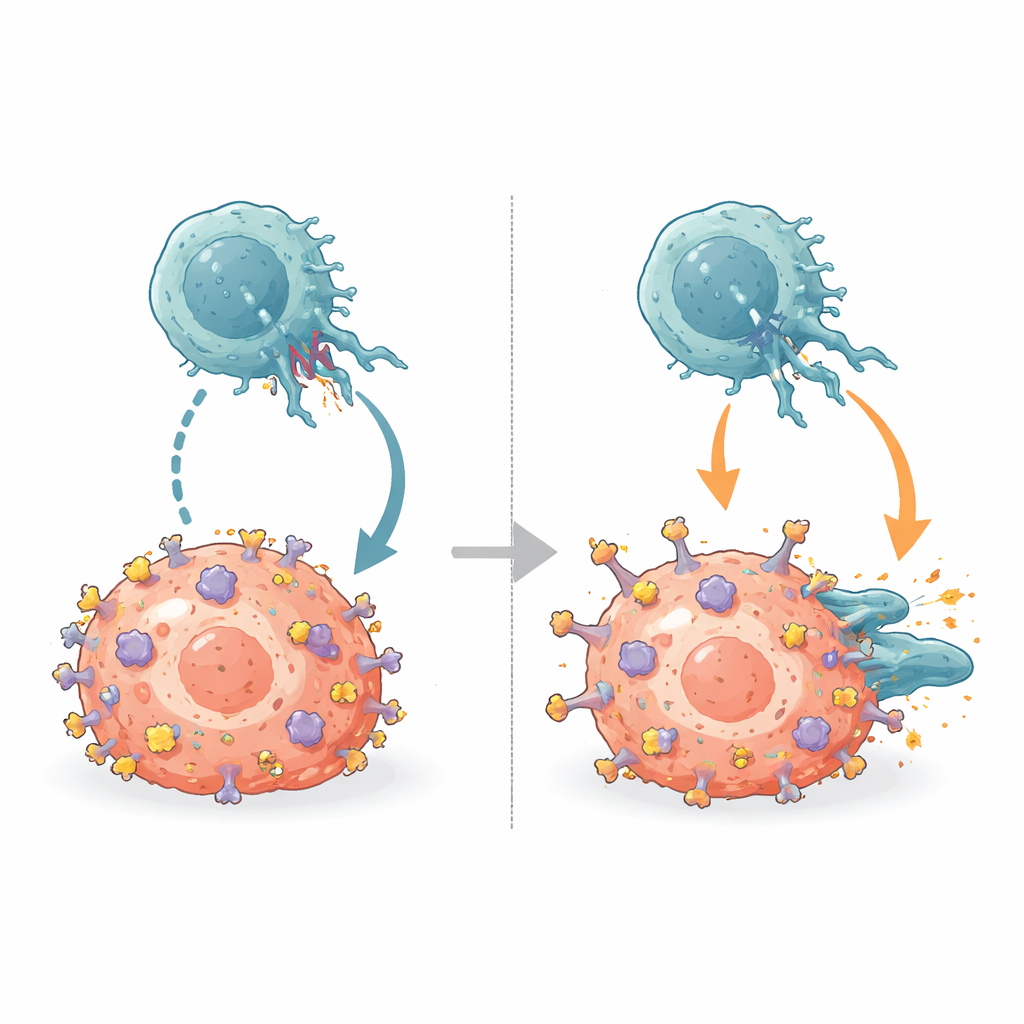
Die Immunbremsen übertrumpfen
NK‑Zellen tragen inhibitorische Rezeptoren, die KIRs genannt werden und normalerweise auf derselben α2‑Kante des MHC andocken. Durch das Ausrichten der neuen Antikörper–MHC‑Strukturen mit bekannten KIR–MHC‑Strukturen zeigte das Team, dass B1.23.2 physisch genau die Stelle des MHC besetzt, an der KIRs greifen müssen. Die Bindungsstelle des Antikörpers und die KIR‑Kontaktflächen überlappen so weitreichend, dass beide nicht gleichzeitig binden können. B1.23.2 bindet außerdem mit höherer Affinität an MHC als KIRs, wodurch es in diesem molekularen Tauziehen gewinnt. Folglich können KIRs auf NK‑Zellen, wenn der Antikörper die MHC‑Moleküle der Tumorzelle umhüllt, ihre inhibitorischen Signale nicht mehr übermitteln, und das Gleichgewicht verschiebt sich zugunsten der NK‑Zell‑Aktivierung.
Feinabstimmung der Passform und breite Reichweite
Obwohl B1.23.2 hauptsächlich die konservierte MHC‑Oberfläche anvisiert, stellten die Autoren fest, dass kleine Unterschiede im MHC‑gebundenen Peptid die Antikörperstärke subtil modulieren können. Durch systematisches Austauschen einer einzelnen Aminosäureposition im Peptid zeigten sie moderate Änderungen in der Bindung—im Allgemeinen innerhalb von etwa dem Zehnfachen—ohne den allgemeinen Erkennungscharakter zu verlieren. Sie untersuchten auch, warum bestimmte verbreitete MHC‑Typen, wie HLA‑A*02:01, der Bindung entgehen. Durch Einsetzen entscheidender Kontaktreste aus einer reagierenden MHC‑Variante in HLA‑A*02:01 erzeugte das Team Versionen, die der Antikörper nun erkennen konnte, und bestätigte so genau, welche Positionen die kritische Andockfläche bilden. Diese Erkenntnisse deuten darauf hin, dass künftige Antikörpervarianten so gestaltet werden könnten, noch mehr MHC‑Typen abzudecken oder gezielt andere zu umgehen.
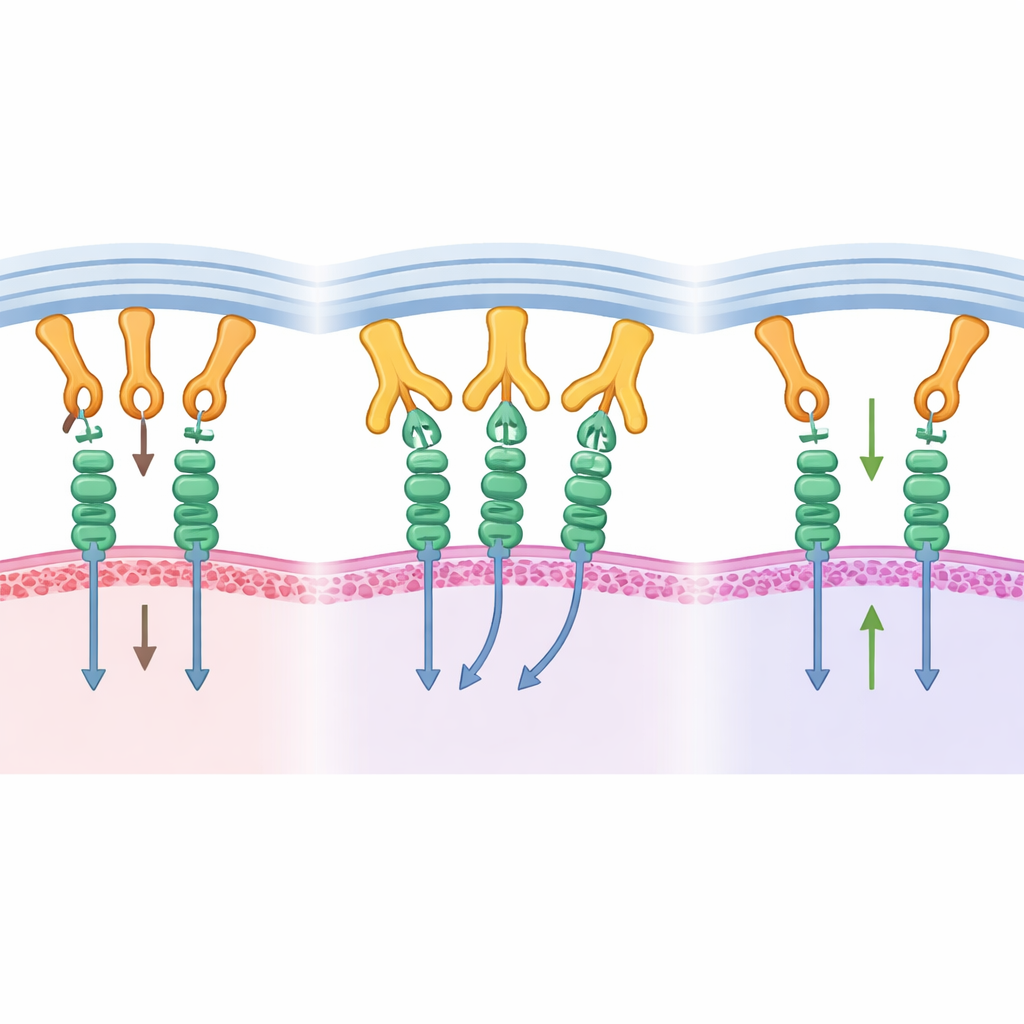
Strukturelle Einsicht in Tumorkontrolle umsetzen
Hilft dieses molekulare Blockieren tatsächlich beim Kampf gegen Tumoren? Um das zu testen, verwendeten die Forscher ein humanisiertes Mausmodell mit menschlichem Bauchspeicheldrüsenkrebs. Sie konstruierten eine Form von B1.23.2, die über ihren eigenen Fc‑Teil keine Effektorfunktionen auslösen kann, sodass etwaige Effekte hauptsächlich aus der Blockade der MHC–KIR‑Interaktion resultieren würden. Wenn Mäuse den Antikörper zusammen mit menschlichen NK‑Zellen erhielten, wuchsen die Tumoren deutlich langsamer. NK‑Zellen zeigten vermehrte Proliferation, erhöhte Aktivität von Wachstums‑ und Signalwegen sowie eine gesteigerte Produktion entzündlicher Moleküle, die mit dem Abtöten von Krebszellen assoziiert sind. Innerhalb der Tumoren wiesen NK‑Zellen mehr aktivierende Rezeptoren auf, was mit einer Befreiung von konstanten inhibitorischen Signalen konsistent ist.
Was das für künftige Krebstherapien bedeuten könnte
Einfach gesagt zeigt diese Studie, wie ein einzelner Antikörper sich zwischen Tumorzellen und die Bremsen des Immunsystems schieben kann und so das „Nicht angreifen“-Signal stoppt, das NK‑Zellen normalerweise ruhigstellt. Indem die Interaktion in atomarer Auflösung abgebildet und ihre Wirkung in Tieren bestätigt wurde, liefert die Arbeit einen Bauplan für eine neue Klasse von Therapeutika: Antikörper, die an die ID‑Schilder des Tumors binden statt an die Immunrezeptoren selbst. Solche Wirkstoffe könnten mit bestehenden Checkpoint‑Inhibitoren oder Zelltherapien kombiniert werden, um sowohl NK‑ als auch T‑Zellen zu mobilisieren und dem Immunsystem einen weiteren Angriffswinkel gegen schwer behandelbare Krebserkrankungen zu geben.
Zitation: Jiang, J., Panda, A.K., Natarajan, K. et al. Structural mechanism of anti-MHC-I antibody blocking of inhibitory NK cell receptors in tumor immunity. Commun Biol 9, 350 (2026). https://doi.org/10.1038/s42003-026-09641-8
Schlüsselwörter: natürliche Killerzellen, MHC Klasse I, Krebsimmuntherapie, monoklonale Antikörper, inhibitorische Rezeptoren