Clear Sky Science · de
LukS-PV, das auf C5aR abzielt, hemmt EMT im hepatozellulären Karzinom über die BCL6/HDAC6/HSPD1-Achse
Aus einer bakteriellen Waffe einen Krebsbekämpfer machen
Das hepatozelluläre Karzinom, die häufigste Form von Leberkrebs, ist oft tödlich, weil es sich von der Leber auf andere Organe ausbreitet. Diese Arbeit untersucht einen unerwarteten Verbündeten gegen diese Ausbreitung: ein Protein, LukS-PV, das ursprünglich Teil eines von Staphylococcus aureus produzierten Toxins ist. Die Forschenden zeigen, wie dieses Protein an einen bestimmten Rezeptor auf Leberkrebszellen bindet und statt normales Gewebe zu schädigen, zentrale Schritte blockiert, die es Krebszellen erlauben, sich zu lösen, zu wandern und neue Tumoren zu bilden.
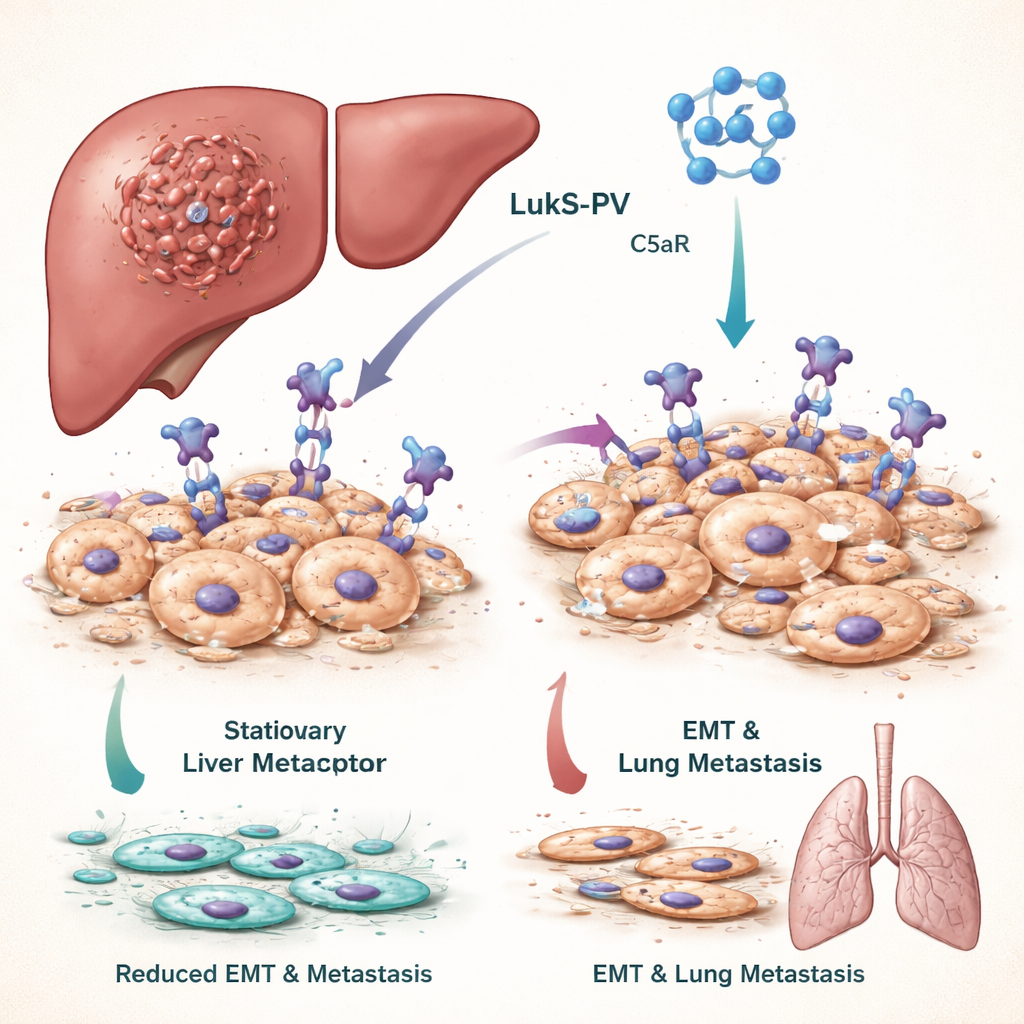
Warum es wichtig ist, formwandelnde Krebszellen zu stoppen
Damit Leberkrebs metastasiert, müssen Tumorzellen einen dramatischen Formen- und Verhaltenswechsel durchlaufen, die epithelial–mesenchymale Transition (EMT). Bei der EMT werden eng gepackte Zellen, die normalerweise sesshaft bleiben, flexibler, mobiler und invasiver, was es ihnen ermöglicht, in Blutgefäße einzudringen und ferne Organe wie die Lunge zu besiedeln. Patientinnen und Patienten, deren Tumoren starke EMT-Aktivität zeigen, haben tendenziell schlechtere Prognosen. Das Team konzentrierte sich auf einen Signalweg, der von dem Molekül C5a und seinem Rezeptor C5aR angetrieben wird; dieser Rezeptor ist auf vielen Tumorzellen ungewöhnlich häufig vorhanden und ist dafür bekannt, EMT und Metastasierung zu fördern.
Eine Toxinkomponente, die ein Krebs-Signal ins Visier nimmt
Panton–Valentine-Leukozidin, ein Toxin von Staphylococcus aureus, enthält die Komponente LukS-PV, die natürlicherweise C5aR erkennt und bindet. Frühere Studien der Autorinnen und Autoren zeigten, dass eine rekombinante, nicht porenbildende Version von LukS-PV das Wachstum mehrerer Krebsarten dämpfen kann, ohne in Tierversuchen offensichtliche Toxizität zu verursachen. In dieser Studie behandelten sie Leberkrebszelllinien mit LukS-PV und beobachteten, dass die Zellen weniger migrations- und invasionsfreudig wurden. Molekulare Tests zeigten, dass Marker für stationäre, gut differenzierte Zellen zunahmen, während Marker für aggressive, mobile Zellen abnahmen. In Mäusen, die mit Leberkrebszellen injiziert wurden, führte die Behandlung mit LukS-PV zu deutlich weniger Tumorknoten in der Lunge, was auf eine reduzierte Metastasierung hinweist.
Unterbrechung einer Kettenreaktion innerhalb der Tumorzellen
Bei tiefer gehenden Untersuchungen entdeckten die Forschenden eine Kette von Regulatorproteinen innerhalb der Krebszellen, die durch LukS-PV gestört wird. Zunächst bindet LukS-PV an C5aR auf der Zelloberfläche und blockiert so effektiv das pro-metastatische Signal von C5a. Diese Abschwächung der C5aR-Signalgebung senkt die Menge eines Proteins namens BCL6, eines Transkriptionsfaktors, der normalerweise bestimmte Gene im Zellkern aktiviert. Eines der Ziele von BCL6 ist HDAC6, ein Enzym, das kleine chemische Markierungen, sogenannte Acetylgruppen, von anderen Proteinen entfernt. Wenn BCL6 reichlich vorhanden ist, steigen die HDAC6-Spiegel, und die Zelle neigt eher zu EMT und Migration. Die Störung von C5aR durch LukS-PV reduziert BCL6, wodurch die HDAC6-Produktion sinkt und dieses pro-metastatische Programm verlangsamt wird.
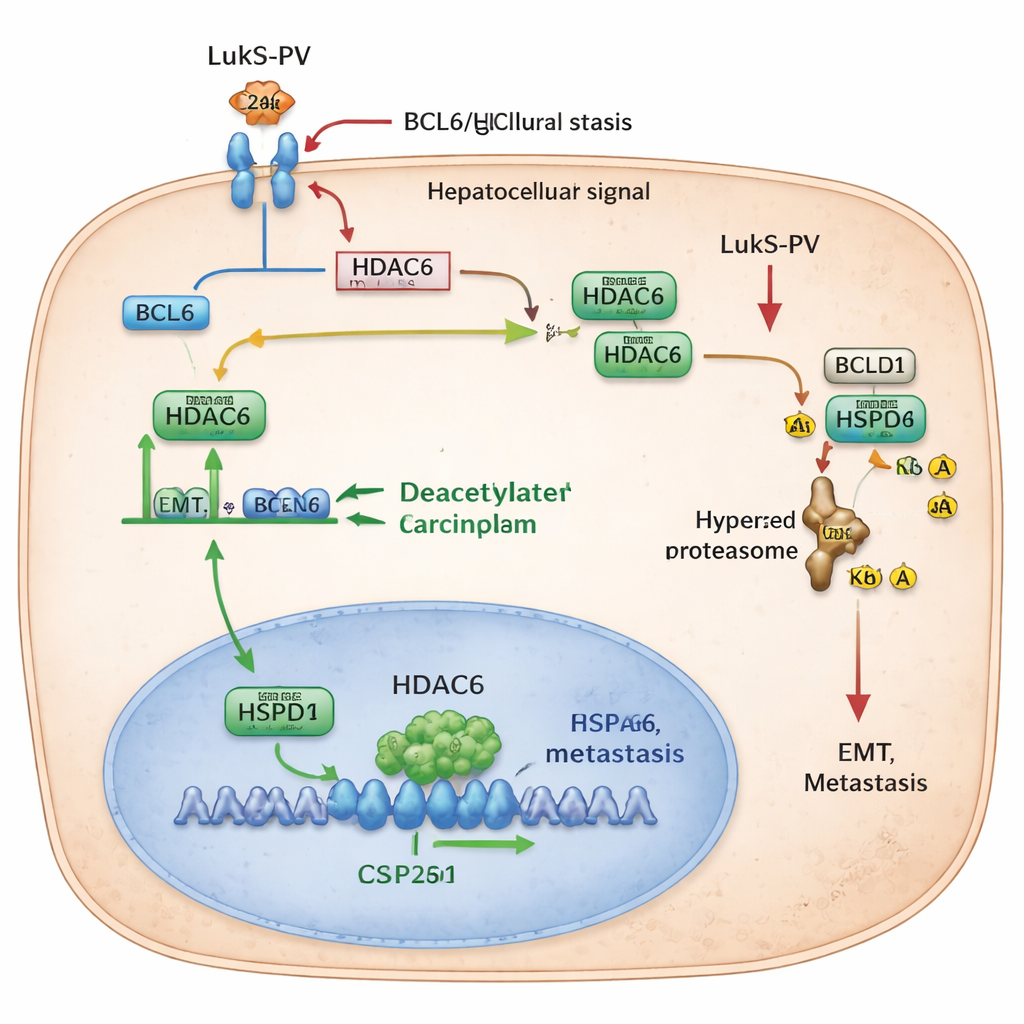
Ein Chaperon zur Zerstörung markieren
Das Team identifizierte anschließend einen wichtigen Partner von HDAC6, genannt HSPD1, auch bekannt als HSP60, ein „Chaperon“-Protein, das anderen Proteinen beim Falten und Stabilbleiben hilft. In Leberkrebs sind die HSPD1-Spiegel höher als im umliegenden normalen Gewebe und mit schlechterer Überlebensprognose verbunden. Die Forschenden fanden heraus, dass HDAC6 physikalisch mit HSPD1 interagiert und Acetylgruppen von zwei spezifischen Positionen daran entfernt. Wenn diese Acetylmarken entfernt werden, wird HSPD1 stabiler und unterstützt EMT und Metastasierung. Wird HDAC6 reduziert—entweder durch genetische Manipulationen oder durch LukS-PV-Behandlung—wird HSPD1 stärker acetylisiert. Diese hyperacetylierte Form wird von der zellulären Müllentsorgungsmaschinerie erkannt, mit Ubiquitin markiert und abgebaut. Mit abnehmenden HSPD1-Spiegeln verlieren Krebszellen einen Teil ihrer Fähigkeit zu migrieren, zu invasieren und die Lunge zu kolonisieren.
Von komplexen Signalwegen zu einer einfachen Schlussfolgerung
Für Nicht-Spezialisten lautet die Botschaft: Die Autorinnen und Autoren haben eine Dominofolge in Leberkrebszellen beschrieben: Ein Oberflächenrezeptor (C5aR) steigert ein Steuerprotein (BCL6), das wiederum ein Enzym (HDAC6) erhöht, welches ein Chaperon (HSPD1) davor bewahrt, abgebaut zu werden. Gemeinsam helfen diese Akteure den Krebszellen, ihre Form zu verändern, sich zu bewegen und zu streuen. LukS-PV, ein im Labor umgenutztes bakterielles Protein, unterbricht diese Sequenz direkt an der Zelloberfläche und führt letztlich zum Abbau von HSPD1 und zu einer Bremse der Metastasierung. Obwohl die Befunde noch experimentell sind, deutet diese Arbeit darauf hin, dass Medikamente, die nach dem Vorbild von LukS-PV entwickelt werden—or auf BCL6, HDAC6 oder HSPD1 abzielen—neue Wege bieten könnten, die Ausbreitung von Lebertumoren zu verhindern und die Prognose von Patientinnen und Patienten zu verbessern.
Zitation: Ding, P., Shi, L., Xu, X. et al. LukS-PV targeting C5aR inhibits EMT in hepatocellular carcinoma via the BCL6/HDAC6/HSPD1 axis. Commun Biol 9, 314 (2026). https://doi.org/10.1038/s42003-026-09640-9
Schlüsselwörter: hepatozelluläres Karzinom, Metastasen, epithelial-mesenchymale Transition, HDAC6, bakterielle Toxintherapie