Clear Sky Science · de
Periodische eingeschränkte Zellmigration treibt teilweise reversible Chromatinumorganisation in Krebszelllinien voran
Wie zusammengedrückte Krebszellen sich an Stress „erinnern“
Krebszellen, die sich von einem Tumor lösen, müssen durch winzige Spalte im Gewebe und in Blutgefäßen kriechen. Dabei quetschen sie ihr weiches Inneres — und insbesondere ihren Zellkern, der die DNA enthält — durch Räume, die manchmal kleiner sind als der Kern selbst. Diese Studie untersucht, was mit der Verpackung der DNA bei diesen wiederholten Quetschungen passiert und stellt eine zentrale Frage: Federte der Kern einfach wieder in den Normalzustand zurück, oder bleibt eine Art „mechanisches Gedächtnis“ zurück, das das Tumorgeschehen fördern könnte?
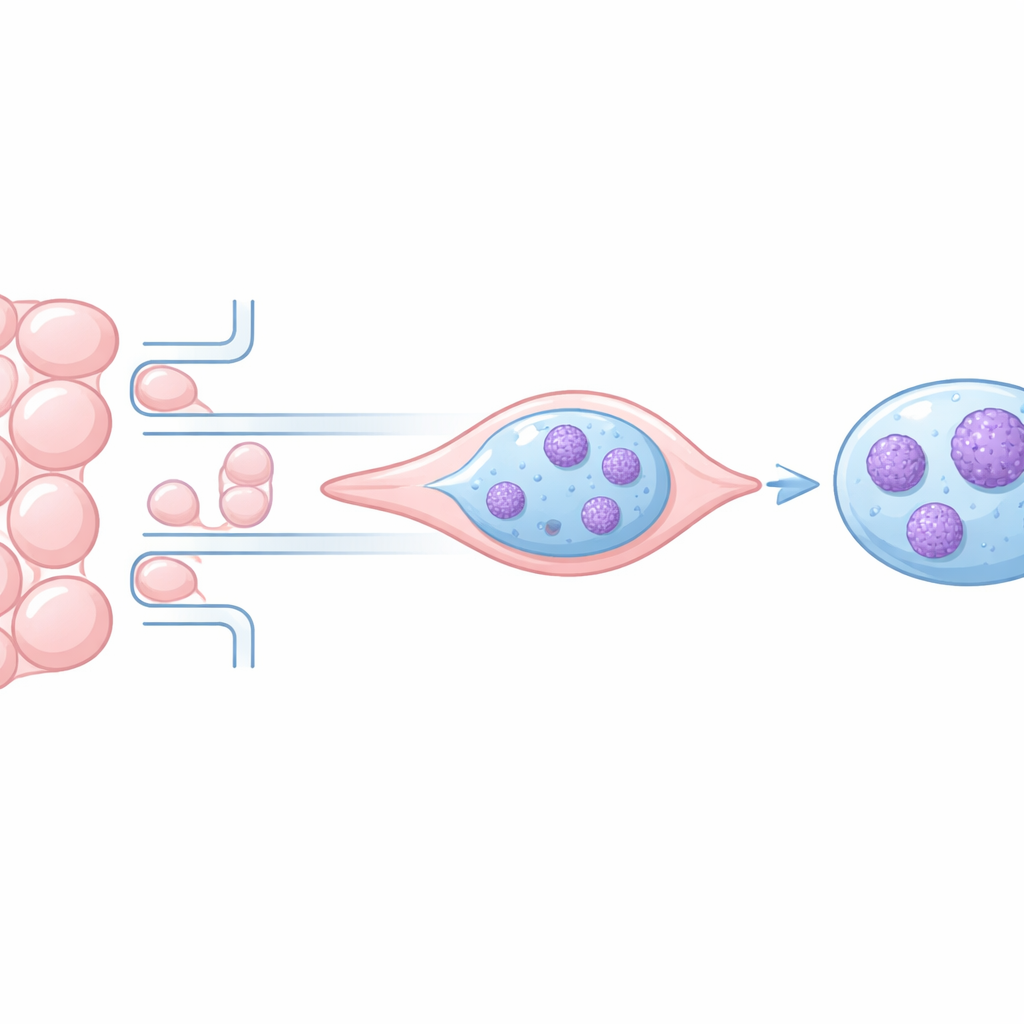
Warum die DNA-Packung beim Zellwandern wichtig ist
Im Zellkern ist die DNA um Proteine gewickelt und zu Chromatin gefaltet, das locker verpackt oder eng kondensiert sein kann. Lockerere Regionen sind meist aktiv und beherbergen häufig genutzte Gene, während dicht gepackte Regionen eher still sind. Wenn Zellen durch enge Spalte wandern, verformen sich die Kerne, und frühere Arbeiten zeigten, dass dies Chromatin vorübergehend verdichten und sogar DNA schädigen kann. Unklar war jedoch, ob diese Veränderungen vollständig reversibel sind oder bleibende Spuren hinterlassen, die das Aggressivitätsverhalten von Krebszellen verändern könnten.
Ein winziges Labyrinth, um einzelne Krebszellen zu quetschen
Die Forschenden konstruierten ein maßgeschneidertes mikrofluidisches Gerät — einen transparenten Chip mit Dutzenden mikroskopischer Kanäle, die abwechselnd breite und enge Abschnitte aufweisen. Zwei verschiedene Krebszelllinien, beide so verändert, dass ihr Chromatin im Mikroskop fluoresziert, wurden mithilfe eines chemischen Lockstoffs dazu gebracht, durch diese Kanäle zu kriechen. Hochauflösende Zeitrafferaufnahmen ermöglichten es dem Team, jeden Zellkern während der Bewegung zu verfolgen, die Kerngröße zu messen und helle, stark kondensierte Chromatincluster Bild für Bild in mehr als 100 einzelnen Zellen zu kartieren.
Was mit dem Kern unter Druck geschieht
Sobald eine Zelle in einen engen Engpass gelangte, verringerte sich die projizierte Kernfläche abrupt, was einer reversiblen Reduktion des Kernvolumens entsprach. Gleichzeitig stieg der Anteil des Kerns, der von stark kondensiertem Chromatin eingenommen wurde — oft um das Zwei- bis Dreifache — und fiel wieder auf das Ausgangsniveau, sobald die Zelle in einen breiteren Bereich gelangte. Dieses Muster wiederholte sich über mehrere aufeinanderfolgende Engstellen und in beiden Zelltypen, was darauf hindeutet, dass die Gesamtmenge dichten Chromatins eine flexible, kurzfristige Reaktion auf mechanischen Stress ist und keine dauerhafte Veränderung. Eine genauere Betrachtung der Fluoreszenzmuster zeigte jedoch, dass Pixel mit sehr hohen und sehr niedrigen Intensitäten während des Quetschens zunahmen, was auf eine komplexere interne Umordnung hindeutet als eine einfache, gleichmäßige Kompaktierung.
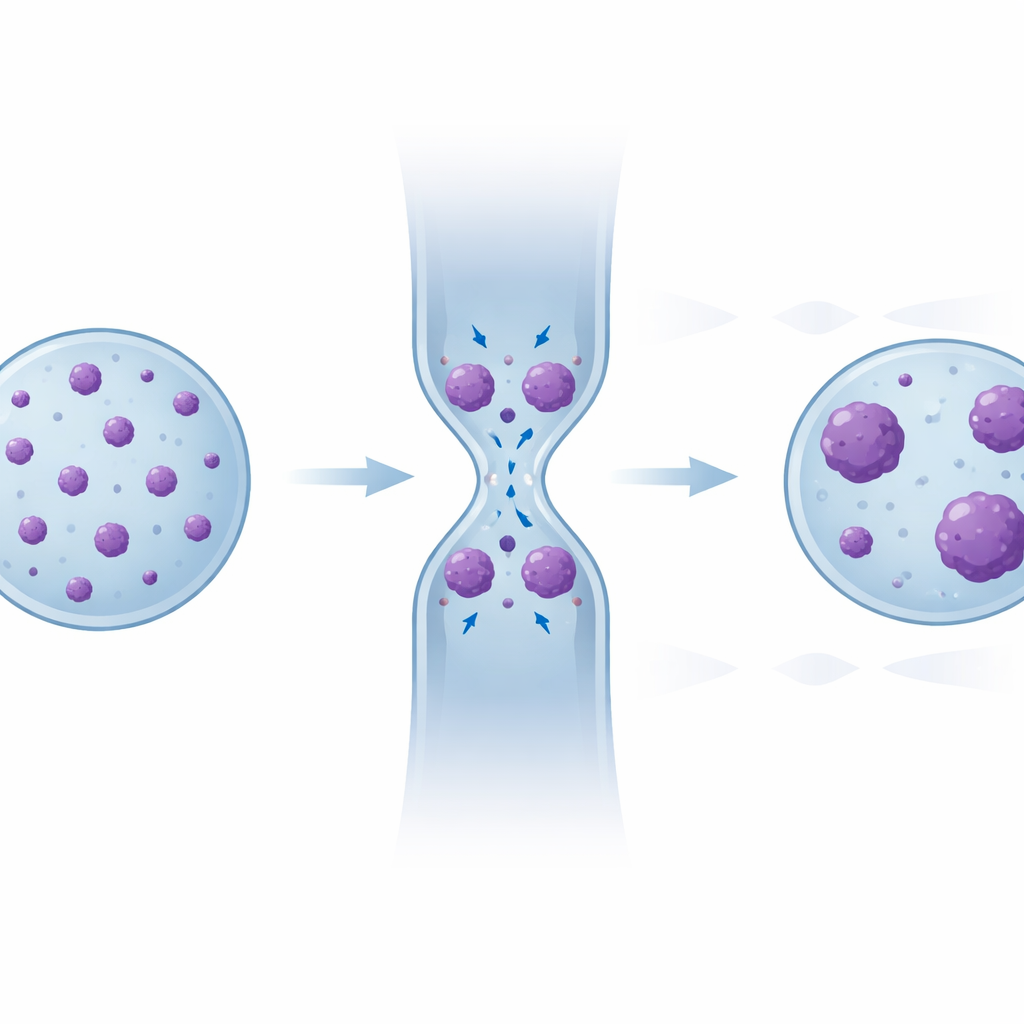
Verborgenes Gedächtnis im Muster der DNA‑Cluster
Um diese verborgene Umorganisation aufzudecken, untersuchten die Forschenden jeden einzelnen kondensierten Chromatincluster — dessen Größe und wie viele solcher Cluster jeder Kern enthielt — vor, während und nach der Einschränkung. Beim Quetschen neigten kleine Cluster dazu, sich zu größeren zusammenzufinden. Nachdem sich der Kern entspannt hatte, kehrte die gesamte kondensierte Fläche zu ihrem ursprünglichen Niveau zurück, doch das Muster tat es nicht: Im Vergleich zum Ausgangszustand zeigten Zellen, die mehrere Engstellen passiert hatten, insgesamt weniger Cluster, mit einer Verlagerung hin zu größeren Größen. Statistische Vergleiche bestätigten, dass die Verteilungen in späteren "Erholungs"-Bereichen zunehmend denen während der Einschränkung ähnelten. Immunfluoreszenzfärbungen zeigten außerdem, dass viele dieser dichten Bereiche mit etablierten Markern für "stilles" Chromatin überlappten, und ein Computermodell, das Chromatin als interagierendes Polymer darstellt, reproduzierte diese teilweise, aber nicht vollständige Entspannung allein aus der Physik klebriger DNA‑Segmente, die durch Deformation zusammengebracht wurden.
Was das für Krebsverbreitung und künftige Therapien bedeutet
Vereinfacht gesagt zeigt die Studie, dass sich bei wiederholtem Quetschen von Krebszellkernen deren DNA‑Packung wie ein Stressball mit Erinnerung verhält. Der Kern kann in der Größe zurückspringen, und die Gesamtmenge an dichter Packung kann sich zurücksetzen, aber das detaillierte Muster dichter DNA‑Klumpen kehrt nicht vollständig in den Ursprungszustand zurück. Über viele Quetschzyklen hinweg verbleibt der Kern mit weniger, dafür größeren dichten Regionen, was potenziell verändert, welche Gene leichter oder schwerer zugänglich sind. Dieses „mechanische Gedächtnis“ könnte Krebszellen dabei helfen, zukünftige Deformationen besser zu tolerieren, während sie in neues Gewebe eindringen. Das Verständnis und die gezielte Störung dieser Kopplung zwischen physikalischen Kräften und DNA‑Organisation könnten neue Wege eröffnen, die Metastasierung zu begrenzen, indem man stört, wie Krebszellen sich an mechanischen Stress anpassen.
Zitation: Blazquez-Romero, M.d.V., Mendivil-Carboni, M., Sarasquete-Martinez, M. et al. Periodic confined cell migration drives partially reversible chromatin reorganization in cancer cell lines. Commun Biol 9, 366 (2026). https://doi.org/10.1038/s42003-026-09637-4
Schlüsselwörter: eingeschränkte Zellmigration, Chromatinkondensation, nukleare Mechanik, mechanisches Gedächtnis, Krebsmetastase