Clear Sky Science · de
PTBP1 unterstützt die Spermienbildung bei Mäusen, indem es in Sertoli-Zellen die Organisation des Zytoskeletts über den mTORC2–PKCα-Weg erleichtert
Warum diese Studie für die männliche Fruchtbarkeit wichtig ist
Männliche Unfruchtbarkeit wirkt oft rätselhaft, beruht aber im Kern auf einer fein abgestimmten Partnerschaft zwischen sich entwickelnden Spermien und den „Pflege“-Zellen, die sie unterstützen. Diese Studie geht einem der verborgenen molekularen Helfer in diesen Pflegezellen nach und zeigt, wie dessen Ausfall die Spermienproduktion zum Erliegen bringen kann. Das Verständnis dieser verborgenen Steuerungsebene könnte den Weg zu neuen Diagnosen oder Behandlungen bestimmter Formen männlicher Unfruchtbarkeit weisen.
Die Stützzellen, die Spermien möglich machen
Spermien entstehen in den langen, gewundenen Kanälen des Hodens, den Samenkanälchen (Tubuli seminiferi). Diese Kanäle sind von Sertoli-Zellen ausgekleidet, einem spezialisierten Zelltyp, der die sich entwickelnden Keimzellen umhüllt, ernährt und beim Teilen und Reifen zu Spermien führt. Sertoli-Zellen bilden außerdem eine Schutzwand, die Blut–Hoden-Schranke, die frühe Zellstadien vom Immunsystem trennt. Dafür sind sie auf ein inneres Gerüst aus Aktinfilamenten und Mikrotubuli angewiesen, das sich ständig umbaut, während Wellen von Keimzellen durch die Tubuli wandern. Wird dieses Gerüst gestört, beginnt die Barriere zu lecken, sich entwickelnde Keimzellen können sich lösen oder absterben, was die Fruchtbarkeit gefährdet.
Ein kleiner RNA-Manager mit großer Aufgabe
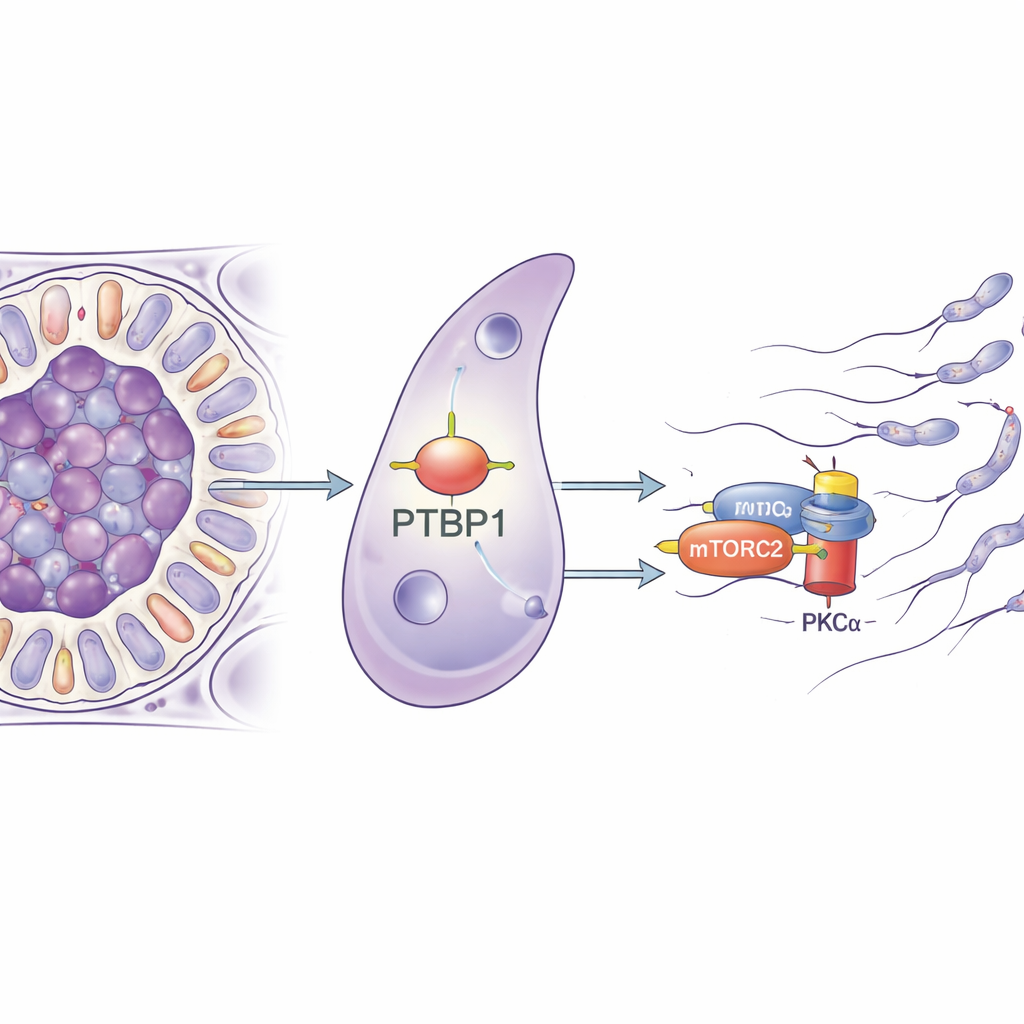
Die Forschenden konzentrierten sich auf ein Protein namens PTBP1, das vor allem für seine Rolle bei der Steuerung von RNA-Molekülen in Zellen bekannt ist — es beeinflusst, wie Gene gespleißt werden, wie stabil ihre Botschaften sind und wie effizient sie in Protein umgesetzt werden. PTBP1 ist sowohl in Keimzellen als auch in Sertoli-Zellen reichlich vorhanden, und frühere Arbeiten zeigten, dass sein Entfernen aus Keimzellen die Spermienproduktion beeinträchtigt. In dieser Studie entfernte das Team PTBP1 gezielt nur in Sertoli-Zellen von Mäusen. Auf den ersten Blick wirkten die jungen Tiere normal, doch mit Erreichen der Geschlechtsreife schrumpften ihre Hoden, die Spermienzahl im Nebenhoden fiel drastisch und keiner der Männchen zeugte Nachkommen — ein vollständiger Verlust der Fruchtbarkeit.
Wenn das zelluläre Gerüst zusammenbricht
Mikroskopische Untersuchungen der Hoden dieser Mäuse zeigten, dass die Spermatogenese mitten im Prozess stehen blieb. Viele Tubuli wiesen Hohlräume, abnorme Klumpen verschmolzener Keimzellkerne und einen Mangel an vollständig verlängerten Spermien auf. Die Kerne der Sertoli-Zellen, die normalerweise an der Außenwand der Tubuli liegen, waren vielfach zur Mitte verschoben, was darauf hinweist, dass diese Stützzellen ihren Halt an der Umgebung verloren. Färbungen für wichtige Verbindungs- und Strukturproteine bestätigten, dass die Blut–Hoden-Schranke geschwächt war und die sonst dicht gebündelten Aktinfilamente durch desorganisierte, übermäßig intensive Stränge ersetzt worden waren, die vom Grund bis zur Mitte des Tubulus verliefen. Ein Tracer-Molekül, das normalerweise auf der „Blut“-Seite der Barriere verbleibt, trat stattdessen tief in die Tubuli ein und demonstrierte so direkt den Zusammenbruch der Barriere.
Die Fehlfunktion bis zu einem Signalzentrum zurückverfolgen
Um zu verstehen, wie ein RNA-bindendes Protein solche mechanischen Probleme verursachen kann, isolierte das Team Sertoli-Zellen und analysierte, welche Gene ihre Aktivität änderten, wenn PTBP1 fehlte. Viele betroffene Gene waren an der Kontrolle des zellulären Gerüsts und an Zelladhäsion beteiligt, was auf einen weitreichenden Umbaufehler hinwies. Die Forschenden identifizierten anschließend die RNA-Moleküle, die physisch an PTBP1 binden, und fanden, dass es an die Botschaft für Rictor bindet, einen Kernbestandteil eines Signalcomplexes namens mTORC2. Dieses Complex aktiviert wiederum ein Enzym namens PKCα, das die Aktinfilamente formt. In Sertoli-Zellen ohne PTBP1 sank die Menge an RICTOR-Protein, und PKCα war deutlich weniger aktiv, obwohl das Rictor-RNA-Niveau kaum verändert war. Das legt nahe, dass PTBP1 Sertoli-Zellen dabei hilft, ausreichend RICTOR-Protein aus seiner RNA-Botschaft zu produzieren und so den mTORC2–PKCα-Weg funktionsfähig hält.
Das Gerüst durch Wiederherstellung des Signals retten
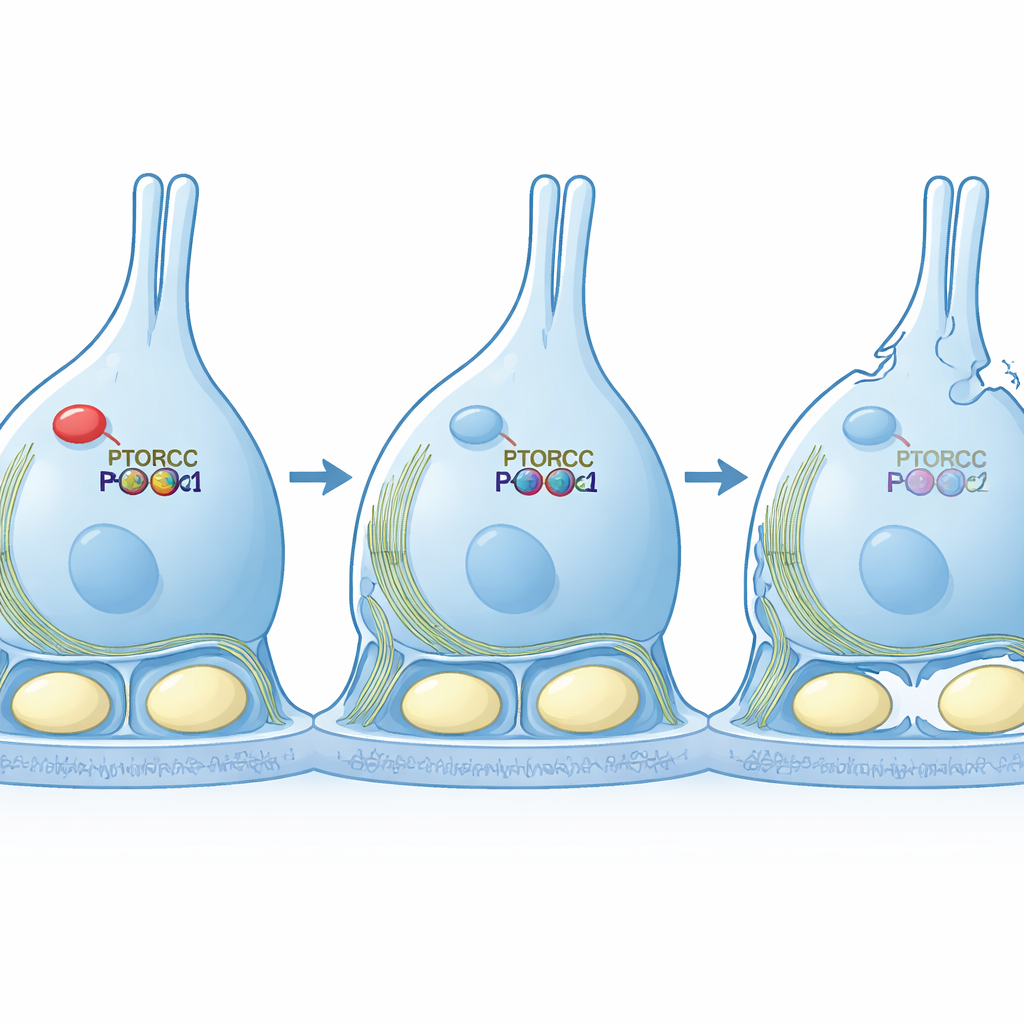
Das Team ging dann in Zellkulturmodelle, um Kausalität zu prüfen. Reduzierten sie PTBP1 in einer Sertoli-ähnlichen Zelllinie, streckten sich die Zellen zu langen, dünnen Formen und zeigten ein durcheinander geratenes Aktinnetz — Kennzeichen eines geschwächten mTORC2-Signals. Wichtig ist: Wenn sie diese Zellen dazu zwangen, eine permanent aktive Version von PKCα zu produzieren, erlangten die Zellen wieder ihre kompakte Form und geordnetere Aktinstrukturen, obwohl RICTOR selbst niedrig blieb. Dieses Rettungs-Experiment zeigt, dass die Hauptaufgabe von PTBP1 in diesem Kontext darin besteht, den mTORC2–PKCα-Weg stark genug zu halten, um das innere Gerüst der Zelle zu organisieren.
Was das Verständnis von Unfruchtbarkeit bedeutet
Einfach gesagt offenbart diese Arbeit eine Abhängigkeitskette im Hoden: PTBP1 hilft Sertoli-Zellen, ein zentrales Signalzentrum aufzubauen; dieses Zentrum ordnet ihr inneres Gerüst; und ein intaktes Gerüst ermöglicht es ihnen, sich an die sich entwickelnden Spermien anzulegen und sie zu schützen. Wird die Kette an PTBP1 unterbrochen, verlieren Sertoli-Zellen ihre Struktur, die Schutzbarriere versagt und die Spermienentwicklung bricht zusammen — mit dem Ergebnis männlicher Unfruchtbarkeit. Obwohl diese Forschung an Mäusen durchgeführt wurde, kommen dieselben Moleküle auch beim Menschen vor, was die Möglichkeit eröffnet, dass subtile Störungen in der RNA-Kontrolle innerhalb von Sertoli-Zellen einigen unerklärten Fällen männlicher Unfruchtbarkeit zugrunde liegen könnten und neue molekulare Ziele für künftige Untersuchungen liefert.
Zitation: Ozawa, M., Taguchi, J., Mori, H. et al. PTBP1 supports mouse spermatogenesis by facilitating cytoskeletal organization through the mTORC2–PKCα pathway in Sertoli cells. Commun Biol 9, 341 (2026). https://doi.org/10.1038/s42003-026-09636-5
Schlüsselwörter: männliche Fruchtbarkeit, Sertoli-Zellen, Spermatogenese, Zytoskelett, RNA-bindende Proteine