Clear Sky Science · de
Negative Regulation des NF-κB-Signalwegs durch die Ubiquitin-Ligase Nedd4-1(NE)
Warum das Abschalten von Entzündungen wichtig ist
Unser Immunsystem ist auf schnelle Entzündungsreaktionen angewiesen, um Infektionen zu bekämpfen und Verletzungen zu heilen, doch dieselben Prozesse können Gewebe schädigen und Krebs fördern, wenn sie zu lange aktiv bleiben. Dieser Beitrag erläutert, wie menschliche und andere Primatenzellen diese Gefahr vermeiden, indem sie eine neu charakterisierte eingebaute "Bremse" nutzen, die eines der zentralen Alarmsysteme des Körpers wieder beruhigt, sobald seine Aufgabe erfüllt ist.
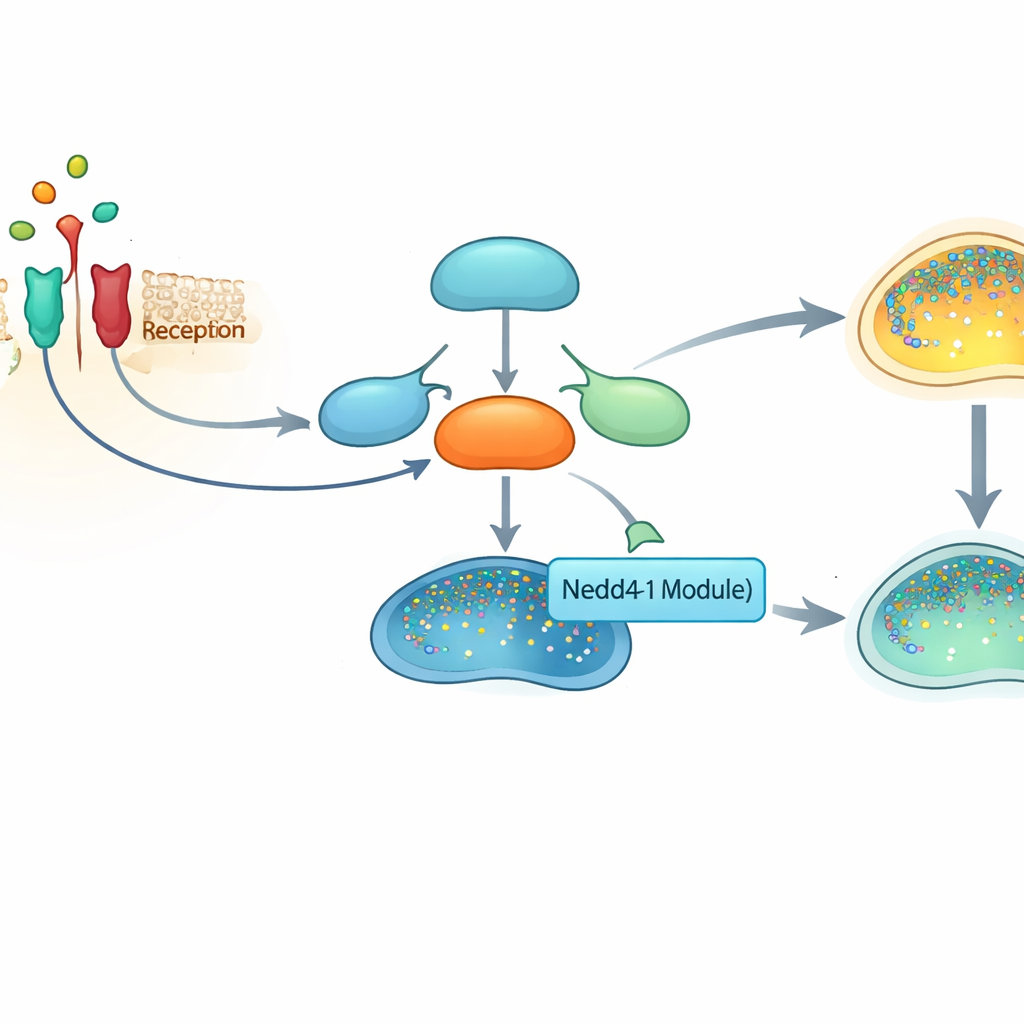
Ein zentraler Alarmschalter in unseren Zellen
Im Zentrum dieser Geschichte steht NF-κB, eine Proteinfamilie, die wie ein Hauptschalter für Hunderte von Genen wirkt, die an Entzündung, Zellüberleben und Immunität beteiligt sind. Wenn Zellen Stresssignale wie das Entzündungsmolekül TNFα wahrnehmen, setzt eine Kaskade von Ereignissen NF-κB aus seinen Protein-"Chaperonen" im Zellplasma frei und ermöglicht ihm, in den Zellkern zu wandern, wo es pro‑inflammatorische und pro‑überlebensfördernde Gene einschaltet. Da dieser Weg so mächtig ist, müssen Zellen sowohl seine Aktivierung als auch seine Abschaltung eng regulieren. Das Versagen, ihn abzuschalten, wird mit chronisch entzündlichen Erkrankungen und vielen Krebsarten in Verbindung gebracht.
Eine nur bei Primaten vorhandene Bremse des Alarms
Die Forscher konzentrierten sich auf Nedd4-1, ein Mitglied einer großen Enzymfamilie, die andere Proteine mit einem kleinen Molekül namens Ubiquitin markiert. Dieses Etikett kennzeichnet Proteine häufig zur Zerstörung oder Umlagerung innerhalb der Zelle und formt so Signalnetzwerke um. Eine zuvor entdeckte Spleißvariante von Nedd4-1, bezeichnet als Nedd4-1(NE), kommt nur bei Primaten vor und trägt ein langes zusätzliches Segment an seinem N‑Termin, das seinen zellulären Aufenthaltsort und seine Erkennungsmerkmale verändert. Im Gegensatz zur Standardform von Nedd4-1, die über andere Partner die NF‑κB-Aktivität sogar verstärken kann, stellten die Autoren fest, dass Nedd4-1(NE) den gegenteiligen Effekt hat: Es dämpft die NF‑κB-Signalübertragung, insbesondere nach länger andauernder TNFα-Exposition.
Zwei Mechanismen, NF-κB in Schach zu halten
Um herauszufinden, wie diese Bremse funktioniert, verwendeten die Autoren Proximity-Labeling- und Protein-Pull‑Down-Methoden, um zu sehen, welche Moleküle physisch mit Nedd4-1(NE) interagieren. Sie identifizierten zentrale Komponenten des NF‑κB-Wegs, darunter die Kinase IKKβ und das NF‑κB-Vorläuferprotein NF‑κB1 (auch p105 genannt). Folgeexperimente zeigten, dass Nedd4-1(NE) Ubiquitin an IKKβ anfügt, was zu dessen Abbau führt. Mit weniger IKKβ wird sein übliches Ziel IκBα nicht mehr so effizient phosphoryliert und abgebaut. Infolgedessen bleibt IκBα stabiler und hält die aktive NF‑κB-Untereinheit p50 im Zytosol gebunden, wodurch deren Eintritt in den Zellkern und das Anschalten entzündlicher Gene verhindert wird.
Eine adaptorgeleitete Übergabe an die Bremse
Nedd4-1(NE) wirkt auch weiter stromabwärts, indem es die Mengen von NF‑κB1 selbst einschränkt. Hier arbeitet das Enzym nicht allein: Es kooperiert mit einem weiteren ubiquitylierenden Protein namens KPC1. KPC1 hilft bei der Verarbeitung des NF‑κB1-Vorläufers p105 zum aktiven p50 und befindet sich in zellulären Kompartimenten, die als späte Endosomen bekannt sind, wo auch Nedd4-1(NE) lokalisiert ist. Die Forscher zeigten, dass Nedd4-1(NE) KPC1 ubiquitinieren kann und dass dieses modifizierte KPC1 als Adapter dient, der NF‑κB1 zu Nedd4-1(NE) an den späten Endosomen rekrutiert. Dieser Dreierkomplex fördert die Destabilisierung von sowohl p105 als auch p50 und verringert erneut den Pool an NF‑κB, der den Zellkern erreichen kann.
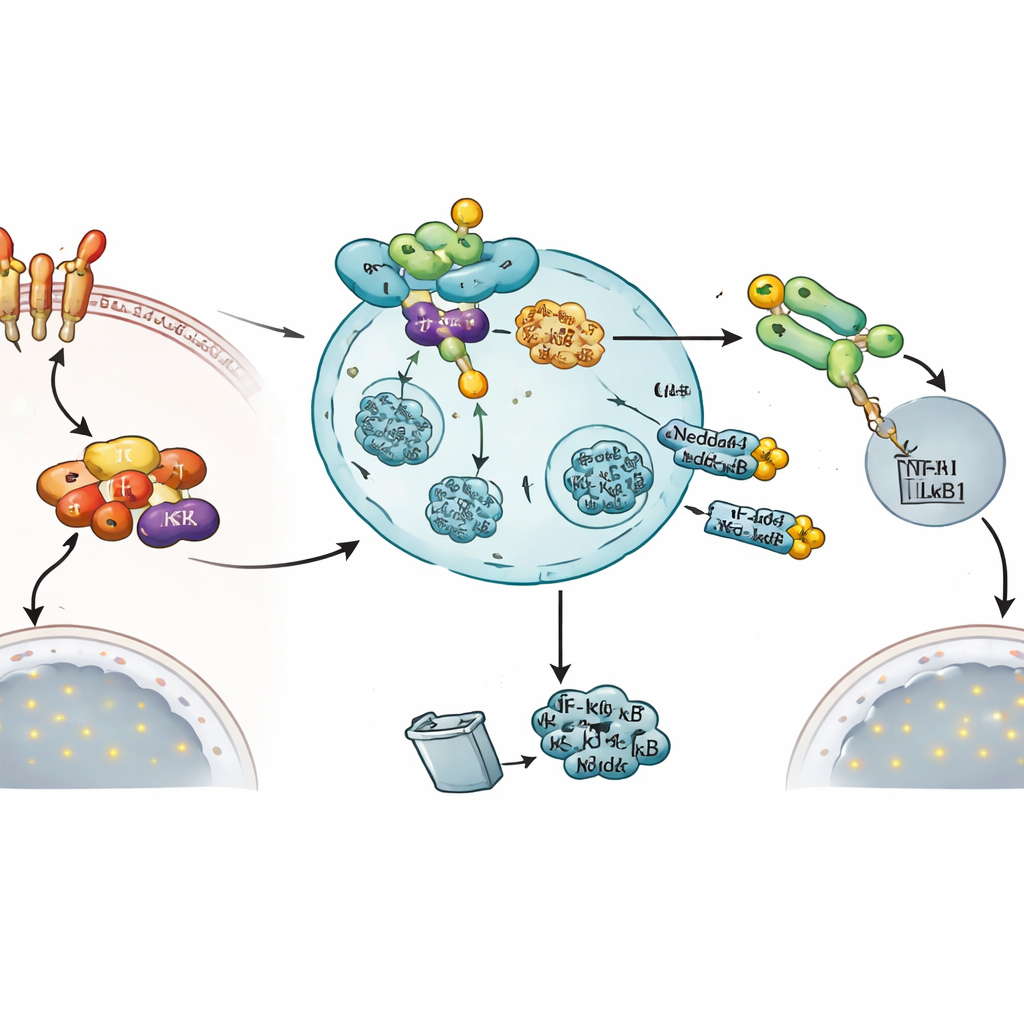
Eine eingebaute Rückkopplungsschleife zur Beendigung des Signals
Bemerkenswerterweise scheint gerade das Signal, das NF‑κB aktiviert, auch diese Bremse zu induzieren. Bei TNFα‑Behandlung der Zellen stiegen die Niveaus der Nedd4-1(NE)-Messenger‑RNA dramatisch an, während die Standardform von Nedd4-1 unverändert blieb. Funktionelle Messungen stützten die Idee, dass Nedd4-1(NE) ein Abschaltventil ist: Eine Erhöhung aktiven Nedd4-1(NE) reduzierte die Bewegung von NF‑κB1 in den Zellkern, senkte die Aktivität eines NF‑κB‑abhängigen Reportergens und verringerte die Expression eines NF‑κB‑regulierten Entzündungsgens, TNFAIP3. Zusammen zeichnen diese Befunde eine negative Rückkopplungsschleife nach, in der die Aktivierung des NF‑κB‑Wegs letztlich Nedd4-1(NE) erhöht, welches dann zwei kritische Knoten — IKKβ und NF‑κB1 — ins Visier nimmt, um die Entzündungsreaktion wieder herunterzufahren.
Was das für Gesundheit und Krankheit bedeutet
Für ein allgemeines Publikum lautet die Kernbotschaft, dass unsere Zellen einen zusätzlichen, primatenspezifischen Sicherheitsmechanismus eingebaut haben, um zu verhindern, dass entzündliche Signalgebung außer Kontrolle gerät. Durch selektives Markieren und Beschneiden zentraler Komponenten des NF‑κB‑Systems hilft Nedd4-1(NE), die Reaktion auf TNFα zu beenden und kann zu einem langfristigen immunologischen Gleichgewicht beitragen. Das Verständnis dieser eingebauten Bremse könnte neue Wege für die Behandlung von Erkrankungen eröffnen, bei denen NF‑κB chronisch überaktiv ist, etwa Autoimmunerkrankungen und bestimmte Krebsarten, indem es Strategien nahelegt, diesen natürlichen Abschaltmechanismus nachzuahmen oder zu verstärken.
Zitation: Persaud, A., Kefalas, G., Shteiman, A. et al. Negative regulation of the NF-κB pathway by the ubiquitin ligase Nedd4-1(NE). Commun Biol 9, 374 (2026). https://doi.org/10.1038/s42003-026-09634-7
Schlüsselwörter: NF-kB-Signalübertragung, Entzündung, Ubiquitin-Ligase, Nedd4-1(NE), TNF alpha