Clear Sky Science · de
Notch3 reguliert die phänotypische Plastizität von Perizyten bei kolorektalem Krebs
Warum die Blutgefäße um Tumoren wichtig sind
Kolorektales Karzinom gehört zu den weltweit häufigsten und tödlichsten Krebserkrankungen, doch viele Therapien zielen direkt auf Tumorzellen und übersehen häufig das umgebende Unterstützungssystem, das das Tumorwachstum fördert. Diese Arbeit konzentriert sich auf eine weniger bekannte Gruppe von Unterstützerzellen, die Perizyten genannt werden und sich um kleine Blutgefäße legen. Indem die Autorinnen und Autoren aufdecken, wie ein Signalschalter namens Notch3 das Verhalten von Perizyten verändert, zeigen sie, wie die Blutversorgung des Tumors entweder in Richtung undichter, chaotischer Gefäße gedrängt werden kann, die dem Krebs zugutekommen, oder in Richtung normalerer Gefäße, die die Krankheit verlangsamen und die Behandlung verbessern könnten. 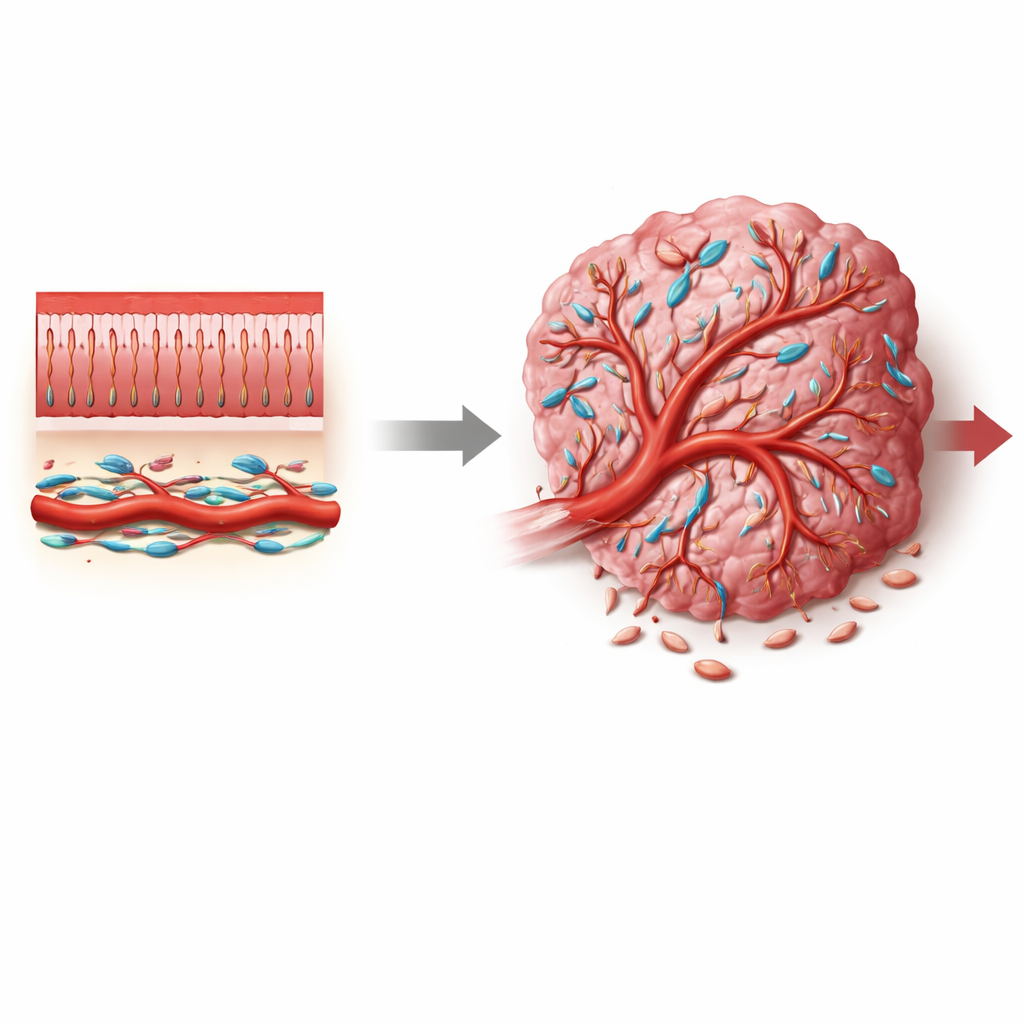
Die versteckten Helfer um tumorale Gefäße
Blutgefäße sind mehr als nur hohle Röhren. In gesundem Gewebe werden kleine Gefäße eng von Perizyten umschlossen — spezialisierten Zellen, die die Gefäßwände stabilisieren, den Blutfluss steuern und Leckagen begrenzen. In Tumoren jedoch sehen und verhalten sich diese Perizyten häufig anders: Sie können sich ablösen, sich vermehren oder ihre Identität verändern und so zur atypischen, undichten Gefäßstruktur beitragen, die für Krebs typisch ist. Bei kolorektalen Tumoren, in denen das Mikromilieu von Fibroblasten, Immunzellen und Gefäßzellen dicht bevölkert ist, war bislang unklar, woher tumorassoziierte Perizyten stammen, welche Zustände sie annehmen und welche molekularen Signale sie in tumorfördernde Rollen treiben.
Perizytenverfolgung während der Tumorentstehung
Um Perizyten über die Zeit zu verfolgen, nutzten die Forschenden Mausmodelle des kolitis-assoziierten kolorektalen Karzinoms, in denen sie bestimmte Zelltypen genetisch „markieren“ und ihr Schicksal beobachten konnten. Sie zeigten, dass die in Tumoren gefundenen Perizyten größtenteils von normalen, gewebsansässigen Perizyten stammen, die sich mit der Tumorentwicklung ausdehnen und proliferieren, anstatt aus entfernten Quellen wie dem Knochenmark heranzuwandern. Mithilfe fortschrittlicher Einzelzell-RNA-Sequenzierung katalogisierten sie zehntausende stromale Zellen aus Maus-Tumoren und normalem Kolon und stellten fest, dass Perizyten im Tumormikromilieu deutlich angereichert sind. Ähnliche Perizytenexpansionen identifizierten sie auch in mehreren humanen Datensätzen zu kolorektalem Krebs, was unterstreicht, dass es sich nicht nur um ein maus-spezifisches Phänomen handelt.
Ein molekularer Schalter, der das Perizytenverhalten verändert
Das Team fragte anschließend, welche Signale das Verhalten von Perizyten in Tumoren formen, und fand, dass Notch3 — ein Rezeptor, der Zellen die Kommunikation mit Nachbarzellen ermöglicht — in tumoralen Perizyten besonders aktiv ist. Computergestützte Analysen der Zell‑zu‑Zell-Kommunikation deuteten darauf hin, dass Perizyten Notch-ähnliche Signale sowohl senden als auch empfangen, insbesondere über Partner auf Gefäßzellen. Durch künstliche Aktivierung von Notch3 in Perizyten beobachteten die Forschenden, dass diese Zellen stärker proliferierten, aber weniger kontraktile Proteine exprimierten, die typischerweise mit gefäßstabilisierendem Verhalten verbunden sind. Die Tumorblutgefäße dieser Mäuse wurden größer, undichter und zeigten mehr proliferierende Endothelzellen — ein Hinweis auf weniger stabile Gefäßstrukturen. Umgekehrt reduzierte die Deletion von Notch3 die Proliferation von Endothelzellen, verringerte die Gefäßgröße und senkte die Leckage, was auf eine Verschiebung hin zu normalisierteren Gefäßen hindeutet, ohne jedoch die frühe Tumoranzahl oder -größe drastisch zu verändern. 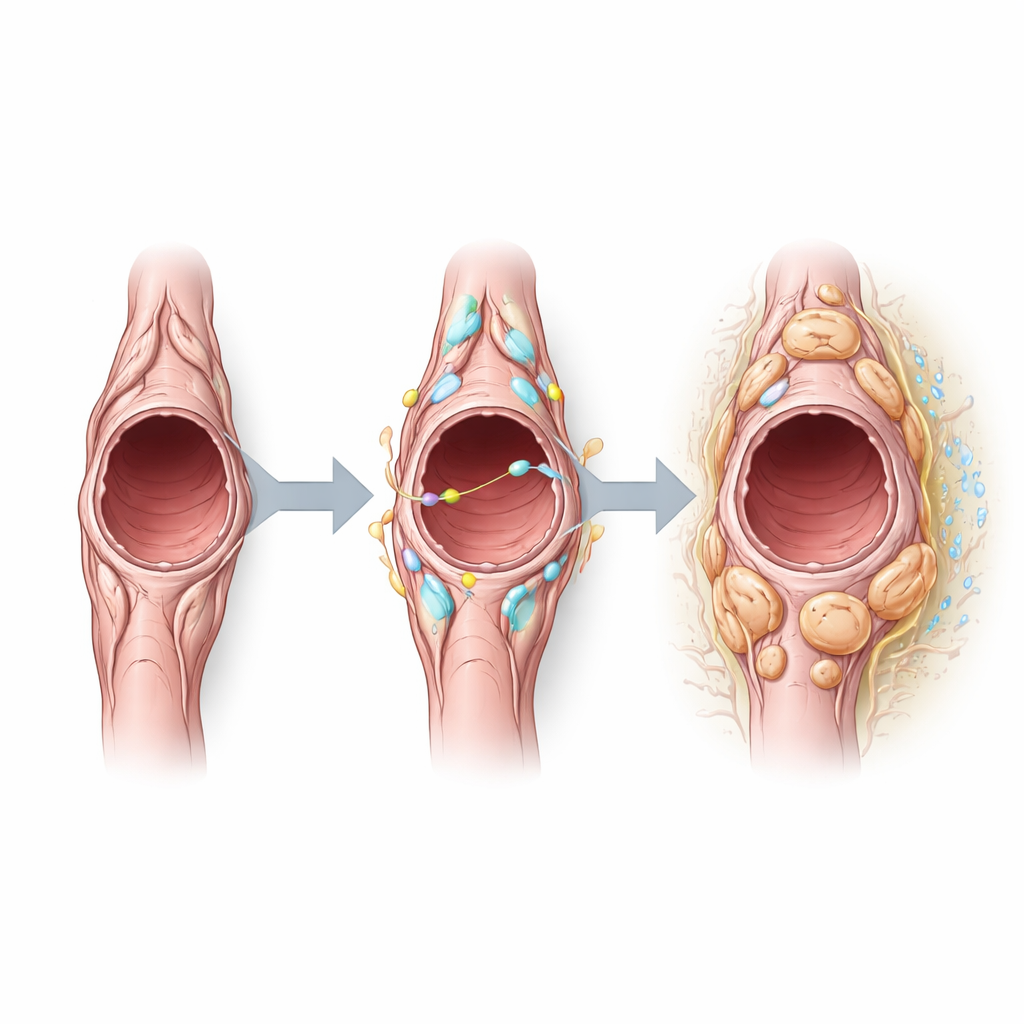
Viele Gesichter der Perizyten im Tumor
Über einfache Ein‑/Aus‑Veränderungen hinaus zeigte die Studie, dass tumorale Perizyten in mehreren unterschiedlichen Zuständen existieren. Einige Untergruppen wiesen Merkmale hochkontraktiler Zellen auf, andere produzierten große Mengen extrazellulärer Matrix, einige zeigten entzündliche Eigenschaften, und eine Untergruppe trug sogar Signaturen, die üblicherweise in Endothelzellen zu finden sind. Die Notch3-Aktivität war nicht gleichmäßig verteilt: Sie war in einer „synthetischen“ beziehungsweise matrixproduzierenden Perizytenpopulation angereichert und in der kontraktileren Untergruppe gering. Trajektorienanalysen deuteten darauf hin, dass Perizyten von einem kontraktilen Zustand in einen synthetischen, proliferativen Zustand übergehen können, wenn die Notch3-Aktivität ansteigt. Bei der Untersuchung humaner Daten zu kolorektalem Krebs fanden die Autorinnen und Autoren ein vergleichbares Spektrum an Perizytenzuständen und erneut erhöhte Aktivität eines Notch3-Zielgens in tumorassoziierten und proliferierenden Perizyten, was die Ergebnisse aus Mausmodellen widerspiegelt.
Aus Chaos der Gefäße eine therapeutische Chance machen
Insgesamt zeichnet die Arbeit Notch3 als ein zentrales Stellrad, das die Identität von Perizyten einstellt und damit Struktur und Funktion tumoraler Blutgefäße beeinflusst. Hohe Notch3-Aktivität treibt Perizyten in einen proliferativen, weniger kontraktilen Zustand, der mit vergrößerten, undichten Gefäßen verbunden ist und das Tumorwachstum fördert. Niedrige Notch3-Aktivität ist mit kontraktileren Perizyten, ruhigeren Endothelzellen und normalisierterer Gefäßarchitektur assoziiert, was das Tumorwachstum bremsen und die Wirkstoffverteilung verbessern könnte. Durch die gezielte Ansteuerung von Notch3 in Perizyten könnten zukünftige Therapien tumorale Gefäße aus dem Chaos in Richtung Stabilität lenken und so eine neue Behandlungsstrategie für fortgeschrittenen kolorektalen Krebs ergänzend zu bestehenden Medikamenten bieten.
Zitation: Chalkidi, N., Stavropoulou, A., Arvaniti, VZ. et al. Notch3 regulates pericyte phenotypic plasticity in colorectal cancer. Commun Biol 9, 343 (2026). https://doi.org/10.1038/s42003-026-09629-4
Schlüsselwörter: kolorektales Karzinom, tumorales Mikromilieu, Perizyten, Notch3-Signalgebung, tumorale Blutgefäße