Clear Sky Science · de
Endotheliales TRIM47 reguliert die Integrität der Blut-Hirn-Schranke und die Kognition über den KEAP1/NRF2-Signalweg bei Mäusen
Warum der Schutz winziger Hirngefäße wichtig ist
Zerebrale kleine Gefäßerkrankung ist ein stiller Störenfried im Gehirn. Sie schädigt die kleinsten Blutgefäße, erhöht das Schlaganfallrisiko und nistet sich langsam in Gedächtnis und Denken ein, doch es fehlen nach wie vor Therapien, die die zugrundeliegenden biologischen Ursachen gezielt angehen. Diese Studie untersucht ein bestimmtes Protein, TRIM47, das in den Zellen der Hirngefäße vorkommt, und stellt eine einfache, aber zentrale Frage: Trägt es dazu bei, die schützende Blut–Hirn-Schranke intakt zu halten, und hat das Auswirkungen auf die Kognition?
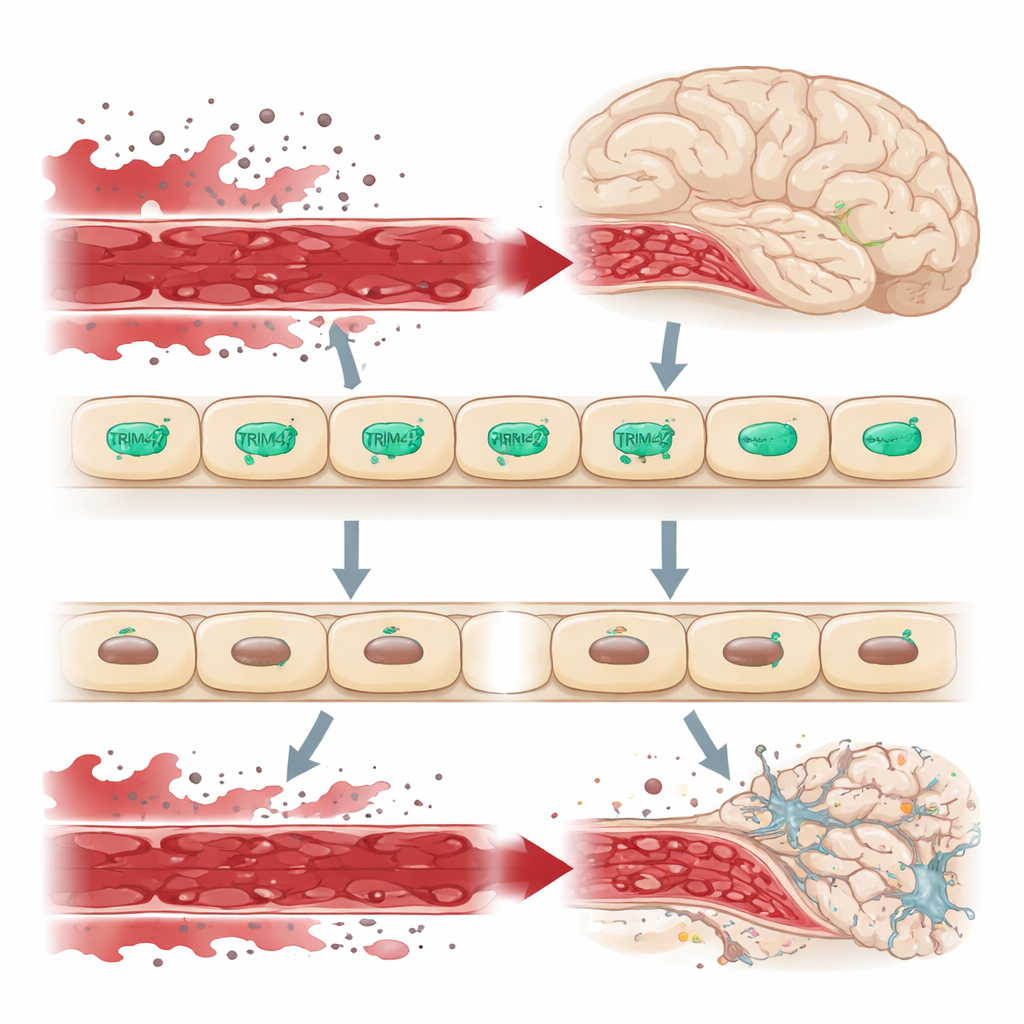
Ein Wächter an der Grenze des Gehirns
Das Gehirn ist von der restlichen Körperzirkulation durch die Blut–Hirn-Schranke abgeschirmt, eine dicht verschlossene Schicht aus Endothelzellen, die genau kontrolliert, was ins Gehirngewebe gelangen darf. Wenn diese Barriere undicht wird, sickern schädliche Moleküle aus dem Blut ins Gehirn, belasten Neurone und Stützzellen und tragen zu Erkrankungen wie Demenz bei. Genetische Untersuchungen in großen menschlichen Kohorten hatten einen DNA-Abschnitt mit dem TRIM47-Gen als Risikoregion für zerebrale kleine Gefäßerkrankung identifiziert. TRIM47 ist in Hirnendothelzellen besonders aktiv, was darauf hindeutet, dass es ein wichtiger Hüter dieser Barriere sein könnte.
Wie TRIM47 Zellen gegen oxidativen Stress rüstet
Die Autoren untersuchten zunächst menschliche Hirnendothelzellen im Labor und verringerten TRIM47 mittels RNA-Interferenz. Das löste breite Veränderungen in der Genaktivität aus, wobei das am stärksten betroffene Netzwerk um NRF2 zentriert war – einen Hauptregulator der zellulären Antioxidantienabwehr. Unter normalen Bedingungen wird NRF2 von einem anderen Protein, KEAP1, in Schach gehalten, das seine Zerstörung einleitet. Das Team zeigte, dass TRIM47 an KEAP1 bindet und dazu beiträgt, NRF2 vor dem Abbau zu bewahren. Mit vorhandenem TRIM47 kann NRF2 sich ansammeln, in den Zellkern wandern und Gene aktivieren, die reaktive Sauerstoffspezies entgiften. Geht TRIM47 verloren, sinken die NRF2-Spiegel, Antioxidantiengene sind weniger aktiv und Endothelzellen werden anfälliger für oxidativen Stress.
Von undichten Gefäßen zu Gedächtnisproblemen bei Mäusen
Um zu sehen, wie sich dieser Mechanismus im lebenden Gehirn auswirkt, erzeugten die Forschenden Mäuse, bei denen das Trim47-Gen im gesamten Körper fehlte, sowie eine Linie, in der Trim47 nur in Endothelzellen entfernt werden konnte. Erwachsene Tiere beider Modelle entwickelten deutliche Probleme beim räumlichen Lernen und Gedächtnis und fielen in Tests wie dem Y‑Maze und dem Morris-Wasserlabyrinth durch, obwohl ihre motorische Aktivität normal war. Untersuchungen der Gehirne zeigten, dass die Blut–Hirn-Schranke undicht geworden war: kleine fluoreszente Marker und Blutproteine entkamen aus den Gefäßen ins umliegende Gewebe. Wichtige „Dichtungs“-Proteine, die enge und Adhärenzverbindungen zwischen Endothelzellen bilden, insbesondere Claudin‑5 und Occludin, waren vermindert. Nahegelegene Astrozyten, die sternförmigen Stützzellen, die schnell auf Verletzungen reagieren, wurden aktiviert, obwohl es zu diesem Zeitpunkt kaum Anzeichen für eine ausgeprägte Entzündung oder Neuronverlust gab.
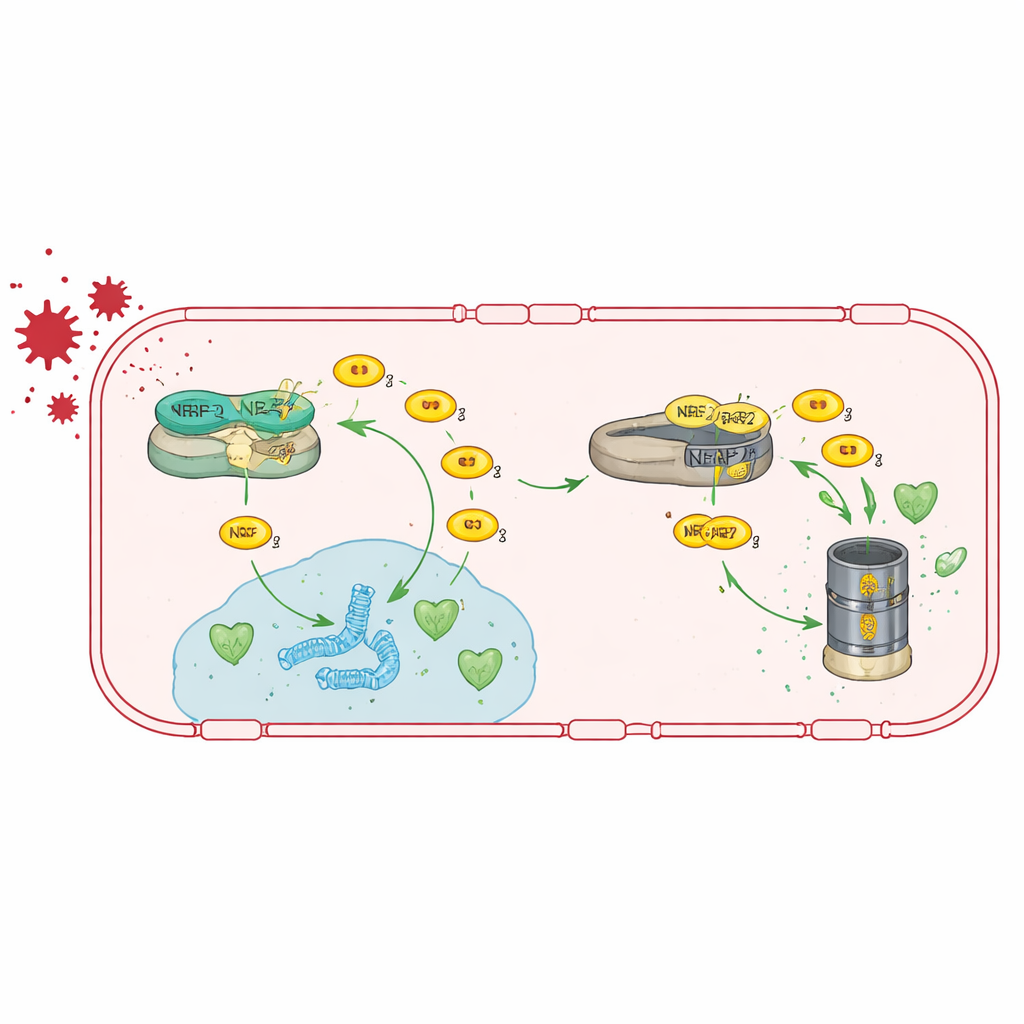
Den Antioxidationsweg wieder einschalten
Da TRIM47 vor allem durch die Stärkung der NRF2-Aktivität wirkt, prüfte das Team, ob sich der Verlust umgehen lässt, indem man NRF2 direkt stimuliert. Sie fütterten Trim47-defiziente Mäuse mit einer Diät, die tert-Butylhydrochinon (tBHQ) enthielt, eine Verbindung, die dafür bekannt ist, NRF2 zu stabilisieren und dessen Zielgene zu aktivieren. Diese Behandlung stellte die Aktivität von Antioxidantiengenen in Hirnendothelzellen wieder her, brachte die Expression von Tight-Junction-Genen nahe an den Normalwert zurück und reduzierte die Undichtigkeit der Blut–Hirn-Schranke. Auffallend war, dass sie auch die Astrozytenaktivierung normalisierte und die Gedächtnisleistung der Tiere rettete, was darauf hindeutet, dass die Verstärkung dieses Antioxidationswegs vaskuläre und kognitive Probleme zumindest bei Mäusen umkehren kann.
Hinweise aus menschlichem Blut und nächste Schritte
Um die Mäusebefunde auf den Menschen zu übertragen, analysierten die Forschenden Proteine im Zusammenhang mit dem NRF2-Weg in Blutproben von Tausenden Menschen, die eine Hirn‑MRT hatten. Die Spiegel mehrerer NRF2-regulierter Proteine standen in Zusammenhang mit Bildgebungsmarkern kleiner Gefäßerkrankung, wie vergrößerten perivaskulären Räumen und Veränderungen der weißen Substanz. Das stützt die Idee, dass veränderte TRIM47–NRF2-Signalgebung beim Menschen relevant ist und dass diese Proteine als Biomarker für Schweregrad oder Progression der Erkrankung dienen könnten.
Was das für die Hirngesundheit bedeutet
Insgesamt zeichnet die Arbeit TRIM47 als molekularen Bodyguard, der Hirngefäße vor oxidativen Schäden schützt, indem er das NRF2-Antioxidationssystem stabilisiert. Fehlt TRIM47 oder ist es beeinträchtigt, schwächt sich die Blut–Hirn-Schranke, es sammelt sich subtile Hirnschädigung an und das Gedächtnis beginnt zu versagen. Die Reaktivierung des NRF2-Wegs kann bei Mäusen sowohl die Barriere reparieren als auch die Kognition wiederherstellen und macht diese Signalkette zu einem vielversprechenden therapeutischen Ziel für vaskuläre Formen der Demenz. Während tBHQ selbst nicht als Medikament für Menschen geeignet ist, könnten sicherere NRF2-aktivierende Verbindungen oder Strategien, die die schützende Rolle von TRIM47 nachahmen, eines Tages helfen, die Gesundheit des Gehirns zu erhalten, indem sie seine kleinsten, empfindlichsten Gefäße stärken.
Zitation: Delobel, V., Grenier, C., Boulestreau, R. et al. Endothelial TRIM47 regulates blood-brain barrier integrity and cognition via the KEAP1/NRF2 signalling pathway in mice. Commun Biol 9, 399 (2026). https://doi.org/10.1038/s42003-026-09628-5
Schlüsselwörter: Zerebrale kleine Gefäßerkrankung, Blut–Hirn-Schranke, TRIM47, NRF2-Signalweg, Vaskuläre Demenz