Clear Sky Science · de
Ein inter‑Untereinheiten‑Pfad ist erforderlich für entropisch getriebene und negativ kooperative Bindung von cyclischen Nukleotiden im HCN2‑Kanal
Wie der winzige Schrittmacher des Herzens chemische Signale wahrnimmt
Jeder Herzschlag und viele Hirnrhythmen hängen von mikroskopischen Kanälen ab, die in den Membranen unserer Zellen auf- und zumachen. Diese Kanäle, sogenannte HCN‑Schrittmacherkanäle, werden nicht nur durch elektrische Spannung, sondern auch durch kleine Botenstoffe gesteuert, die als cyclische Nukleotide bekannt sind. Die Studie stellt eine auf den ersten Blick einfache, aber weitreichende Frage: Wie binden diese winzigen Moleküle koordiniert an den HCN2‑Kanal, und wie können feine Störungen in diesem Prozess zu Erkrankungen wie Epilepsie beitragen?
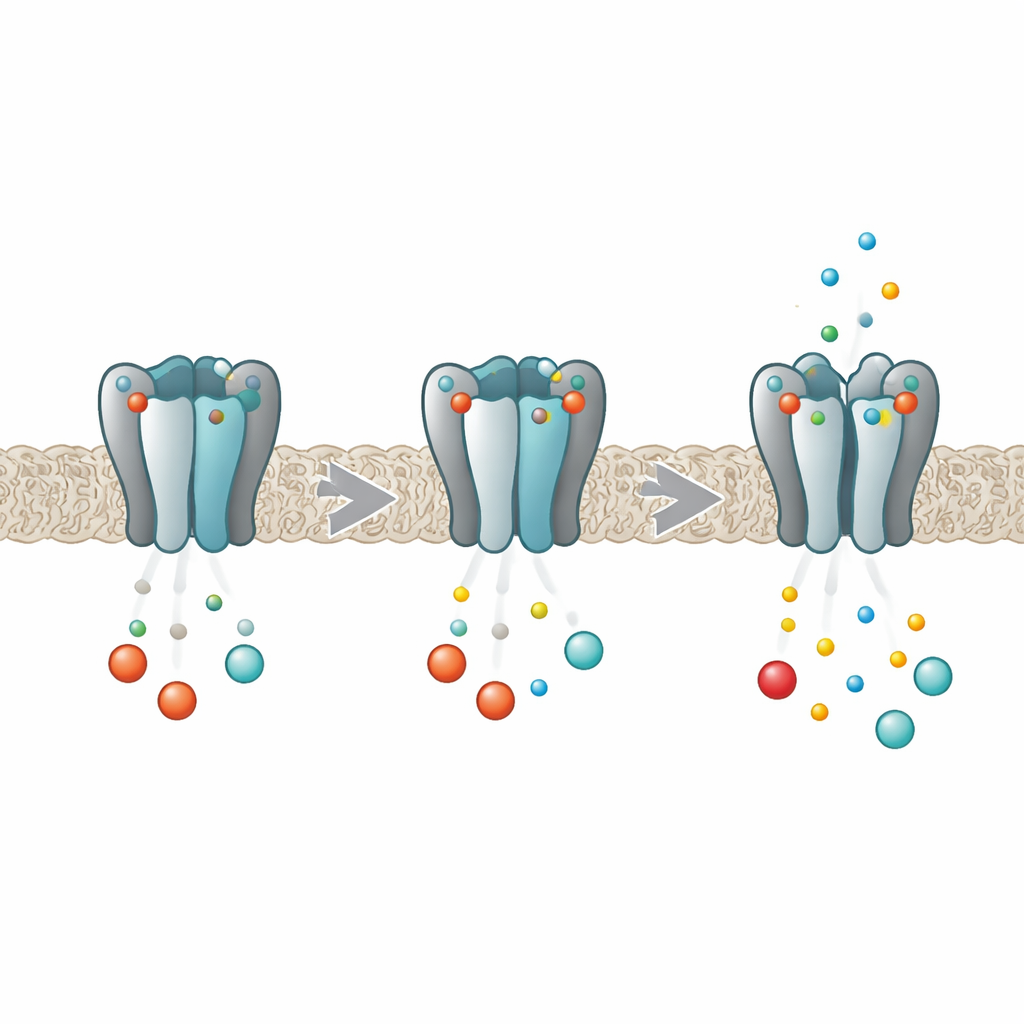
Ein molekularer Dimmer für die Rhythmen des Körpers
HCN‑Kanäle funktionieren wie Dimmer für die elektrische Aktivität in Herz‑ und Nervenzellen. Jeder Kanal besteht aus vier identischen Proteinuntereinheiten, die zusammen einen Zentralpore bilden, durch den Ionen fließen. Tief in jeder Untereinheit befindet sich eine Tasche, die cyclische Nukleotide wie cAMP und cGMP binden kann. Wenn diese Botenstoffe binden, erleichtert das Öffnen des Porenkanals und verstärkt den Schrittmacherstrom. Frühere Arbeiten zeigten, dass beim HCN2‑Isoform die Bindung nicht unabhängig an jedem Bindungsplatz erfolgt; vielmehr beeinflussen sich die vier Stellen gegenseitig, sodass das erste Molekül leichter bindet als die folgenden — ein Verhalten, das als negative Kooperativität bekannt ist. Die neue Arbeit hatte zum Ziel, genau aufzudecken, wie die vier Untereinheiten während dieses Prozesses miteinander „sprechen“.
Untereinheiten, die ihre Nachbarn spüren
Die Forschenden kombinierten Computersimulationen mit Labormessungen an isolierten Fragmenten des HCN2‑Kanals. In langen molekularen Dynamiksimulationen verfolgten sie, wie sich der Schwanzbereich des Kanals — der Teil, der die cyclischen Nukleotidtaschen und den sogenannten C‑Linker enthält, der mit dem Porenbereich verbunden ist — biegt und schwankt, wenn unterschiedlich viele cAMP‑ oder cGMP‑Moleküle gebunden sind. Sie fanden heraus, dass die Bindung eines Botenstoffs an eine Untereinheit diese nicht einfach nur stabilisierte. Stattdessen veränderte sie subtil die Stabilität der Nachbaruntereinheiten, machte sie mal steifer, mal flexibler, obwohl die Gesamtstruktur des Proteins kaum verschob. Diese Nachbar‑zu‑Nachbar‑Einflüsse hingen davon ab, wie viele Stellen besetzt waren und wo sie im Ring lagen, und entsprachen damit dem, was man bei negativer Kooperativität erwarten würde.
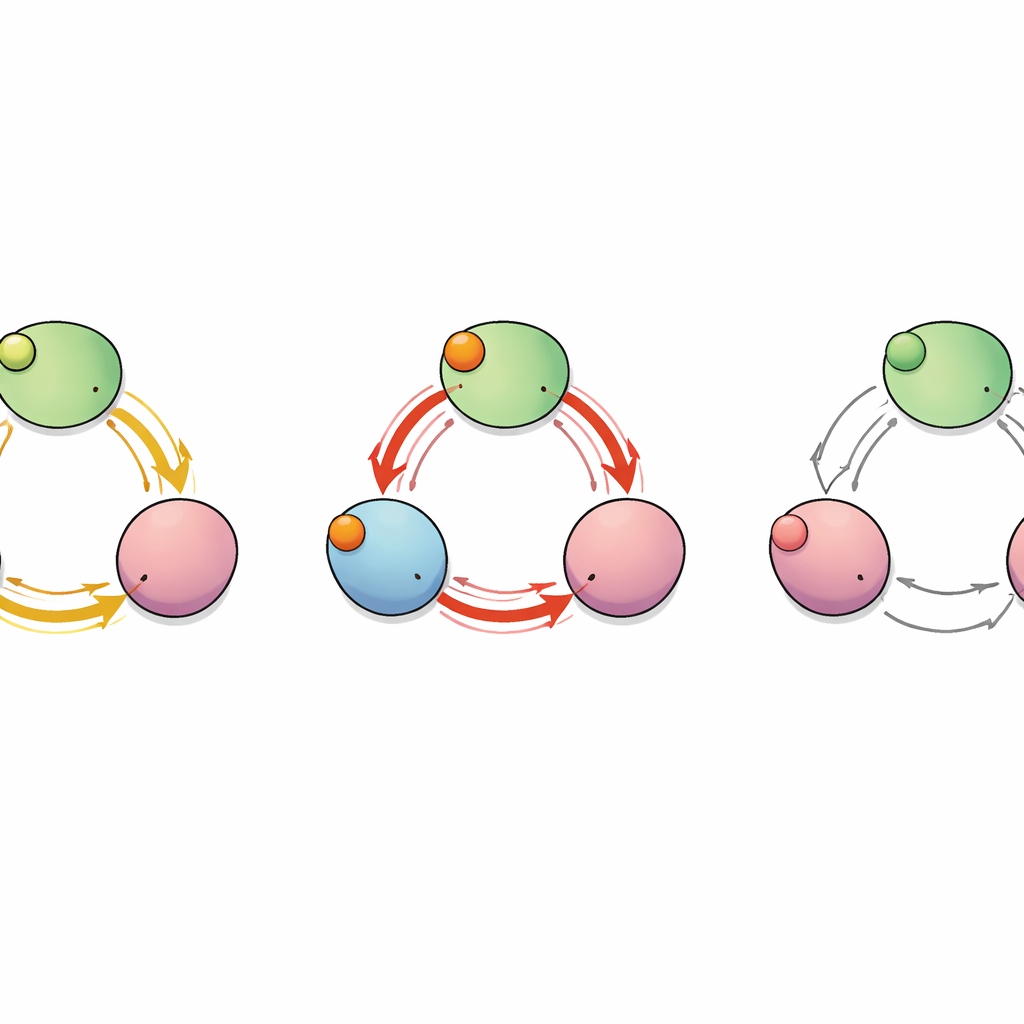
Ein verborgener Pfad zwischen Untereinheiten
Um abzubilden, wie das „Signal“ der Bindung durch das Protein läuft, betrachtete das Team den Kanal als Netzwerk wechselwirkender Aminosäuren. Sie berechneten, welche Residuen sich in den Simulationen korreliert bewegten, und nutzten graphentheoretische Werkzeuge, um die kürzesten und effizientesten Kommunikationswege von den Bindungstaschen zu den C‑Linker‑Segmenten zu identifizieren, die den Porenbereich steuern. Diese Analyse zeigte mehrere mögliche Routen, von denen zwei herausstachen: eine, die innerhalb einer einzelnen Untereinheit verbleibt, und eine andere, die von einer Untereinheit zur benachbarten springt. Entlang dieses inter‑untereinheiten Pfads fungierte eine einzelne Aminosäure — das Glutamat an Position 488 (E488) — als kritischer Knoten, durch den viele der kürzesten Wege liefen, was darauf hindeutet, dass sie ein wichtiger Relaispunkt für kooperative Bindung sein könnte.
Mutationen, die das Gespräch unterbrechen
Die Autoren führten anschließend Experimente an gereinigten Kanal‑Schwanzfragmenten durch, um die Bedeutung dieses Pfads zu prüfen. Sie veränderten E488 und das benachbarte Tyrosin 459 (Y459), das an der Nachbaruntereinheit liegt, wo der Pfad ankommt. Mittels dynamischer Lichtstreuung bestätigten sie, dass die mutierten Proteine weiterhin zu Viererkomplexen assembleierten, aber sie zeigten nicht mehr die starke ligand‑induzierte Verfestigung zwischen den Untereinheiten, die beim normalen Protein zu beobachten war. Isotherme Titrationskalorimetrie, die die winzigen Bindungswärmen misst, zeigte eine noch größere Veränderung: Wildtyp‑HCN2 wies zwei unterschiedliche Bindungsereignisse auf, einen hochaffinen Schritt, der hauptsächlich durch einen Anstieg der Entropie (größere interne Beweglichkeit) getrieben wurde, gefolgt von drei nieder‑affinen Schritten. Im Gegensatz dazu zeigten Mutanten an E488 oder Y459 nur einen einzigen, mäßig‑affinen Bindungsmodus, dem dieser günstige entropische Beitrag fehlte und bei dem die charakteristische negative Kooperativität verlorenging.
Warum subtile Entropie‑Änderungen wichtig sind
In der Zusammenschau zeichnet die Studie das Bild eines dynamischen HCN2‑Rings aus vier Untereinheiten, die über spezifische „Gesprächspfade“ verbunden sind. Wenn das erste cyclische Nukleotid bindet, verändert es über E488 und Y459 die Bewegungen entfernter Teile des Rings und macht spätere Bindungsereignisse weniger günstig und justiert so die Reaktion des Porenkanals. Dieser Effekt beruht nicht auf großen strukturellen Umlagerungen, sondern auf Verschiebungen in der internen Flexibilität — Entropieänderungen, die in statischen Schnappschüssen unsichtbar sind, aber für die Funktion entscheidend sind. Mutationen, die die Schlüsselreste entlang dieses inter‑untereinheiten Pfads stören, unterdrücken das Gespräch, beseitigen die negative Kooperativität und stehen in Verbindung mit Erkrankungen wie der idiopathischen generalisierten Epilepsie. Für Leser ohne Fachhintergrund lautet die Quintessenz: lebenswichtige Schalter in Herz und Gehirn beruhen auf kunstvoll abgestimmten molekularen „Flüstern“ zwischen Proteinuntereinheiten, und das Verständnis dieser Flüstertöne erklärt sowohl normale Rhythmen als auch das, was schiefläuft.
Zitation: Costa, F., Ng, L.C.T., Chow, S.S. et al. An inter-subunit path is required for entropically-driven and negatively cooperative binding of cyclic nucleotides in the HCN2 channel. Commun Biol 9, 362 (2026). https://doi.org/10.1038/s42003-026-09626-7
Schlüsselwörter: HCN2‑Ionenkanal, Bindung cyclischer Nukleotide, negative Kooperativität, allosterische Kommunikation, Epilepsie‑Mutation