Clear Sky Science · de
Ein kleines Molekül aktiviert allosterisch SecA‑abhängige Sekretion
Die Bakterien‑Verladestation in den Overdrive versetzen
Bakterien überleben, indem sie kontinuierlich Proteine durch winzige Tore in ihren Membranen exportieren. Diese Exporte helfen ihnen beim Aufbau der Zellwand, bei der Sekretion von Toxinen und bei der Anpassung an Stress – Prozesse, die vielen Infektionen zugrunde liegen. Diese Studie beschreibt ein kleines Chemikal namens HSI#6, das etwas Ungewöhnliches tut: statt die Exportmaschinerie zu blockieren, bringt es sie in einen hyperaktiven, weniger selektiven Modus. Zu verstehen, wie dieser Schalter funktioniert, könnte sowohl neue antibakterielle Strategien aufzeigen als auch der Biotechnologie eine Möglichkeit bieten, die Proteinsekretion auf Abruf zu steigern.
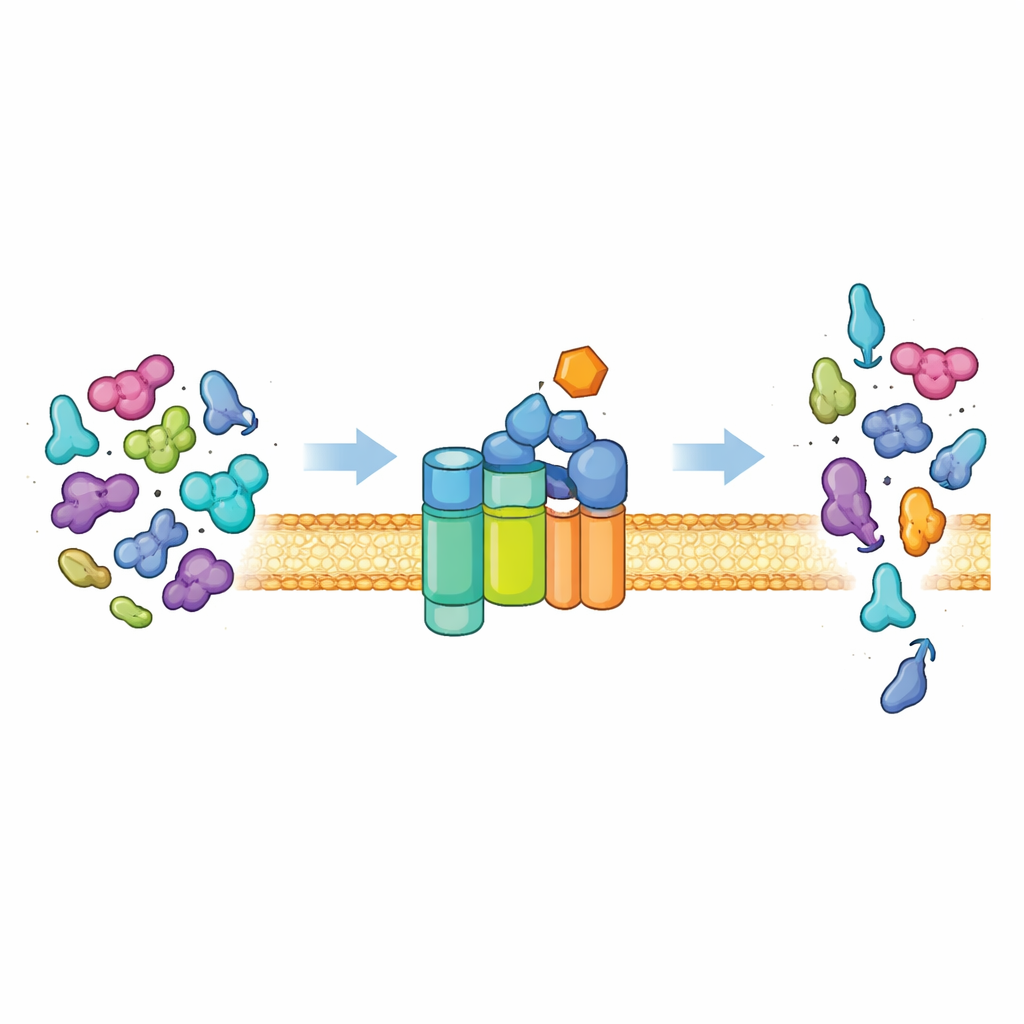
Das Protein‑Ausgangstor der Zelle
Die meisten Bakterien exportieren Proteine über einen universellen Weg, das Sec‑System. Im Kern steht ein Membrankanälchen (SecYEG) und ein Motorprotein (SecA), das zellulären Treibstoff (ATP) verbraucht, um ungefaltete Proteinketten durch den Kanal zu drücken. Unter normalen Bedingungen ist dieses System wählerisch. Es exportiert vorwiegend „Preproteine“, die spezielle Adressetiketten tragen, sogenannte Signalpeptide, plus zusätzliche Merkmale im Hauptteil des Proteins. Diese Eigenschaften sind nötig, um SecA von einem ruhigen, wenig aktiven Zustand in einen leistungsfähigen Motor umzuschalten. Nur Proteine, die die richtige Kombination an Signalen präsentieren, können die volle Aktivität freischalten — so stellt die Zelle sicher, dass sie die richtige Fracht exportiert und gewöhnliche zytoplasmatische Proteine sicher im Inneren behält.
Ein kleines Molekül, das den Motor weckt
Die Forschenden entdeckten HSI#6 in einem Screen nach Verbindungen, die die bakterielle Proteinsekretion und das Wachstum stören. Biochemische Tests zeigten, dass HSI#6 direkt an SecA mit mikromolarer Affinität bindet und dessen ATP‑Nutzung verändert. In Lösung bewirkt es, dass SecA ATP stärker hält; wenn SecA an den Kanal gebunden ist, verbessert HSI#6 sowohl die ATP‑Bindung als auch die ATP‑Umsatzrate. Dieses Muster ist typisch für einen allosterischen Aktivator: ein Molekül, das an einer Stelle des Proteins bindet, aber die Aktivität an einer anderen, räumlich entfernten Stelle verändert. Im Gegensatz zu den natürlichen Protein‑Klienten muss HSI#6 nicht als Fracht fungieren, um den Motor zu stimulieren — es justiert schlicht die internen Dynamiken von SecA so, dass die gesamte Translokase katalytisch voraktiviert wird.
Vom selektiven Filter zur promiskuitiven Nanomaschine
Sobald HSI#6 gebunden ist, besteht das Sec‑System nicht mehr auf die üblichen Export‑Markierungen. In Reagenzglasexperimenten verdoppelte die Verbindung ungefähr die Sekretion eines Standard‑Preproteins und machte den Komplex widerstandsfähiger gegen Natriumazid, einen bekannten SecA‑Inhibitor. Noch auffälliger: HSI#6 ermöglichte der normalen, „wildtypischen“ Maschinerie den Transport von Proteinen, die völlig ohne Signalpeptide sind, sowie von Proteinen, die normalerweise im Zytoplasma verbleiben. In lebenden Bakterienzellen wurde derselbe Effekt mit alkaline‑Phosphatase‑Reportern beobachtet: Wenn zytoplasmatische Proteine mit einem sekretierten Enzym fusioniert wurden, führte das Vorhandensein von HSI#6 zu einem starken Anstieg der sezernierten Aktivität, ohne die produzierte Proteinmenge zu verändern. Anders gesagt entkoppelt HSI#6 effektiv den Export von den üblichen Prüfungen der Klientenidentität und verwandelt das Sec‑System in eine breit wirkende Förderpumpe für jedes ausreichend ungefaltete Protein.
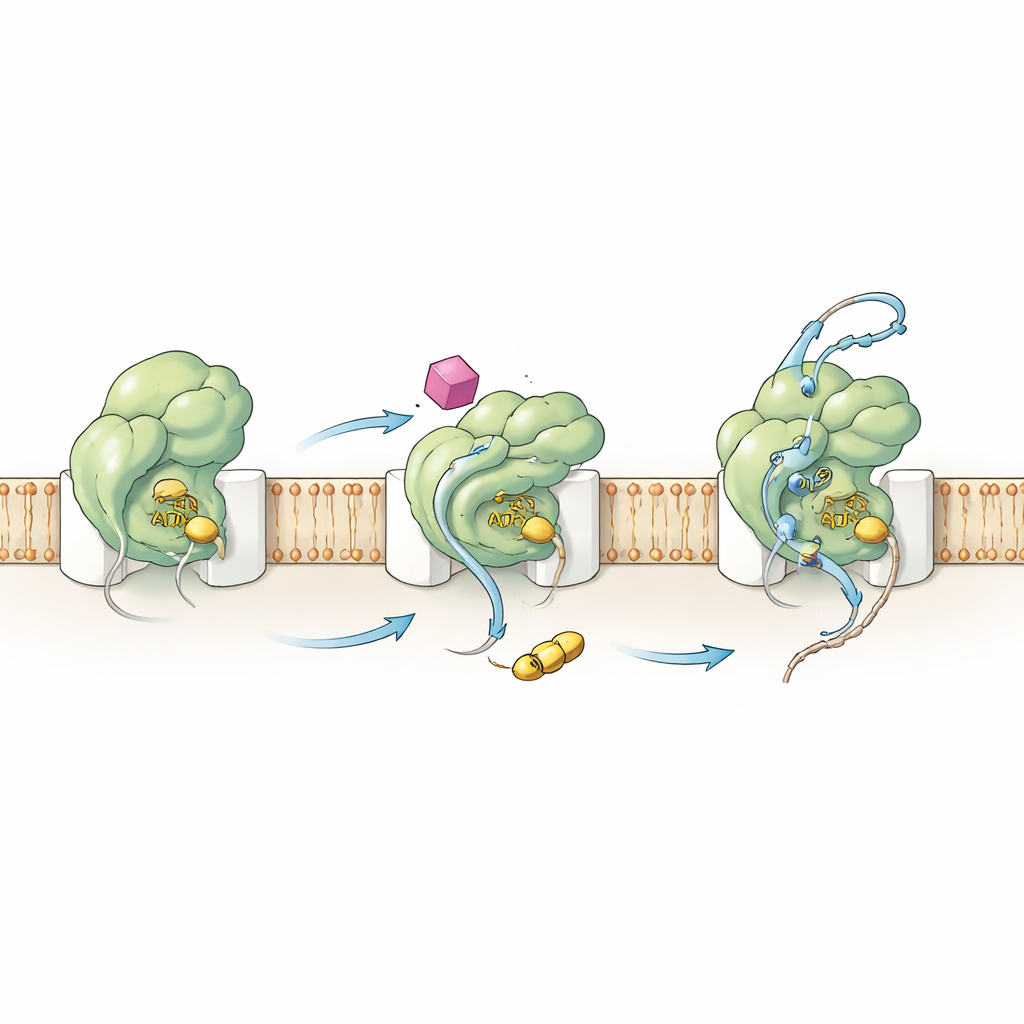
Den Motor von innen umverdrahten
Um zu verstehen, wie HSI#6 dieses Verhalten auslöst, untersuchte das Team sowohl die Chemie als auch die Bewegungen von SecA. Kinetische Messungen zeigten, dass die Verbindung den entscheidenden Aktivierungsschritt nach oben verlagert: Der SecA‑Kanal‑Komplex wird katalytisch aktiv, noch bevor ein Protein‑Klient bindet. HSI#6 hilft SecA außerdem, verbrauchte Energie (ADP) freizusetzen, einen normalerweise langsamen, geschwindigkeitsbestimmenden Schritt, und unterstützt so schnellere ATP‑Zyklen. Mithilfe von Wasserstoff‑Deuterium‑Austausch‑Massenspektrometrie kartierten die Autoren, wie HSI#6 die Flexibilität verschiedener SecA‑Regionen umgestaltet. Die Verbindung lockert selektiv Bereiche des Proteins, die Klienten wahrnehmen und an den Kanal ankoppeln, und versteift gleichzeitig ein Gerüst‑Region, die wahrscheinlich die Bindungsstelle beherbergt. Das resultierende Bewegungsmuster ähnelt einem bereits engagierten, „eingeschalteten“ Zustand der Translokase und legt nahe, dass HSI#6 eine aktivierte Form stabilisiert — möglicherweise begünstigt es sogar ein monomeres SecA, das an den Kanal gebunden ist — ohne dass ein Klient vorhanden sein muss.
Warum das für Medizin und Biotechnologie wichtig ist
Indem gezeigt wird, dass ein kleines Molekül SecA allosterisch aktivieren und seine übliche Klientenselektivität aufheben kann, offenbart diese Arbeit einen neuen Weg, eine zentrale bakterielle Maschine zu kontrollieren. Für die Infektionsbekämpfung könnte eine solche erzwungene, unkontrollierte Sekretion Pathogene schwächen, indem sie Energie entzieht und ihre fein abgestimmten Exportprogramme stört — dadurch sind HSI#6‑ähnliche Aktivatoren attraktive Ausgangspunkte für die Antibiotikadesign‑Entwicklung oder als Leitmoleküle für die Herstellung künftiger Inhibitoren, die dieselben Regulationsmerkmale blockieren. Für die Biotechnologie könnte dasselbe Prinzip umfunktioniert werden, um die Sekretion nützlicher rekombinanter Proteine zu verbessern, ohne dass man auf konstruierte Signalpeptide oder aufwändige genetische Modifikationen angewiesen ist. Im Kern demonstriert die Studie, dass sich die bakterielle Protein‑„Verladestation“ chemisch umprogrammieren lässt und so neue Wege eröffnet, sowohl Mikroben zu bekämpfen als auch sie als mikroskopische Fabriken nutzbar zu machen.
Zitation: Sedky, H., Hamed, M.B., Krishnamurthy, S. et al. A small molecule allosterically activates SecA dependent secretion. Commun Biol 9, 368 (2026). https://doi.org/10.1038/s42003-026-09623-w
Schlüsselwörter: bakterielle Proteinsekretion, SecA-Translokase, allosterische Aktivierung, Kleinmolekül-Regulatoren, Entdeckung antibakterieller Wirkstoffe