Clear Sky Science · de
Ein Histidin‑Pseudokinase moduliert polares Wachstum und Zellform in Streptomyces venezuelae
Wie Bakterien filigrane verzweigte Körper bauen
Die filamentösen Bakterien der Gattung Streptomyces leben im Boden und bilden verzweigte Netzwerke aus Fäden, die mikroskopischen Pilzen ähneln. Diese Bakterien sind eine wichtige natürliche Quelle von Antibiotika, und ihr Erfolg beruht darauf, wie präzise sie steuern, wo und wie ihre Zellen wachsen. Diese Studie macht ein zuvor unbekanntes Protein sichtbar, das Streptomyces hilft, ihre wachsenden Spitzen stabil und ihre Verzweigungen geordnet zu halten, und liefert neue Einblicke darin, wie komplexe Zellformen aufgebaut und erhalten werden.
Wachstum nur an den Spitzen
Anders als viele vertraute stäbchenförmige Bakterien, die sich über ihre gesamte Länge ausdehnen, wachsen Streptomyces hauptsächlich an den Spitzen. Jeder Faden oder jede Hyphe verlängert sich dadurch, dass neue Zellwandbausteine nur in einer kleinen Zone ganz am Ende eingelagert werden. Diese Wachstumszone wird von einem Proteinkomplex organisiert, der als Polarisom bezeichnet wird. Im Zentrum steht ein Protein namens DivIVA, das dazu neigt, sich an gekrümmten Zellenden zu sammeln und den Ort zu markieren, an dem neues Wandmaterial eingebaut werden soll. Wenn sich kleine DivIVA‑Cluster vom Hauptzipfel abschnüren und sich entlang der Seite einer Hyphe niederlassen, können sie zu neuen Wachstumszonen heranreifen und so laterale Verzweigungen und ein fein verästeltes Myzel entstehen lassen.
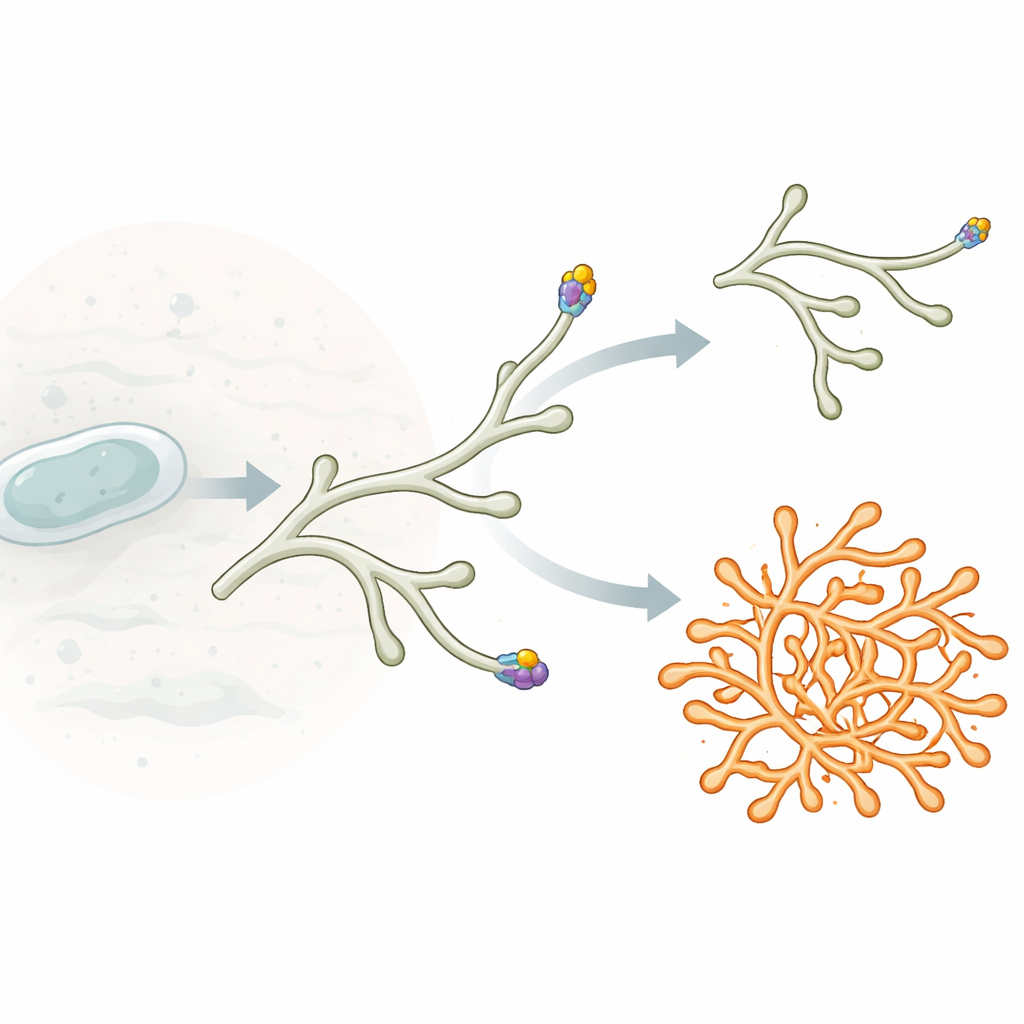
Ein neuer Formregler an der Spitze
Die Autor*innen suchten gezielt nach bislang unbekannten Komponenten des Streptomyces‑Polarisoms. Durch das Heranziehen von DivIVA aus Zelllysaten und die Analyse der mitgezogenen Partner entdeckten sie ein großes Protein, das sie PsmA (für polar growth and shape modulator A) nannten. PsmA ähnelt in seinem domänenhaften Aufbau einem verbreiteten bakteriellen Signalübertragungsenzym, der Histidinkinase: sensorähnliche Regionen, ein zentrales katalytisches Kernstück und eine Receiver‑Domäne, verbunden durch ein langes flexibles Segment. Eine genauere Analyse zeigte jedoch, dass PsmA wichtige Aminosäuren fehlt, die für die Phosphatübertragung erforderlich wären, und dass keine nachweisbare Kinaseaktivität vorliegt. Damit handelt es sich um eine „Pseudokinase“, die wahrscheinlich eher als struktureller oder Gerüstpartner denn als klassisches Enzym wirkt.
Wenn der Formregler fehlt
Um PsmAs Funktion zu erforschen, löschten die Forschenden sein Gen in Streptomyces venezuelae. Die Kolonien des Mutanten waren kleiner und dichter und zeigten eine pockennarbige Oberfläche. Unter dem Mikroskop erwiesen sich die vegetativen Hyphen als dicker, unregelmäßiger und wiesen deutlich vermehrte Verzweigung an den Spitzen auf. Statt sich glatt zu verlängern und gelegentlich Seitenzweige zu bilden, spalteten sich viele Spitzen in zwei oder mehr wachsende Enden auf und erzeugten so ein hyperverzweigtes, kompaktes Myzel. Wichtig ist, dass die Fähigkeit, Luftfilamente und Sporen zu bilden, weitgehend erhalten blieb, was darauf hindeutet, dass PsmA hauptsächlich während des vegetativen Spitzenwachstums wirkt und weniger in der späteren Sporulationsphase.
Die Wachstumszone zusammenhalten
Durch das Markieren von Proteinen mit Fluoreszenzmarkern visualisierten die Autor*innen, wo PsmA in lebenden Zellen lokalisiert ist. PsmA bildete fokale Punkte genau an der äußersten Spitze wachsender Hyphen und überlappte eng mit DivIVA sowie einem weiteren Spitzenprotein, Scy, war aber deutlich von FilP getrennt, das unmittelbar hinter der Spitze sitzt. In Abwesenheit von PsmA wurden die DivIVA‑Cluster an den Hyphenspitzen breiter und unregelmäßiger geformt. Zeitrafferaufnahmen zeigten, dass diese verzerrten Cluster deutlich verstärkt dazu neigten, in zwei ähnlich große Teile aufzuspalten. Jeder Teil trieb dann das Wachstum seiner eigenen Spitze voran, was zu Verzweigungen sehr nahe der ursprünglichen Spitze führte und das Muster der Hyperverzweigung erklärt. Wurde die PsmA‑Produktion im Mutanten wieder eingeschaltet, verengten sich die DivIVA‑Cluster rasch, die Spitzenform glättete sich und übermäßiges Aufspalten nahm ab.
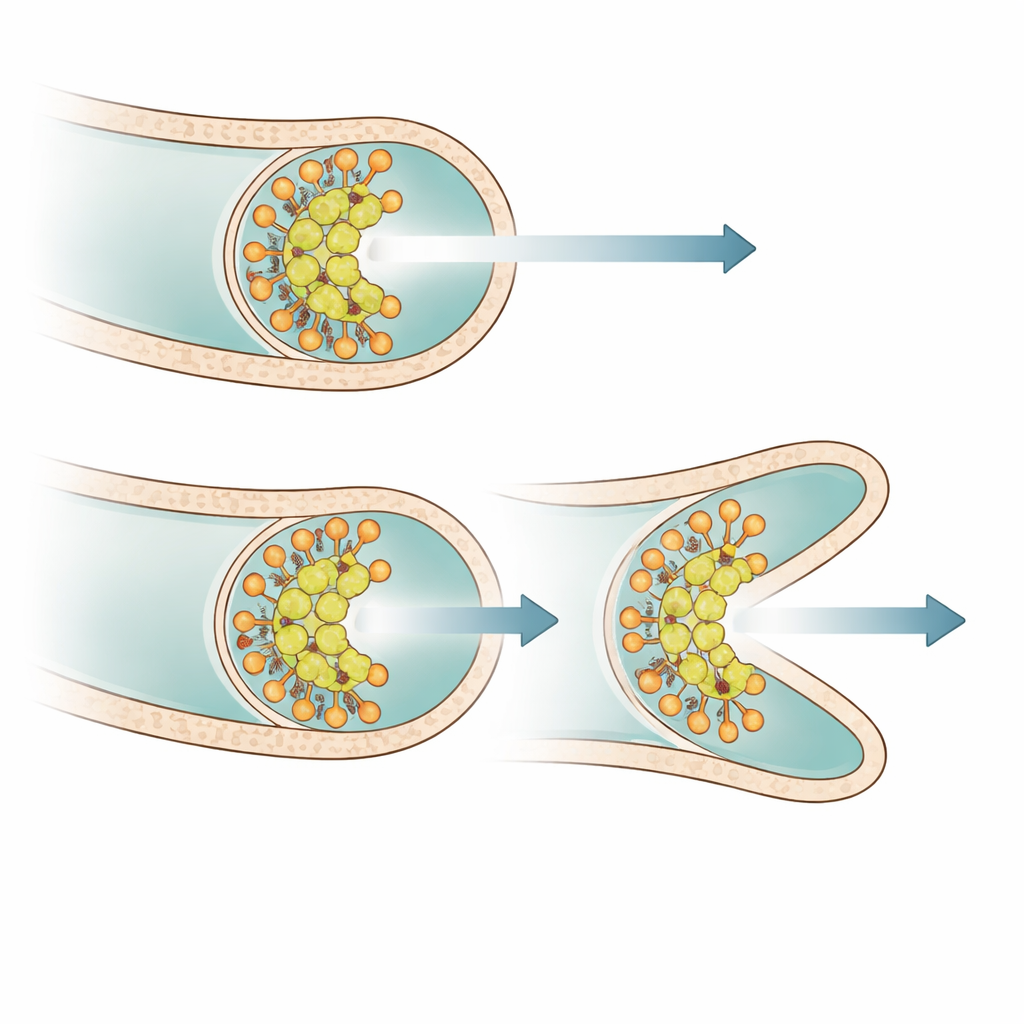
Parallel arbeitend mit anderen Spitzenfaktoren
PsmA ist nicht das einzige Protein, das Streptomyces‑Spitzen stabilisiert. Frühere Arbeiten hatten Scy und FilP identifiziert, zwei längliche, coiled‑coilartige Proteine, die mit DivIVA assoziieren und das Spitzenverhalten beeinflussen. Doppelmutanten, denen sowohl PsmA als auch entweder Scy oder FilP fehlten, zeigten noch schwerwiegendere Wachstumsdefekte und dichtere, verfilzte Myzelien als einfache Mutanten, blieben jedoch lebensfähig. Dieses Muster legt nahe, dass PsmA größtenteils parallel zu Scy und FilP wirkt: Alle drei tragen auf teils unabhängige Weise dazu bei, die Wachstumszone kohäsiv zu halten und zu verhindern, dass sie in mehrere konkurrierende Spitzen zerfällt.
Was das für bakterielle Architektur bedeutet
Zusammengefasst stellen die Ergebnisse PsmA als einen nicht‑enzymatischen Partner dar, der die Stabilität und Dynamik des DivIVA‑basierten Polarisoms an Streptomyces‑Hyphenspitzen feinabstimmt. Statt Gene über klassische Signalwege ein‑ oder auszuschalten, scheint PsmA direkt am wachsenden Ende zu wirken, vermutlich als struktureller Organisator, der DivIVA‑Cluster dabei unterstützt, eine fokussierte Einzelwachstumszone aufrechtzuerhalten. Fehlt PsmA, wird die Spitzenausrüstung zu instabil, spaltet sich zu oft und führt zu übermäßiger Verzweigung. Das Verständnis dieser Form lokaler architektonischer Kontrolle vertieft nicht nur unser grundlegendes Wissen über bakterielle Zellbiologie, sondern kann auch Bemühungen informieren, Streptomyces‑Wachstumsmuster für Biotechnologie und Antibiotikaproduktion zu manipulieren.
Zitation: Singh Mavi, P., Flärdh, K. A histidine pseudokinase modulates polar growth and cell shape in Streptomyces venezuelae. Commun Biol 9, 345 (2026). https://doi.org/10.1038/s42003-026-09620-z
Schlüsselwörter: Streptomyces, Zellpolarität, bakterielle Morphogenese, Pseudokinase, hyphale Verzweigung